Clear Sky Science · ar
تنافس ترتيب الروابط الهيدروجينية يقود التوتر السطحي الشاذ للماء
لماذا سطح الماء أغرب مما يبدو
يسمح سطح الماء للحشرات بالمشي فوق البرك، ويشكل قطرات المطر، ويحدد كيفية تشكّل وانفجار الفقاعات. ومع ذلك، عندما يقيس العلماء مدى «شدة» هذا السطح — أي التوتر السطحي — يجدون أن سلوك الماء يصبح مفاجئًا على نحو غريب مع انخفاض درجة الحرارة، لا سيما عندما يبرد إلى ما دون نقطة التجمد الاعتيادية. تكشف هذه المقالة عبر محاكيات حاسوبية متقدمة كيف يفسر التنظيم الخفي لجزيئات الماء عند السطح هذا اللغز القديم.
نوعان خفيان من ماء سائل
مع أننا نخبر تجربة الماء كسائل بسيط ومتماثل، يمكن لجزيئاته أن ترتب نفسها محليًا بطريقتين متباينتين. أحد الترتيبين أكثر اكتظاظًا وفوضوية؛ يسمي الباحثون هذه الحالة حالة ρ. الآخر أكثر انفتاحًا وتناسقًا، حيث يحيط بكل جزيء نمط رباعي تقريبا (تتراهيدرالي)؛ تسمى هذه الحالة حالة S. أشارت أعمال سابقة إلى أن التوازن بين هذين النمطين المحليين يساعد في تفسير العديد من خصائص الماء الغريبة في الحالة الكلية. هنا، يسأل المؤلفون كيف يتجلّى نفس نموذج الحالتين عند واجهة الهواء–الماء، حيث يولد التوتر السطحي.
كيف يجذب السطح الجزيئات لتتماشى
عند الحد الفاصل بين الهواء والماء، لم تعد الجزيئات تشعر بجذب متساوٍ من كل الاتجاهات. تكسر هذه اللاتماثل يفضّل جزيئات حالة ρ التي تستطيع ذرات الهيدروجين والقطب الجزيئي فيها الانحناء بسهولة في اتجاه مفضّل. تُظهر المحاكيات أنه بالقرب من درجة حرارة الغرفة وما دونها بقليل، تصبح الطبقة العلوية جدًا من الماء مشبعة بهذه الجزيئات المصطفة من حالة ρ، بينما تكثر جزيئات حالة S تحت السطح بقليل وفي الحجم الكلي. وبما أن جزيئات حالة ρ تصطف بقوة، فإنها تخلق عدم توازن في القوى — أي لا تماثل إجهاد — يُولّد توترًا سطحيًا نسبيًا كبيرًا مقارنةً بالسوائل العادية مثل البنزين.
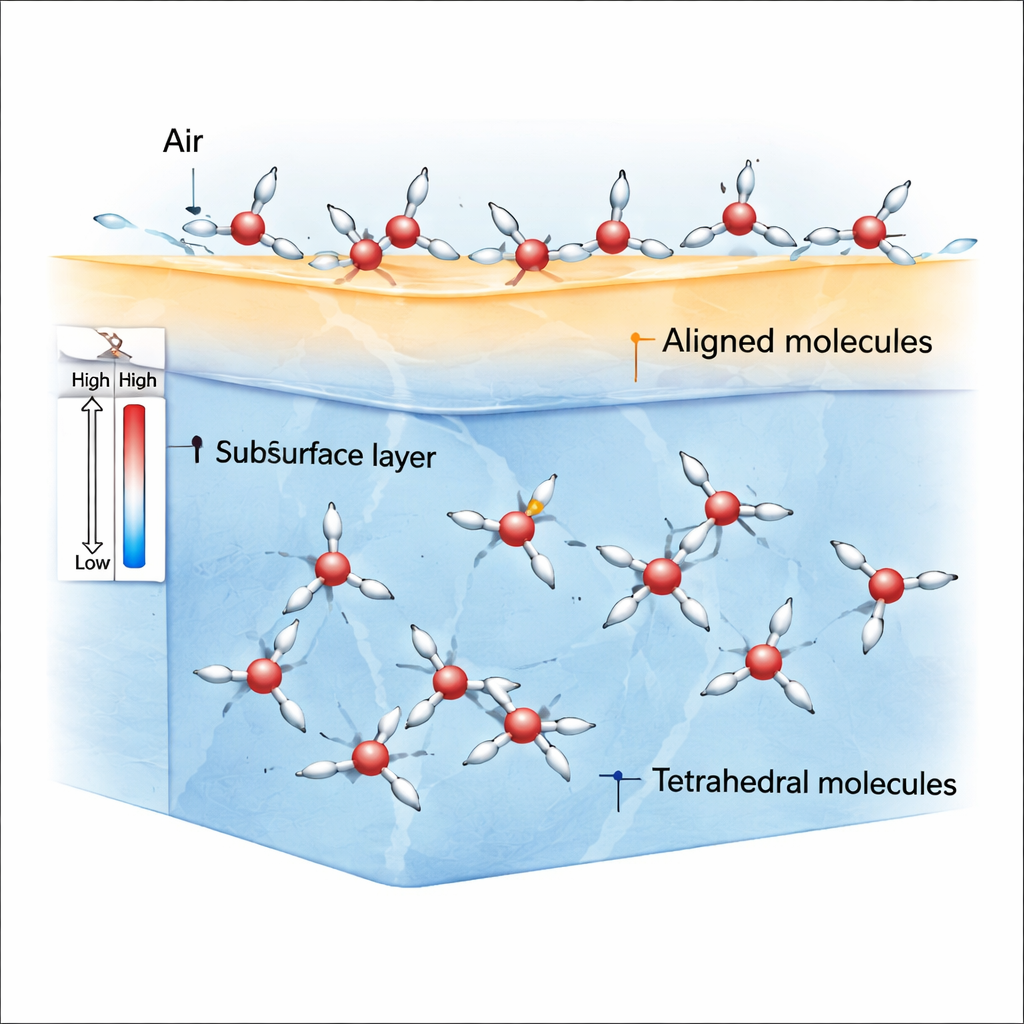
لماذا يبطئ التبريد أولًا ثم يسرّع تشديد السطح
في معظم السوائل البسيطة، يؤدي التبريد إلى تشديد السطح تدريجيًا، مما يجعل التوتر السطحي يرتفع تقريبًا بشكل خطّي. يفعل الماء ذلك فقط عند درجات الحرارة الأعلى. مع تبريده باتجاه نحو −0.15 °C (275 K)، يبدأ ارتفاع التوتر السطحي في التباطؤ. تُبيّن المحاكيات أن هذا التباطؤ يحدث لأن جزيئات حالة ρ عند السطح أصبحت مصفوفة إلى أقصى حد؛ فالتبريد الإضافي يكاد لا يغيّر مساهمتها. وفي الوقت نفسه، تظل جزيئات حالة S تحت السطح عشوائية التوجيه إلى حد كبير، لذا فهي لا تضيف كثيرًا إلى إجهاد السطح. النتيجة الصافية تشبه نوعًا من الهضبة: تستمر درجة الحرارة في الانخفاض، لكن التوتر السطحي ينمو ببطء.
التبريد العميق فوق المبرد يُطلق تشديدًا ثانٍ
عندما يُبرَّد الماء أكثر بكثير، إلى ما هو أدنى بكثير من نقطة تجمده الاعتيادية في نطاق التبريد العميق (حوالي 250 K وما دون)، يتغير سلوكه مرة أخرى. ترتفع نسبة هياكل حالة S الرباعية بشكل حاد، حتى قرب السطح. والأهم أن جزيئات حالة S هذه لا تعود تشير في اتجاهات عشوائية. تبدأ أقطابها في الاصطفاف على طول الاتجاه العمودي على السطح، مدفوعة بتفاعلات بين أقطاب الجزيئات المجاورة وبمنطقة ضغط سالب تحت السطح مباشرة. عند حصول ذلك، ينقلب دور ماء حالة S من مُرخٍ للتوتر السطحي إلى معزّز له. هذه الإضافة المرتبة تولّد زيادة متجددة وأسرع — الارتفاع «العاود» — في التوتر السطحي عند درجات الحرارة المنخفضة.
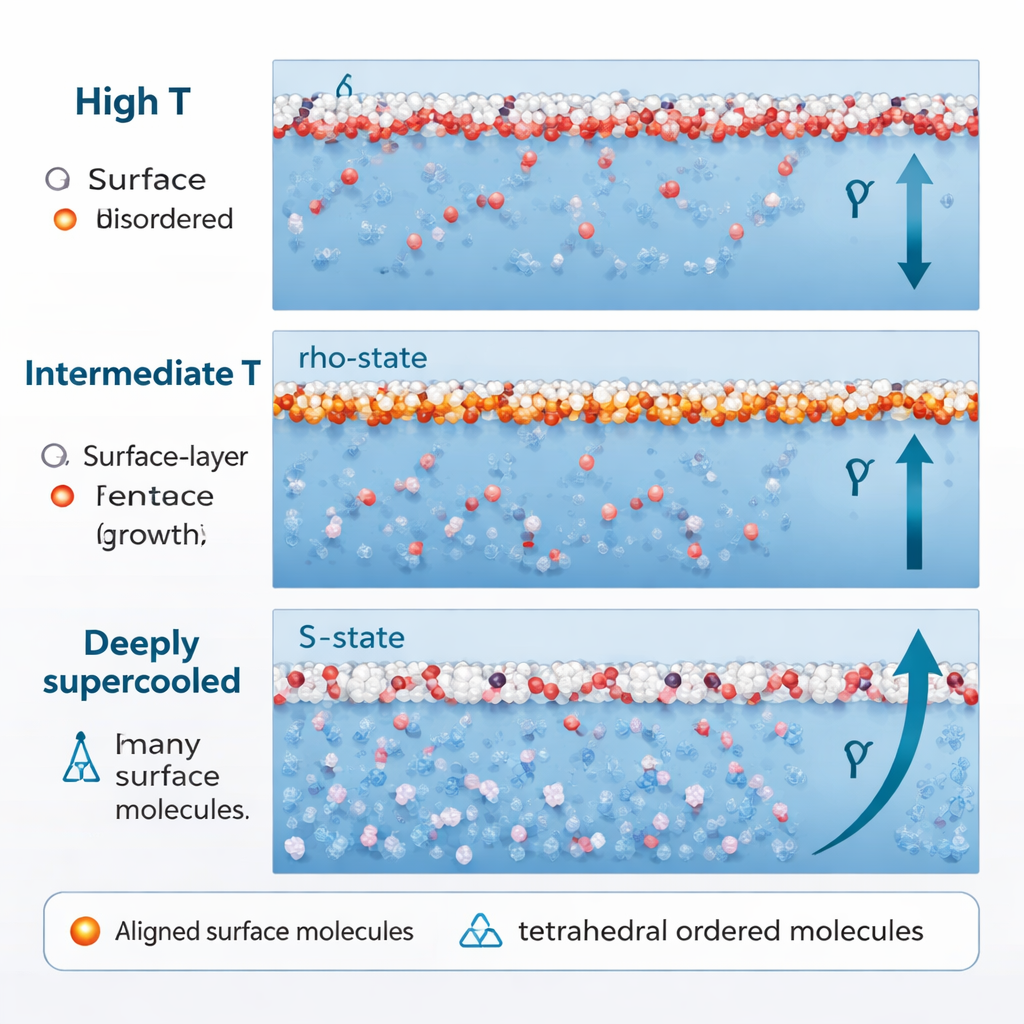
من ألغاز السطح إلى الجليد وما بعده
تتشابه عناقيد حالة S الرباعية ذاتها التي تقسِّي السطح عند درجات الحرارة المنخفضة مع اللبنات الأولية لعدة أشكال من الجليد، وتجد المحاكيات أنها متراكمة قرب الواجهة. هذا يعني أن حدّ الهواء–الماء يمكن أن يعمل مَهْدًا لتكوّن الجليد، مما يساعد على تفسير لماذا يبدأ التجمد غالبًا عند الأسطح. وعلى نحو أوسع، توفر الدراسة رابطًا ملموسًا على مستوى الجزيئات بين كيفية ترتيب وتوجيه جزيئات الماء ومدى قوة جذب السطح إلى الداخل. تصور البنية–الميكانيكا هذا لا يحل فقط منحنى درجة الحرارة الغريب لتوتر سطح الماء، بل يقدم أيضًا خارطة طريق لفهم والتحكم بالظواهر الواجهية في سوائل أخرى مكوّنة لشبكات، من الماء فوق المبرد في السحب إلى مواد تُستخدم في التكنولوجيا والبيولوجيا.
الاستشهاد: Yuan, J., Qiu, K., Sun, G. et al. Competing hydrogen-bond orders drive water’s anomalous surface tension. Nat Commun 17, 1498 (2026). https://doi.org/10.1038/s41467-026-69356-6
الكلمات المفتاحية: توتر سطح الماء, الترابط الهيدروجيني, الماء فوق المبرد, بنية السائل, نواة التجمّد