Clear Sky Science · ar
تآزر STING مع TOX لقمع تعبير HO-1 لتحفيز الفيروپتوسيس في خلايا CD8+ المتوغلة في الورم ومقاومة العلاج المناعي
لماذا يهم هذا البحث لعلاج السرطان
تعمل علاجات المناعة الحديثة للسرطان عن طريق إطلاق العنان لخلايا ت القاتلة في الجسم، ومع ذلك تظل العديد من الأورام قادرة على إيقاف هذه الخلايا. يكشف هذا البحث عن مفتاح تدمير ذاتي خفي داخل خلايا CD8+ «القاتلة» تستغله الأورام، ويُظهر كيف يؤدي تعطيل هذا المفتاح إلى جعل العلاج المناعي أقوى بكثير.
مسار موت خفي داخل خلايا ت المقاتلة للأورام
داخل الورم، من المفترض أن تطارد خلايا CD8+ الخلايا السرطانية وتدمرها. بدلاً من ذلك، غالباً ما تصبح نادرة وبطيئة وقصيرة العمر. ركز الباحثون على جزيئين داخل الخلايا التية—STING، مستشعر تلف الحمض النووي، وTOX، بروتين مرتبط بإرهاق الخلايا التية. هندسوا فئراناً تفتقر خلايا CD8+ لديها إلى STING أو TOX أو كلاهما، ثم زرعوا أنواعا عدة من الأورام. وعلى نحو مفاجئ، قضت الفئران التي افتقدت خلاياها التية إما STING أو TOX على الأورام بشكل أفضل بكثير. نمت أورامها بشكل أبطأ، واحتوت على عدد أكبر بكثير من خلايا CD8+، وكانت هذه الخلايا تنتج كميات أكبر من الجزيئات القاتلة للسرطان مثل الإنترفيرون-غاما والگرانزيم B. وقد دلّ ذلك على وجود برنامج داخلي كان يخرب الخلايا التية داخل الأورام بهدوء.
كيف يضعف الموت المعتمد على الحديد المناعة
من خلال فحص نشاط الجينات في الخلايا التية المتوغلة في الورم، وجد الباحثون أن الخلايا التية العادية داخل الأورام كانت مهيأة لشكل معين من الموت الخلوي يُدعى الفيروپتوسيس. على عكس الاستماتوپتوز (الاستماتة)، يُثار الفيروپتوسيس بفرط حمولة الحديد وتراكم الدهون المؤكسدة في أغشية الخلايا. في خلايا CD8+ العادية المعرضة للخلايا الورمية، كانت الجينات التي تعزز تراكم الحديد وتلف الدهون مفعَّلة، بينما كانت الجينات الوقائية مخفَّضة. بالمقابل، أظهرت الخلايا التية الخالية من STING أو TOX النمط المعاكس: عبّرت عن كميات أكبر من الإنزيمات الوقائية HO-1 وGPX4، وكان لديها مستويات حديد أقل، وتأكسد دهون أقل في الأغشية، ومتكَّرات صحية أكثر، ومقاومة للموت الفيروپتوتي. أكدت اختبارات المختبر أن حجب الفيروپتوسيس كيميائياً يبقي الخلايا التية العادية على قيد الحياة، بينما جعلت إزالة STING أو TOX هذه الخلايا مقاومة بطبيعتها.
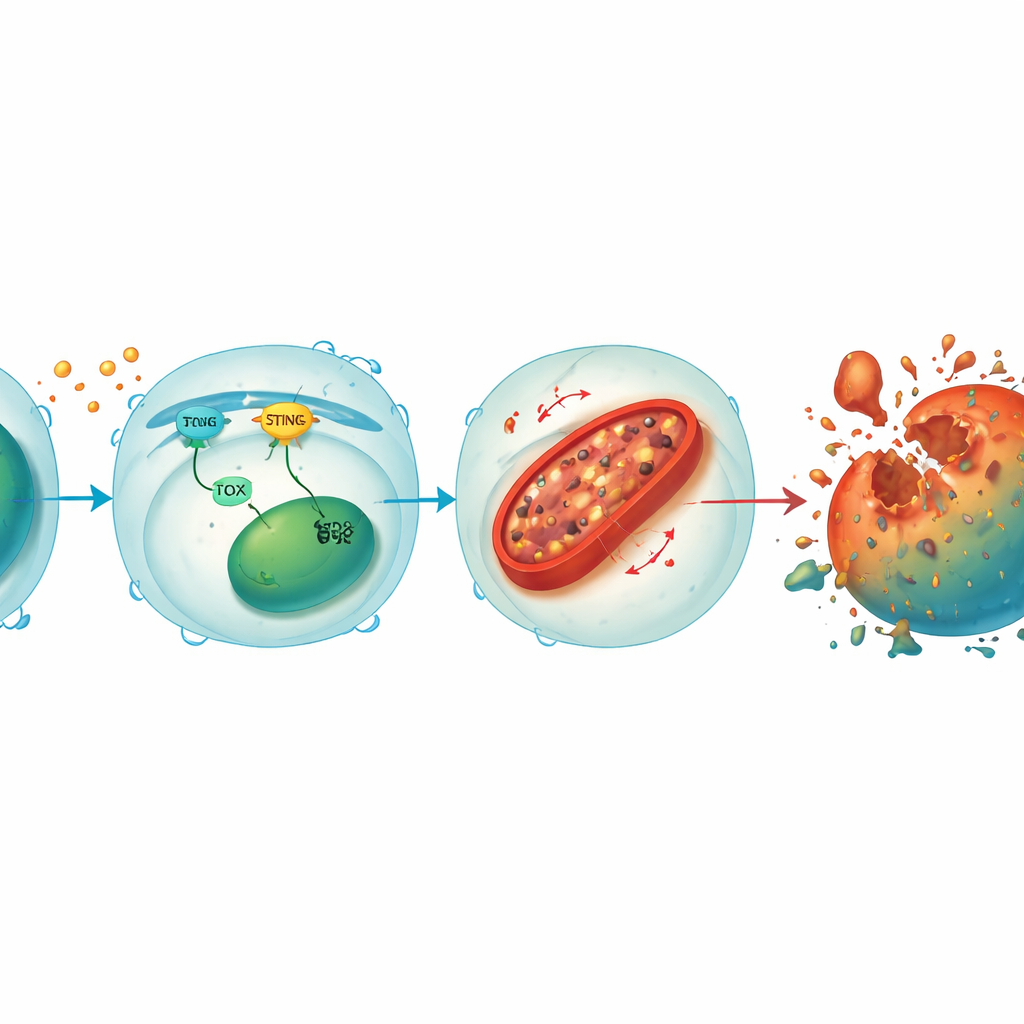
حلقة تربط إشارات الإجهاد بتلف الميتوكندريا
بتعمق أكبر، اكتشف الفريق أن STING وTOX يشكلان حلقة تعزيزية داخل خلايا CD8+ التية. عندما تنشط إشارات ورمية أو فيروسية STING، فإنها تحفز عوامل أدنى تسهم في رفع مستوى TOX، ويُسهم TOX بدوره في الحفاظ على نشاط STING. معاً، يقومان بقمع HO-1، وهو إنزيم يساعد عادة في ضبط الحديد داخل الخلية. مع كبت HO-1، يتراكم الحديد في الميتوكوندريا—مصانع طاقة الخلية—مما يؤدي إلى مستويات عالية من الجذور التفاعلية للأكسجين وأكسدة دهون الأغشية. يتسبب هذا التلف الميتوكوندري في استنزاف إنتاج الطاقة ويدفع الخلية التية في نهاية المطاف نحو الفيروپتوسيس. إعادة STING أو TOX في الخلايا المعدّلة أعادت حمولة الحديد والموت الخلوي، بينما جعل خفض HO-1 أكثر جعل حتى الخلايا المحمية عرضة مجدداً، مؤكداً دور HO-1 كفرامل مركزية لهذا المسار المدمر.
كيف يشغّل اللاكتات المصنعه من الورم المفتاح
بيئة الورم الغنية باللاكتات، ناتج ثانوي لتمثيل السرطان المعدَّل. يظهر البحث أن هذا اللاكتات ليس مجرد نفاية أيضية—بل يساعد فعلياً في قلب مفتاح الفيروپتوسيس في الخلايا التية. بالمقارنة مع خلايا أخرى، كانت خلايا CD8+ حساسة بشكلٍ خاص للاكتات. عند دخول اللاكتات إلى الخلايا عبر ناقلات محددة، تسبب تراكم الحديد، انكماش الميتوكوندريا، فقدان الحمض النووي الميتوكوندري، ومزيداً من التلف التأكسدي. في نفس الوقت، عزز اللاكتات نشاط STING وTOX وقمع HO-1 بشكل إضافي. كانت الخلايا التية الخالية من STING أو TOX أكثر مقاومة بكثير لإصابات اللاكتات. حجب ناقل لاكتات رئيسي بدواء (AZD3965) حمى خلايا CD8+ من الفيروپتوسيس في الفئران، وزاد وجودها داخل الأورام، وأبطأ نمو الورم، مقلداً الفائدة الناتجة عن حذف STING جينياً في الخلايا التية.
تحويل نقطة ضعف إلى ميزة علاجية
لهذه الرؤى الآلية تطبيقات عملية. عندما استخدم الباحثون علاج الخلايا بالتبني—حقن فئران بخلايا تية منشطة مخبرياً—وجدوا أن الخلايا التية المصممة لتفتقد STING أو TOX أنتجت سيطرة على الورم أقوى بكثير من الخلايا التية العادية. علاوة على ذلك، أدى الجمع بين هذه الخلايا «المقاومة للفيروپتوسيس» والعلاجات القائمة مثل حاصرات نقاط التفتيش PD-1 أو TIM-3، أو عقار سيسبلاتين الكيمياوي، أو دواء منشط لـSTING إلى تقلص أورام أفضل بكثير من أي علاج منفرد. أخيراً، في عينات أورام من مرضى بسرطان عنق الرحم، ارتبطت مستويات TOX الأعلى وHO-1 الأقل في الخلايا اللمفاوية المتوغلة في الورم ببقاء أسوأ، مما يوحي بأن هذا المسار يشكل أيضاً النتائج السريرية لدى البشر.
ماذا يعني هذا لرعاية السرطان المستقبلية
بعبارات بسيطة، يكشف البحث أن الأورام يمكن أن تجبر أفضل خلايانا التية المقاتلة للسرطان على الصدأ من الداخل عن طريق دفع شكل موت خلوي مدفوع بالحديد. حلقة اللاكتات–STING–TOX تخفّض الحماية التي يوفرها HO-1، تتلف الميتوكوندريا، وتؤدي إلى الفيروپتوسيس، ما يخفف صفوف خلايا CD8+ الفعالة. تعطيل هذه الحلقة—عن طريق هندسة خلايا تية تفتقد STING أو TOX، تعزيز HO-1، أو حجب دخول اللاكتات—يبقي الخلايا التية حية، نشطة، وجاهزة للهجوم. يشير هذا العمل إلى أجيال جديدة من العلاجات المناعية التي تجمع بين ضبط أيضي وجيني للخلايا التية مع الأدوية الحالية لتجاوز المقاومة وتقديم سيطرة سرطانية أكثر دواماً.
الاستشهاد: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
الكلمات المفتاحية: المناعات ضد السرطان, خلايا CD8 T, الپيروپتوسيس, بيئة الورم الدقيقة, مسار STING TOX HO-1