Clear Sky Science · ar
Seq-Scope-eXpanded: علم الأمُوْم المكاني أبعد من دِقة البَصَر البصري
رؤية الخلايا بتفصيل أوضح
أجسامنا مبنية من عدد هائل من الخلايا الصغيرة، وكل واحدة تنشط بعمليات غالباً ما لا نراها حتى باستخدام مجاهر قوية. تعرض هذه الورقة تقنية Seq-Scope-X، التي تتيح للباحثين تكبير بنية الأنسجة الداخلية بدقة غير مسبوقة، مع رسم خرائط للجينات والبروتينات النشطة في نقاط دقيقة داخل الخلايا وبينها. هذا المستوى من التفصيل قد يغيّر طريقة دراستنا للتطوّر، والجهاز المناعي، وأمراض مثل السرطان أو إصابات الكبد.
لماذا نرسم خرائط الجزيئات في موضعها؟
الخلايا لا تعمل بمعزل: فهي تعيش في أحياء، وتكوّن طبقات، وتتخصّص بحسب مكانها. تقنيات تسلسل الجينات التقليدية تفكّك الأنسجة وتفقد هذا البُعد المكاني. أدوات «الأمُوْم المكانية» الحديثة تحتفظ بالجزيئات في مواضعها، لكن ثمة مقايضة. الطرق المعتمدة على التصوير ترى تفاصيل دقيقة جداً لكنها عادة تتتبّع مجموعة محدودة من الجينات. أما الطرق القائمة على التسلسل فتقرأ تقريباً كل الجينات دفعة واحدة، لكنها تُغَيّب التفاصيل الدقيقة، غالباً بتمويه الإشارات على عدة ميكرومترات — أكبر من كثير من البُنى تحت خلوية. هدف المؤلفين كان سد هذه الفجوة: الاحتفاظ بالقراءة الشاملة وغير المتحيّزة للتسلسل، مع الوصول إلى دقة تضاهي أو تتفوق على مجاهر اليوم.
تمدّد الأنسجة لتجاوز حدود البَصَر البصري
الفكرة الأساسية وراء Seq-Scope-X بسيطة بشكل خادع: تكبير النسيج نفسه بلطف بحيث يصبح كل نانومتر أصلي أسهل في الفصل. أولاً يثبّت الفريق جزيئات الـRNA — أو وسمات DNA مرتبطة بالأجسام المضادة — داخل هلام مائي مرن يُبنى حول شريحة النسيج. ثم يهضمون النسيج الأصلي وينفخون الهلام في محلول مالح، موسّعين البنية نحو ثلاث مرّات مع الحفاظ على المواقع النسبية بصورة شبه سليمة. يوضع هذا الهلام الموسّع فوق شريحة تسلسل فائقة الكثافة مغطاة بمجمّعات الالتقاط. وبالتسخين المتحكّم تُطلق الجزيئات المثبتة من الهلام وتُعاد ربطها بالشريحة، التي تُسلَّل لاحقاً لتكشف أي الجينات أو البروتينات وُجدت في كل إحداثي صغير. 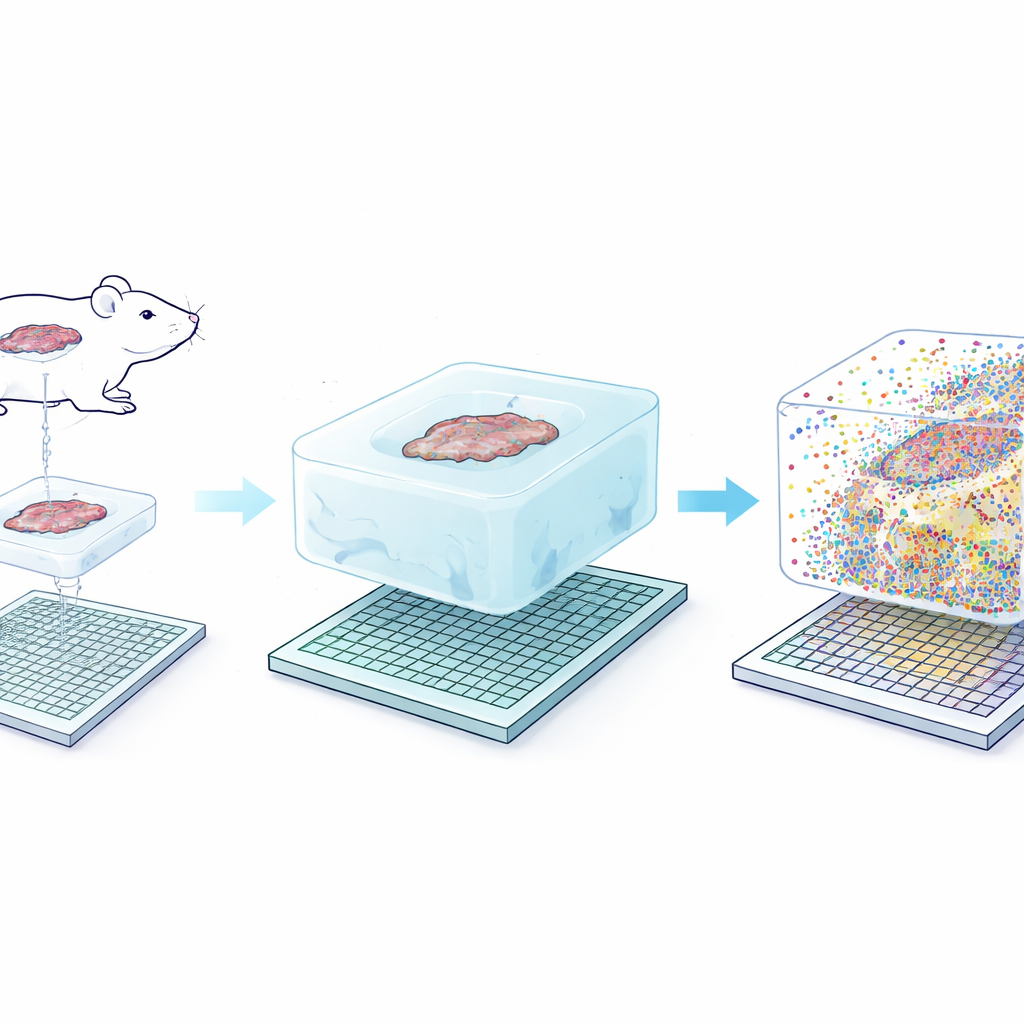
من خلايا مبهمة إلى خرائط تحت خلوية
عندما طبّق الباحثون Seq-Scope-X على كبد الفأر، وجدوا أن الطريقة حَسّنت الدقة المكانية من نحو 0.6 ميكرومتر إلى حوالي 0.2 ميكرومتر وزادت عدد المواضع القابلة للقياس لكل مليمتر مربع بما يقارب عشرة أضعاف. عملياً، ما كان يبدو كتجمعات ضبابية من الإشارة أصبح الآن حدوداً حادة للخلايا الفردية. والأكثر لفتاً أن مجموعات الـRNA غير المكتملة المعالجة (غير مرتبطة تماماً) تركزت بإحكام حول مراكز النوى، بينما رسمت الـRNA الناضجة (المعالجة) محيط السيتوبلازم. سمح ذلك للمؤلفين برسم حدود الخلايا باستخدام الـRNA وحده وفصل قراءات الجينات النووية عن السيتوبلازمية لما يقرب من كل خليّة كبدية في النسيج — ما كانت طرق التسلسل السابقة تلمّح إليه فقط.
خلايا ذات هويّتان منفصلتان
بفضل هذه الوضوحية الجديدة، اكتشف الفريق نوعاً غير متوقع من «الحياة المزدوجة» الجزيئية داخل خلايا الكبد. على طول التدرّج المعروف من الأوعية الدموية عند الجانب البابي للفصيص الكبدي إلى الجانب المركزي، تتخصّص الخلايا الكبدية في مهام أيضية مختلفة. أظهر Seq-Scope-X أنه في كثير من الخلايا لا تتطابق أنماط الجينات في النواة مع الأنماط في السيتوبلازم المحيط. بدا أن نحو ثلث الخلايا الكبدية تمتلك ملفاً نووياً يتماشى مع منطقة ما وملفاً سيتوبلازمياً يتماشى مع منطقة مجاورة. طرق تصوير مستقلة، بما في ذلك MERFISH وتجارب التصوير الفلوري للـRNA الجزيئية المنفردة، أكّدت أن النسخ الفردية يمكن أن تتجمع إما في النواة أو في السيتوبلازم. مجتمعة، تقترح هذه النتائج أن الخلايا الكبدية قد تغيّر أدوارها الأيضية ديناميكياً مع الزمن، بحيث تتهيأ النواة لحالة مستقبلية بينما يعكس السيتوبلازم الحالة الجارية. 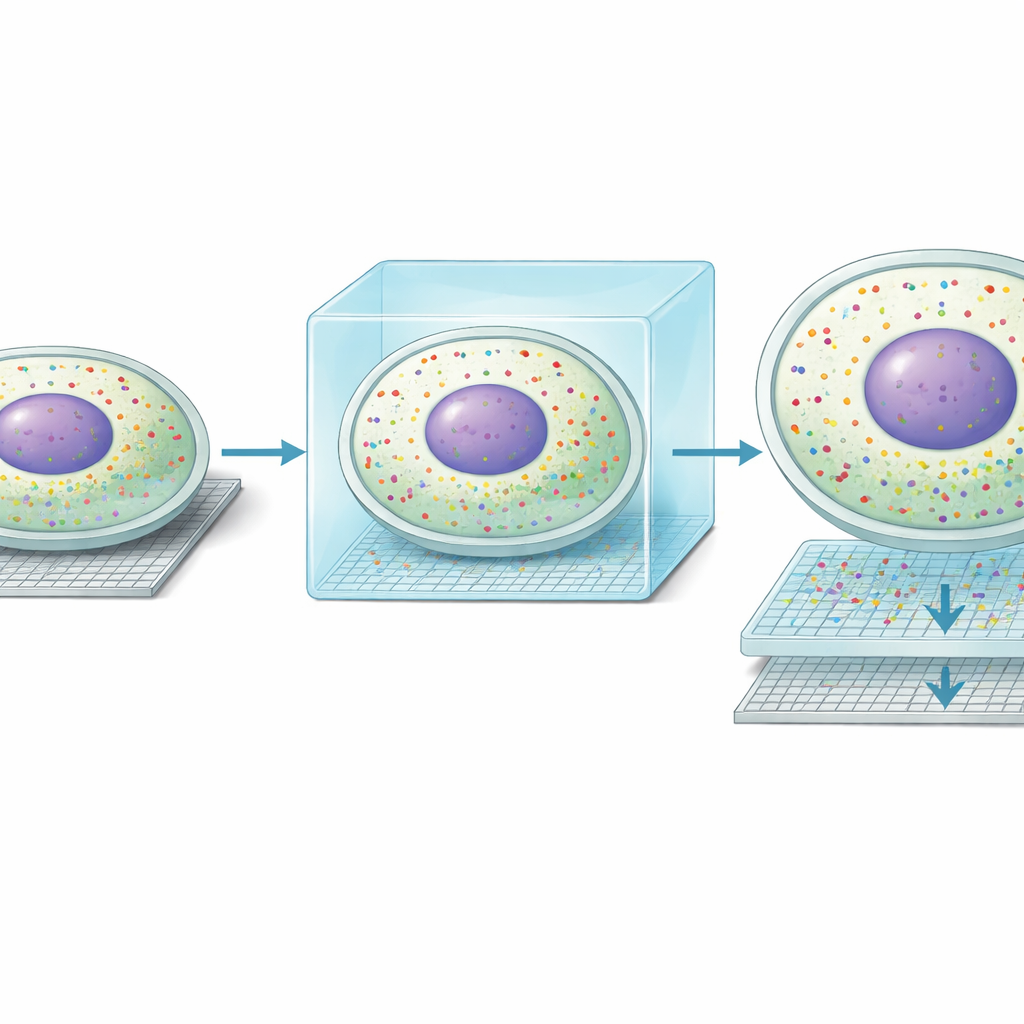
ما وراء الكبد: المخ، الأمعاء والأنسجة المناعية
اختبر المؤلفون بعد ذلك ما إذا كانت Seq-Scope-X تعمل في أعضاء أخرى. في المخ، فصلت بوضوح بين أنواع الخلايا العصبية والخلايا الداعمة وكشفت أنماطاً تحت خلوية للـRNA حول النوى. في القولون، مكنت من تمييز أنماط فرعية مختلفة من خلايا الكُغّطة وطبقات الخلايا المعوية على طول المحور من التجويف إلى السطح، مجدداً مع التقاط توقيعات نووية. وربما بشكل أكثر دراماتيكية، عدّل الفريق الطريقة لتشمل البروتينات باستخدام أجسام مضادة مرمّزة بـDNA في طحال الفأر وحنك الإنسان. استطاعت Seq-Scope-X رسم خرائط لأكثر من مئة وسم سطحي خلوي مختلف بدقة خلية مفردة، مميزة مجموعات T وB المكدّسة والمتجاورة والخلايا النخاعية. وبالتحوّل إلى كيمياء هلامية أكثر قابلية للتمدد، دفعوا الدقة الفعّالة نحو النطاق النانوي الحقيقي مع الحفاظ على بنية النسيج بما يكفي للخرائط التفصيلية.
ماذا يعني هذا للمستقبل
تُظهر Seq-Scope-X أن تكبير الأنسجة فعلياً قبل التسلسل يمكن أن يتجاوز حدود الدقة الطويلة الأمد، مقدّمة تفصيلاً يوازي مستوى المجهر مع قراءة آلاف الجينات أو وسمات البروتين دفعة واحدة. للمراقب العام، يعني هذا أن العلماء باتوا قادرين على بناء «أطالس جزيئية» لا تقول فقط أين توجد الخلايا، بل تكشف أيضاً ما يحدث داخل أجزاء مختلفة من كل خلية. قد تساعد مثل هذه الخرائط في تفسير كيف تستجيب الأنسجة للإصابة، وكيف تنظم الخلايا المناعية نفسها في الأعضاء اللمفاوية والأورام، أو كيف تنذر التحولات الطفيفة داخل الخلايا بحدوث المرض. على الرغم من أن مزيداً من التحسينات ضرورية لتوسيع التغطية وتحسين بعض لوحات الصبغ، تفتح Seq-Scope-X نافذة قوية جديدة على المناظر المجهرية الكامنة وراء الصحة والمرض.
الاستشهاد: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
الكلمات المفتاحية: التعبير الجيني المكاني, توسيع الأنسجة, علم الأمُوْم على مستوى الخلية الواحدة, البروتيومات المكانية, تقسيم الكبد إلى مناطق