Clear Sky Science · ar
إنزيم CD38 يحلل MAVS عبر البلعمة الميتوكوندرية ليثبط إفراز الإنترفيرون من النوع الأول في خلايا سرطان البلعوم الأنفي ويضعف مناعة الخلايا CD8+T المضادة للأورام
لماذا هذا مهم لعلاج السرطان
سرطان البلعوم الأنفي ينشأ خلف الأنف ويشيع بشكل خاص في شرق وجنوب شرق آسيا. أدت الأدوية المناعية التي تفرج عن خلايا T في الجسم إلى تغيير توقعات المريضين في بعض الحالات، لكن معظم المرضى لا يستفيدون. تكشف هذه الدراسة عن فرامل مخفية داخل خلايا الورم نفسها: جزيء يُدعى CD38 الذي يطفئ بهدوء نظام إنذار داخلي ويضعف هجوم خلايا CD8 القاتلة للسرطان. فهم هذه الفرامل وتعطيلها قد يجعل العلاجات المناعية الحالية فعالة لعدد أكبر من الناس.
مفتاح خفي على خلايا الورم
ركز الباحثون على CD38، وهو بروتين يوجد على العديد من الخلايا المناعية لكنه موجود أيضاً على خلايا سرطان البلعوم الأنفي. ربطت أعمال سابقة CD38 بمقاومة أدوية نقاط التفتيش الشهيرة التي تستهدف PD-1 وPD-L1. هنا تساءل الفريق عما إذا كان CD38 داخل خلايا الورم يغيّر مباشرة مدى قدرة خلايا CD8 على التعرف على هذه الخلايا وتدميرها. بواسطة زرع خلايا ورمية بشرية مع أو بدون CD38 جنباً إلى جنب مع خلايا CD8 بشرية مفعّلة، وجدوا أن إزالة CD38 من خلايا السرطان جعلت خلايا T أقوى بكثير: أفرزت مستويات أعلى من جزيئات الهجوم الرئيسة، ونجت بشكل أفضل، وقتلت المزيد من خلايا الورم. وعند إعادة إضافة CD38، تراجعت وظائف الخلايا T، ما يشير إلى أن CD38 يعمل ككابح جوهري داخل الورم للهجوم المناعي.
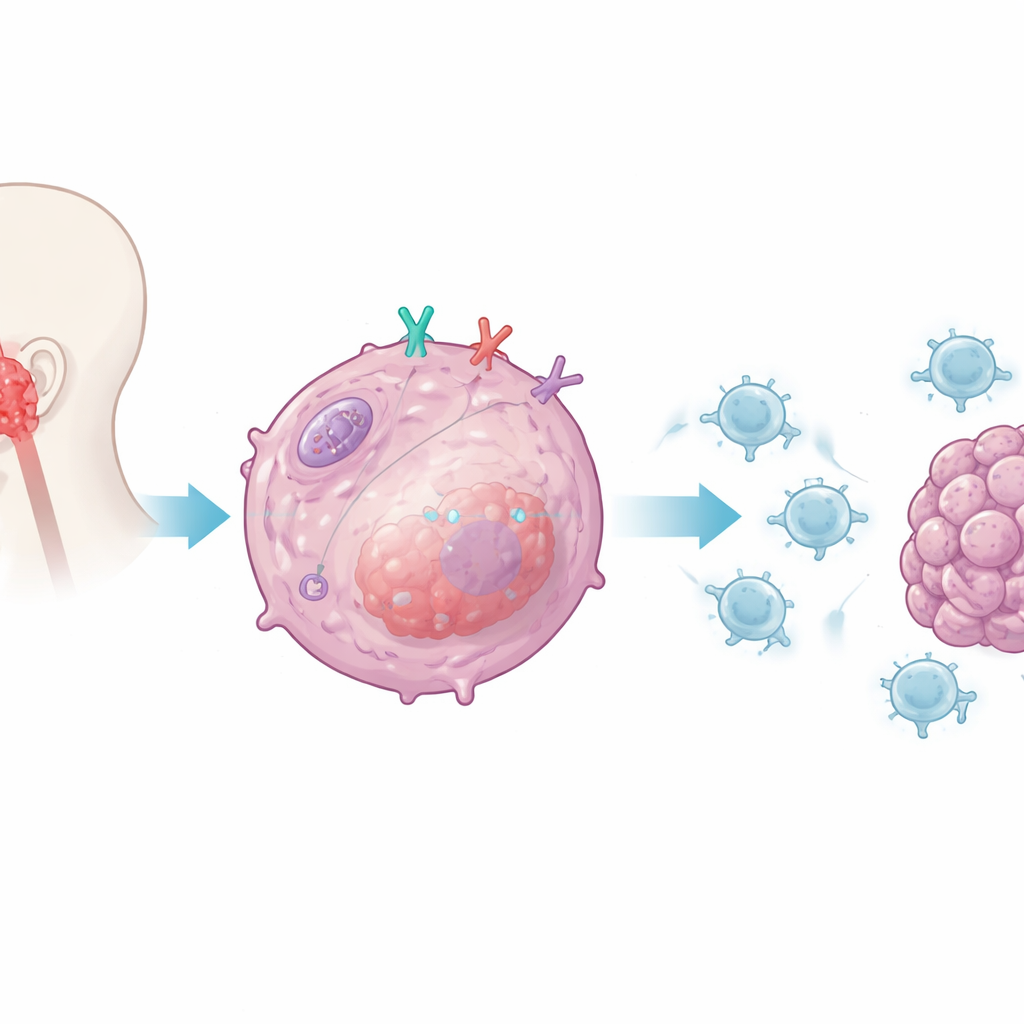
خفض إنذار الخلية الداخلي
بعد ذلك بحث الفريق كيف يرسل CD38 هذه الإشارة القامعة. ركزوا على نظام إنذار الخلية الفطري، الذي يكتشف عادةً مادّة وراثية شبيهة بالفيروس ويشغّل الإنترفيرونات من النوع الأول—رسالٍة منشطة قوية للمناعة. في خلايا الورم الخالية من CD38، لاحظ الباحثون ارتفاعاً قوياً في الإنترفيرون-بيتا وفي الكيموكينات التي تجذب خلايا CD8 إلى الأورام. أظهروا أن CD38 يثبط بشكل انتقائي المسار المسيطر عليه بواسطة المستشعر الداخلي RIG-I وبروتين المراسل الخاص به MAVS، الذي يقع على الميتوكوندريا، مصانع طاقة الخلية. عندما كان CD38 موجوداً، كان تفعيل هذا المسار وجزيئات الإشارة المنتَجة عنه مخففاً؛ وعند إزالة CD38، ارتفعت الإشارات وإنتاج الإنترفيرون، معززةً رؤية الورم للجهاز المناعي.
كيف يدمر CD38 محور الإشارة الرئيسي
عند التعمق أكثر، وجد العلماء أن CD38 يرتبط فيزيائياً بـMAVS على الميتوكوندريا ويتداخل مع شراكة MAVS مع RIG-I، مما يضعف نقل الإشارة. والأبرز من ذلك أن مستويات CD38 الأعلى أدت إلى انخفاض في بروتين MAVS دون تغيير المخطط الجيني له، ما يشير إلى وجود تدمير نشط. أظهرت اختبارات باستخدام مثبطات مختلفة أن هذا الفقد يعتمد على آلية إعادة التدوير الخلوية المعروفة بالالتهام الذاتي (autophagy)، وبشكل خاص على شكل يستهدف الميتوكوندريا. زاد CD38 من مؤشرات "أكل الذات" الميتوكوندري، وخفّض عدة بروتينات ميتوكوندرية، وشجّع تغليف MAVS داخل هياكل الحويصلات الالتهابية التي تُحلّل لاحقاً. إن حجب البلعمة الميتوكوندرية حافظ على MAVS وأعاد إشارات الإنترفيرون، مما يدل على أن CD38 يعيق الإنذار بدفع MAVS نحو مجرى التخلص الخلوي.
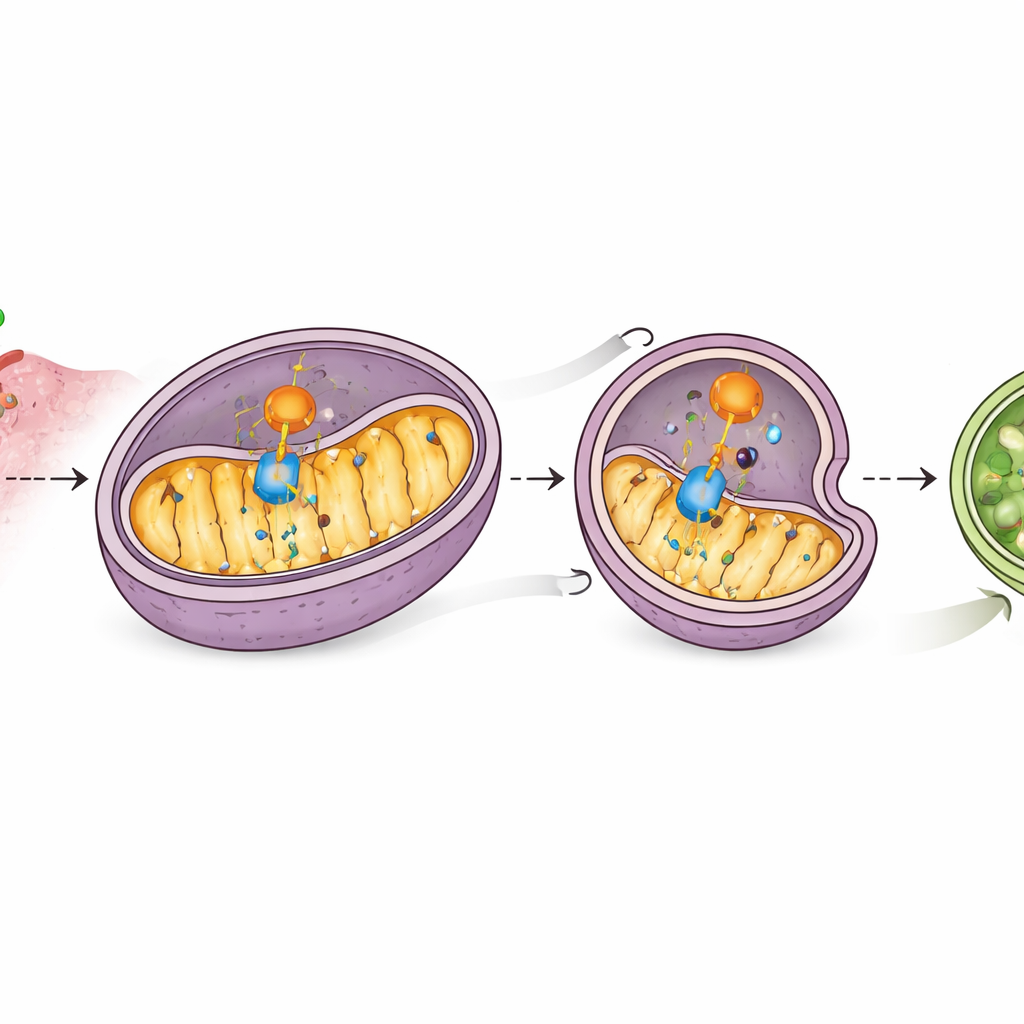
مساعد يوجّه الميتوكوندريا إلى التدمير الذاتي
حددت الدراسة لاعباً آخر، PHB2، وهو بروتين داخل الميتوكوندريا يعمل كمستقبل لإزالة الميتوكوندريا المستهدفة. أظهرت دراسات الطيف الكتلي وتجارب الالتحام أن CD38 يتفاعل مع PHB2 ويزيد وجود PHB2 في الميتوكوندريا، حيث يقوم PHB2 بدوره بتجنيد آلية الالتهام الذاتي الأساسية. يرتبط PHB2 أيضاً بـMAVS، ويقوّي CD38 هذا الاتصال. عندما خُفض مستوى PHB2، لم يعد بإمكان CD38 أن يحفز البلعمة الميتوكوندرية بفعالية، تعافت مستويات MAVS، وأُعيد تفعيل جينات مرتبطة بالإنترفيرون. يكشف ذلك سلسلة أحداث: يتفاعل CD38 مع PHB2، وPHB2 يتفاعل مع MAVS، ومعاً يوجّهون MAVS إلى ميتوكوندريا مهيأة للتحلل، كاتمين بذلك إنذار الإنترفيرون.
دلالات من نماذج حيوانية
لاختبار الأثر في كائنات حية، استخدم الباحثون أوراماً في الفئران مُهندَسة لعدم احتوائها على CD38. في الفئران ذات الجهاز المناعي السليم، نمت هذه الأورام ببطء أكبر، واحتوت على عدد أكبر من خلايا CD8، وكان لها نسبة أعلى من الخلايا المنتجة للإنترفيرون-غاما، وهو علامة على استجابات مناعية مضادة للأورام نشطة. أزال حجب مستقبل الإنترفيرونات من النوع الأول هذه الأفضلية، مؤكداً أن إشارة الإنترفيرون ضرورية للمناعة المحسّنة. في فئران مُؤنسة تحمل أورام البلعوم الأنفي البشرية، أدى تقليل CD38 أيضاً إلى إبطاء النمو وزيادة تسلل خلايا CD8، لكن هذه الفائدة اختفت عندما خفّضوا MAVS أيضاً في خلايا الورم. تدعم هذه النتائج الحية الفكرة أن محور CD38–PHB2–MAVS داخل خلايا الورم يشكّل قوة استجابة خلايا T في الجسم.
ماذا يعني هذا للعلاجات المستقبلية
بشكل عام، تُظهر النتائج أن CD38 في خلايا سرطان البلعوم الأنفي يعمل كمخرب داخلي للمناعة المضادة للأورام. من خلال دفع شكل انتقائي من إعادة تدوير الميتوكوندريا، يستنزف CD38 MAVS، ويضعف إنتاج الإنترفيرون من النوع الأول، ويقلل تقديم المستضدات، وفي النهاية يضعف هجوم خلايا CD8. المركبات الحالية الحابسة لـCD38 تستهدف في الغالب نشاطه الإنزيمي ولا تزيل البروتين أو تستعيد MAVS. يجادل المؤلفون بأن استراتيجيات جديدة تهدف إلى تقليل مستويات CD38 أو تعطيل شراكته مع PHB2 أو MAVS قد تعيد إنعاش إنذار الإنترفيرون داخل الأورام. وبالاقتران مع مثبطات نقاط التفتيش الحالية، قد تحول مثل هذه المقاربات مزيداً من سرطانات البلعوم الأنفي — وربما أنواعاً أخرى — من حالة باردة مناعياً إلى حالة قابلة للاستجابة مناعياً.
الاستشهاد: Liang, L., Li, W., Liu, S. et al. CD38 degrades MAVS through mitophagy to inhibit type I interferon secretion in nasopharyngeal carcinoma cells and impairs CD8+T cell-mediated anti-tumor immunity. Nat Commun 17, 2544 (2026). https://doi.org/10.1038/s41467-026-69339-7
الكلمات المفتاحية: سرطان البلعوم الأنفي, العلاج المناعي للأورام, الإنترفيرون من النوع الأول, خلايا T CD8, البلعمة الميتوكوندرية