Clear Sky Science · ar
متغيرات فقدان الوظيفة في منشّط CAPN1 CD99L2 تسببَ ضمورًا مُتلوّحًا مُترابطًا صِبغيًا-X
لماذا هذا مهم للعائلات التي تعاني مشاكل حركة غير مفسّرة
يعيش كثير من الناس لسنوات مع صعوبات في المشي، أو تيبّس العضلات، أو مشاكل في التوازن والكلام دون أن يعرفوا السبب الحقيقي. تُظهر هذه الدراسة كيف يمكن لفحوصات الحمض النووي الحديثة أن تمنح بعض هذه العائلات إجابات أخيرًا. لم يكتف الباحثون بمقارنة اختبارات جينية مختلفة لاضطرابات الحركة النادرة، بل كشفوا أيضًا عن سبب غير معلوم سابقًا لحالة تُسمى الضمور المتلوّح المترابط المرتبط بالكروموسوم X، ما يوجّه الانتباه إلى مسارات بيولوجية قد تكون مهمة أيضًا في أمراض دماغية أكثر شيوعًا.
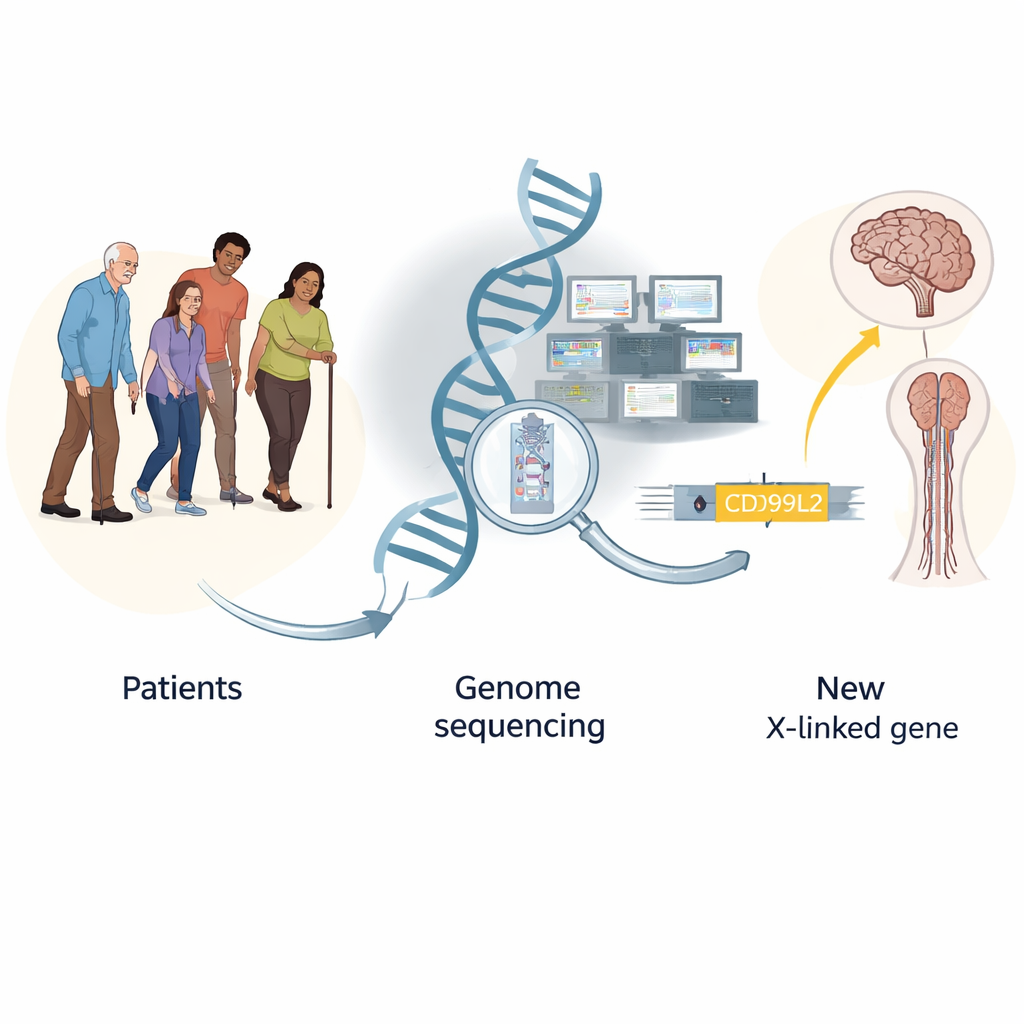
العثور على إبرٍ جينية في كوم من الأمراض النادرة
غالبًا ما يُشتبه في أن اضطرابات الحركة النادرة مثل الترنّح (حركات غير ثابتة) والشلل الرخو المتصلب (أرجل متيبّسة وضعيفة) لها أساس جيني، لكن لدى معظم المرضى تعود الاختبارات القياسية سلبية. تابع الفريق 2811 شخصًا في ألمانيا وفي أنحاء أوروبا أُحيلوا بسبب اشتباه باضطرابات حركة نادرة على مدى ست سنوات. أولًا، نظروا في اختبارات مستهدفة تقليدية تبحث عن توسعات متكررة معروفة في عدد قليل من الجينات؛ ومنحت هذه الإجابات في نحو 11% من الحالات. ثم استخدموا تسلسل الإكسوم، الذي يقرأ أجزاء الشيفرة البروتينية فقط من الجينوم، ووجدوا تفسيرات جينية مؤكدة في نحو 19% من المرضى، لا سيما لدى من لديهم تيبّس عضلي.
التطلع لما هو أبعد من الاختبارات القياسية بتسلسل الجينوم الكامل
لدفع التحري أبعد، استخدم العلماء تسلسل الجينوم الكامل، الذي يقرأ تقريبًا كل حمض نووي للشخص، بما في ذلك مناطق قد تغفلها الاختبارات القياسية والإكسوم. بين 486 فردًا خضعوا لهذا الاختبار الأشمل، ارتفعت نسبة التشخيص بحوالي 7.5 نقطة مئوية، إلى حد كبير لأن تسلسل الجينوم أفضل في رصد تغيّرات معقّدة مثل إعادة ترتيب البُنى والتوسعات المتكررة. كما أظهرت الدراسة أن تسجيل المعلومات السريرية بعناية — خاصة وصف الأعراض بدقة، وصغر سن الفحص، ووجود مزيج من التيبّس مع مشاكل حركة أخرى — ساعد في توقع من هم الأكثر احتمالًا للحصول على تشخيص جيني واضح.
كشف سبب جديد مرتبط بالكروموسوم X للضمور المتلوّح المتصلب
حتى بعد هذه الفحوص المكثفة، ظل كثير من المرضى دون تشخيص. جمع الباحثون بيانات جينية من أكثر من 13,000 فرد واستخدموا نهج «عبء الجين»، سائلين أي الجينات تحمل متغيرات مريبة بتواتر أكبر في المرضى مقارنة بالضوابط السليمة. أشارت هذه التحليلات ليس فقط إلى جينات مرض معروفة، بل وأيضًا إلى جين رسميًا مُهمل سابقًا على الكروموسوم X يُسمى CD99L2. من خلال تجميع النتائج من عدة عائلات عبر أوروبا، حددوا 25 ذكرًا متأثرًا من 20 عائلة يحملون متغيرات ضارة في هذا الجين. عادةً ما ظهرت لدى هؤلاء الرجال مشاكل في المشي، وتيبّس في الساقين، وحدوث كلام متلعثم، وأحيانًا صعوبات في التوازن في منتصف أو أواخر مرحلة البلوغ، بينما كانت الحامِلات الإناث في الغالب غير متأثرات — نمط يتوافق مع اضطراب مرتبط بـX. المتغيرات ألحقت في الغالب دمارًا بالبروتين الطبيعي أو أزالت أجزاء حاسمة منه، ما يشير بقوة إلى أن فقدان وظيفته يسبب المرض.
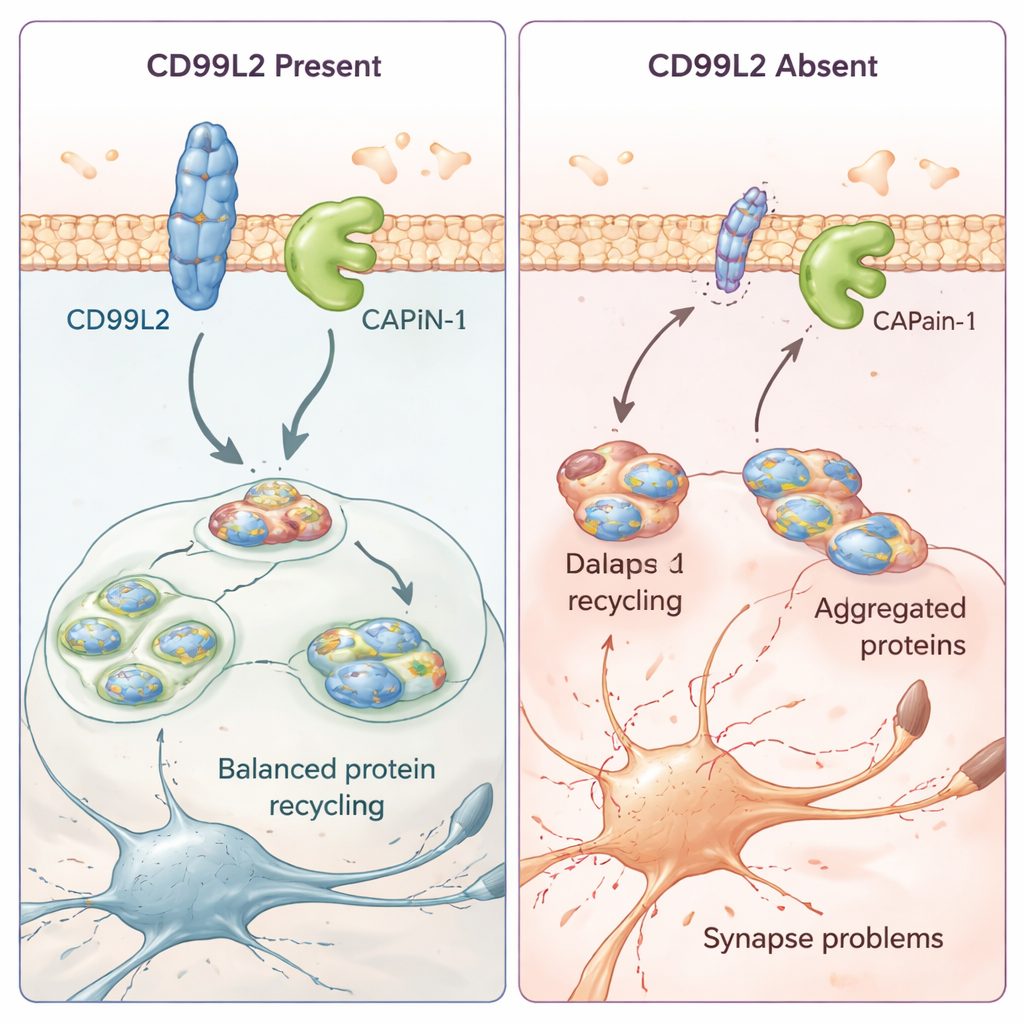
كيف يساعد بروتين غشائي صغير في حماية خلايا الدماغ
لفهم ما يفعله CD99L2 فعلًا داخل الخلايا، لجأ الفريق إلى نماذج خلوية وخلايا جلد مأخوذة من المرضى. وجدوا أن بروتين CD99L2 يستقر في غشاء الخلية وعادةً ما يُوسَم بعلامات صغيرة من «اليوبيكويتين» التي تتحكم في مدة بقائه قبل أن يُحلل. يرتبط CD99L2 ماديًا بكالباين-1 (CAPN1)، وهو إنزيم منشط بالكالسيوم يقص البروتينات الأخرى ويساعد في الحفاظ على صحة المشابك — نقاط التواصل بين الخلايا العصبية. عندما يكون CD99L2 موجودًا وسليمًا، فهو يساعد في تشغيل كالباين-1 وإيقافه بطريقة منظمة، ثم يُقَص ويعاد تدويره بنفسه. عندما يغيب CD99L2 أو يتغيّر هيكليًا، تُضعف فعالية تنشيط كالباين-1. في خلايا المرضى، يصاحب ذلك اضطراب في نشاط العديد من الجينات المرتبطة بالمشابك وتواصل الخلايا العصبية، ما يوحي بأن تغيّرات طفيفة لكن واسعة النطاق في دوائر الدماغ قد تكون أساس المشكلات الحركية التدريجية.
ما الذي يعنيه هذا للمرضى اليوم ومستقبلاً
للعا ئلات التي تعاني ضمورًا متلوّحًا مترابطًا غير مفسّر أو شللًا رخوًا متصِلًا متيبّسًا، يقدم هذا العمل نوعين من التقدّم. أولًا، يُظهر أن استخدام تسلسل الجينوم الكامل مبكرًا، مع الوصف السريري الدقيق، يمكن أن يزيد بشكل ملحوظ فرص الحصول على تشخيص جيني قاطع. ثانيًا، يضيف CD99L2 إلى قائمة الجينات التي تتحكم بنشاط كالباين، وهو مسار سبق ربطه بأنواع نادرة من الترنّح وبأمراض شائعة مثل الزهايمر وباركنسون. بعبارة بسيطة، تكشف الدراسة عن مفتاح تشغيل/إيقاف جديد يساعد في الحفاظ على توازن صيانة خلايا الدماغ؛ عندما ينكسر هذا المفتاح، تتدهور الخلايا العصبية ببطء، مما يؤدي إلى التيبّس وسوء التنسيق. قد يفتح فهم هذا المفتاح في نهاية المطاف الباب أمام علاجات تضبط نشاط كالباين وتحمِي خلايا الدماغ عبر طيف من الأمراض العصبية.
الاستشهاد: Menden, B., Incebacak Eltemur, R.D., Demidov, G. et al. Loss-of-function variants in the CAPN1 activator CD99L2 cause X-linked spastic ataxia. Nat Commun 17, 1698 (2026). https://doi.org/10.1038/s41467-026-69337-9
الكلمات المفتاحية: الضمور المتلوّح, اضطرابات الحركة النادرة, تسلسل الجينوم, CD99L2, كالباين-1