Clear Sky Science · ar
تقييم أداء استنتاج مسار إشارة EGF باستخدام الفوسفوبروتيوميات وتفاعلات كيناز-ركيزة
لماذا يهم هذا خارج المختبر
تستمع خلايانا باستمرار وتتفاعل مع الإشارات من محيطها. واحدة من أهم هذه الإشارات هي عامل نمو البشرة (EGF)، الذي يساعد في التحكم بكيفية نمو الخلايا وانقسامها وبقائها. عندما يختل هذا النظام الاتصالي، يمكن أن يدفع ذلك نحو السرطان وأمراض أخرى. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكن له تبعات كبيرة: إذا استخدمنا تقنيات القياس القوية ونماذج الحاسوب الحالية، إلى أي مدى يمكننا فعلاً فهم مسار إشارة EGF أفضل مما تظهره رسوم الكتب الدراسية؟
من خطوط مستقيمة إلى مخططات التوصيل في الحياة الحقيقية
غالباً ما تُرسم "مسارات الإشارة" التقليدية كسلاسل مرتبة تقريباً من البروتينات تنقل رسالة من سطح الخلية إلى النواة. تم بناء تلك الخرائط خلال عقود باستخدام تجارب مستهدفة وبطيئة كانت تنظر إلى عدد قليل من البروتينات في كل مرة. يجادل المؤلفون بأن ذلك تركنا بنظرة ضيقة على ضوء عمود الإنارة: نعرف الكثير عن البروتينات القليلة التي كان من السهل دراستها، وأقل بكثير عن شبكة الاتصالات الأوسع التي من المحتمل أن توجد في الخلايا الحقيقية.
الاستماع إلى آلاف المفاتيح الجزيئية في آن واحد
لتجاوز تلك النظرة المحدودة، استخدم الفريق الفوسفوبروتيوميات، وهي تقنية طيف الكتلة القادرة على تتبع عشرات الآلاف من العلامات الكيميائية الصغيرة المسماة مجموعات الفوسفات على البروتينات في تجربة واحدة. توضع هذه العلامات بواسطة إنزيمات تسمى الكينازات وتعمل كمفاتيح تشغيل/إيقاف سريعة للإشارة. جمع الباحثون أولاً أكثر خرائط "من يمكنه أن يفوسفوريل من" شمولية حتى الآن بدمج ثلاثة أنواع من المعلومات: نتائج مُنقحة من الأدبيات، وتنبؤات من نموذج ذكاء اصطناعي يقرأ تسلسلات البروتينات، وشاشات تجريبية واسعة لتفضيلات الكينازات. وسّع ذلك بشكل كبير تغطية علاقات الكيناز–الركيزة المعروفة أو المشتبه بها من نحو 5% من المواقع القابلة للقياس إلى ما يصل إلى 70–80%.
اختبار صمود إشارة EGF عبر العديد من التجارب
بعد ذلك، ركزوا على استجابة EGF، وهو مسار كلاسيكي ولاعب رئيسي في سرطانات الرئة والثدي والجلد والدماغ. جمع الفريق ثلاث مجموعات بيانات منشورة متقدمة مع ثلاث قياسات جديدة وعميقة حساسة زمنياً في خلايا مشتقة من الكلى، بالإضافة إلى دراستين ضابطة استخدمتا محفزات مختلفة. معاً، قاست هذه التجارب أكثر من 40,000 موقع فسفرة في كل مجموعة بيانات وتتبعت كيف ارتفعت أو انخفضت علاماتها خلال الدقائق التالية لتحفيز EGF. وبينما اختلفت الأنماط العامة إلى حد ما بين أنواع الخلايا والتقنيات، تكرر تنشيط مواقع فسفرة رئيسية في مسار EGF، مؤكداً أن الإشارة الجوهرية متينة حتى عبر تجارب متنوعة.
إعادة بناء المحادثة الخفية بين الكينازات
بعد استنتاج أي الكينازات أصبحت أكثر أو أقل نشاطاً، حاول المؤلفون بعد ذلك إعادة بناء "المحادثة" الأساسية بينها: أي الكينازات من المرجح أن تنشط أو تؤثر في غيرها. حولوا خرائط الكيناز–الركيزة إلى شبكات كيناز–كيناز وطبقوا ثلاث استراتيجيات حسابية، تتراوح من أساليب ترتيب بسيطة إلى نهج أكثر تعقيداً يفرض أن يبدو الناتج كشجرة موجهة متجذرة في مستقبل EGF. قارنوا المسارات المستنتجة الناتجة مع عدة أنواع من "الحقيقة الأرضية": خريطة EGF مُنقّحة بعناية من قاعدة بيانات، وتجارب واسعة النطاق حيث تم إفراط التعبير عن كينازات مفردة، وأزواج من مواقع الكيناز التي كان سلوكها مرتبطاً ارتباطاً قوياً عبر الزمن.
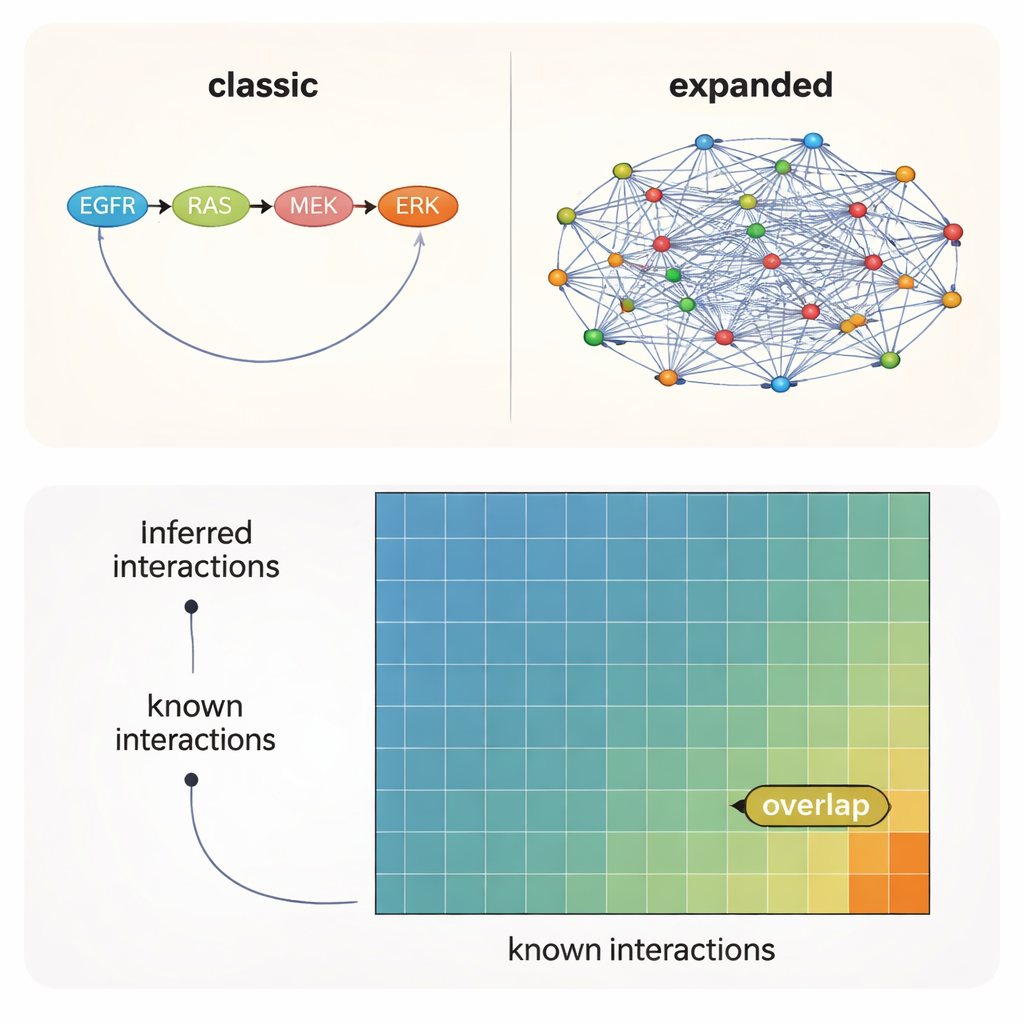
أغلب الروابط المعقولة لا تزال خارج الخريطة الرسمية
عبر جميع الاختبارات، كانت رسالة واضحة: اختيار المعرفة الأولية — أي الشبكة البادئة التي تغذيها إلى الخوارزمية — كان أكثر أهمية من الطريقة المستخدمة أو حتى من السياق التجريبي. استعادت الشبكات المبنية من الأدبيات أكبر عدد من التفاعلات المعروفة، بينما أشارت الموارد التنبؤية الأوسع إلى العديد من الاتصالات المعقولة الإضافية التي لم تُوثق رسمياً بعد. ومع أفضل الظروف، مع ذلك، وُجد أن نحو 10–12% فقط من التفاعلات المقترحة من قبل البيانات والنماذج كانت موجودة في أي من مجموعات المرجع. بمعنى آخر، نحو 90% من الروابط المدعومة بين الكينازات–الكينازات تقع في أراضٍ غير مستكشفة.
ماذا يعني هذا للعلاجات المستقبلية
بالنسبة لغير المتخصصين، الخلاصة أن مخطط مسار EGF المعروف في الكتب الدراسية على الأرجح هو مجرد قمة جبل الجليد. تكشف الفوسفوبروتيوميات الحديثة المدموجة مع طرق حسابية متقدمة عن شبكة إشارات أغنى وأكثر تشابكاً. قد تمثل العديد من هذه الروابط المقترحة حديثاً طرقاً مهملة يعيد فيها خلايا السرطان توجيه الإشارات للهروب من الأدوية، أو فرصاً جديدة لتصميم تركيبات علاجية أكثر ذكاءً. لا تثبت الدراسة أن كل رابط جديد حقيقي، لكنها توفر خارطة طريق وأدوات مفتوحة للباحثين لاختبار هذه الأفكار، بهدف الوصول في النهاية إلى علاجات أكثر دقة وفعالية للأمراض التي يلعب فيها مسار EGF دوراً مركزياً.
الاستشهاد: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
الكلمات المفتاحية: إشارة EGF, الفوسفوبروتيوميات, كينازات البروتين, شبكات الإشارات الخلوية, علم أحياء السرطان