Clear Sky Science · ar
المتفطرة السلية تعدل فوسفorylation الوحدة المضخية ATP6V1E1 للمضيف لتعزيز البقاء داخل الخلايا
لماذا هذا مهم في مكافحة السل
لا يزال مرض السل واحداً من أشد الأمراض المعدية فتكاً في العالم، إذ يودي بحياة أكثر من مليون شخص سنوياً. خلايا جهاز المناعة لدى البشر مزودة بـ "صناديق إعادة التدوير الحمضية" القوية التي عادة ما تهضم الميكروبات الغازية. تكشف هذه الورقة كيف تقوم بكتيريا السل، المتفطرة السلية (Mtb)، بتخريب نظام التحميض هذا داخل خلاينا، وتُظهر أن دواءً يستهدف هذه الحيلة يمكن أن يساعد الحيوانات المصابة على التخلص من العدوى بشكل أكثر فعالية.
الحمّام الحمضي داخل الخلية للجراثيم
عندما تُستنشق بكتيريا السل إلى الرئتين، تُبتلع سريعاً بواسطة خلايا مناعية تُسمى البلاعم. تنتهي البكتيريا داخل حويصلات غشائية من المفترض أن تلتحم بالليسوسومات — أكياس صغيرة مملوءة بإنزيمات هاضمة تعمل بشكل أفضل في بيئة شديدة الحموضة. تُنشأ هذه الحموضة بواسطة مضخة جزيئية، الڤاكْيولار ATPase (V-ATPase)، التي تستخدم وقود الخلية لدفع البروتونات إلى داخل الليسوسومات وخفض الرقم الهيدروجيني الداخلي. يعد التحميض السليم أمراً حاسماً لتحطيم Mtb، ومع ذلك أظهرت أبحاث عقود أن هذا الممرض بطريقة ما يحافظ على حويصلاته أقل حموضة ويستمر في البقاء.
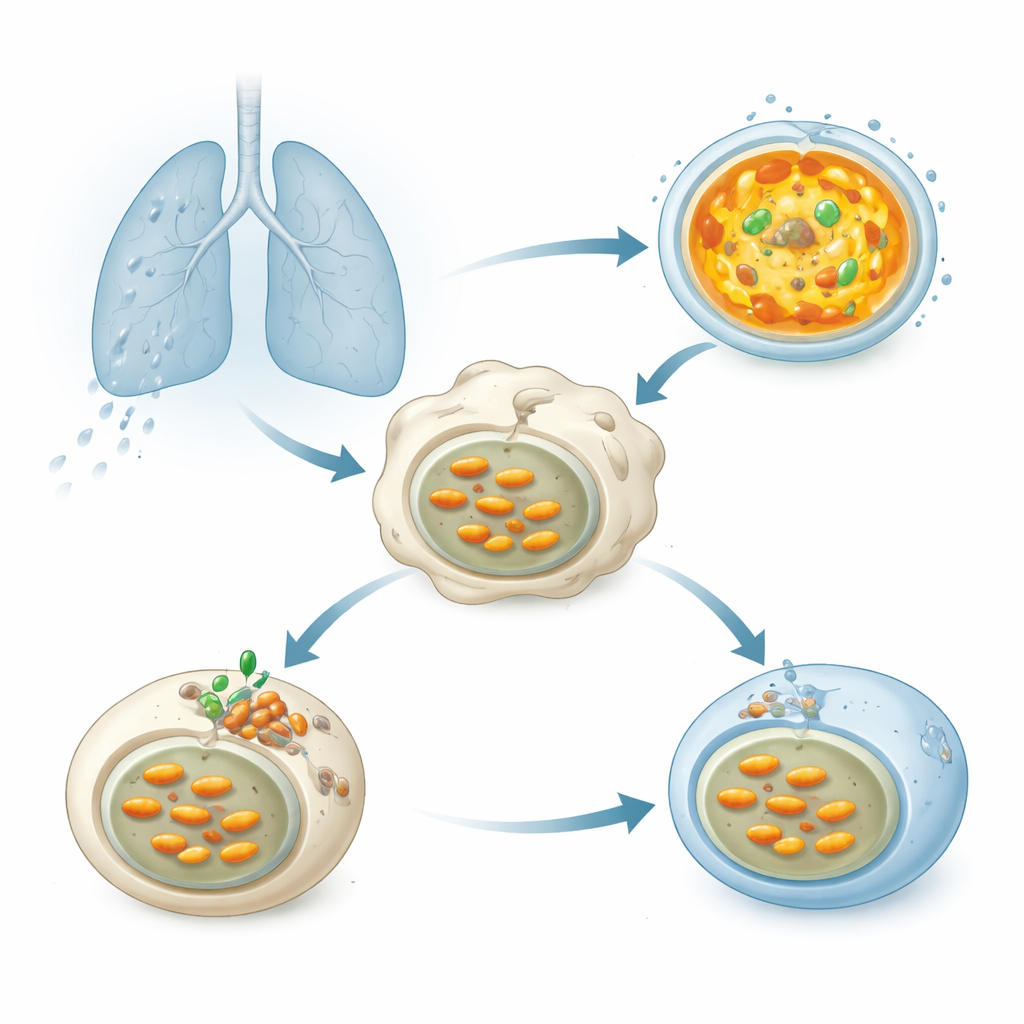
مساعدة بكتيرية سرية تُعيق التحميض
فحص الباحثون أكثر من 200 بروتين يمكن أن تُطلقها Mtb لمعرفة أيها يضعف تحميض الليسوسومات في الخلايا البشرية. برز واحد منها: إنزيم يُدعى Chp2 (المعروف أيضاً باسم Rv1184). عندما تنتج الخلايا Chp2، كانت ليسوسوماتها تُظهر تلوناً أضعف بصبغات حساسة للحموضة، ما يدل على رقم هيدروجيني أعلى وأقل عداءً. لم تعد سلالات Mtb المهندسة لانتزاع Chp2 قادرة على قمع التحميض؛ في البلاعم المصابة وفي الفئران، تم تطهير هذه البكتيريا الطافرة بكفاءة أكبر وأدت إلى تلف رئوي أخف. إعادة Chp2 إلى السلالة الطافرة أعادت كل من حاجز التحميض وازدياد الحمل البكتيري، محددةً Chp2 كعامل ضراوة يساعد Mtb على البقاء داخل خلايا المضيف.
وحدة المضخة في المضيف التي تعمل كمفتاح تحكم
لفهم كيف يتداخل Chp2 مع التحميض، بحث الفريق عن مكونات مضيفة قد يرتبط بها. وجدوا أن Chp2 يلتصق مباشرةً بجزء محدد من V-ATPase، وحدة تسمى ATP6V1E1 (مختصراً E1)، التي تساعد على استقرار بنية المضخة. زيادة كمية E1 في الخلايا عززت تحميض الليسوسومات وجعلت بقاء Mtb أصعب، بينما أدى تقليل E1 إلى العكس. الفئران التي حملت نسخة واحدة عاملة فقط من جين E1 كانت تملك ليسوسومات أقل حموضة، وحمولات بكتيرية أعلى في رئتيها، وتلف نسيجي أشد بعد العدوى، ما يبيّن أن E1 مدافع مضيف مهم ضد السل.
وسمة فسفورية على المضخة تخفض الحموضة
سأل المؤلفون بعد ذلك ما إذا كانت "وسوم" كيميائية على E1 قد تضبط نشاط المضخة. اكتشفوا أن إضافة مجموعات الفوسفات إلى اثنين من التيروسينات المحددة (Tyr56 وTyr57) على E1 تعمل كفرامل: محاكاة الفوسفorylation قلّلت التحميض ومنعت التجميع الكامل لـ V-ATPase، بينما منع الفوسفorylation كان له التأثير المعاكس. من خلال فحص مجموعة من الإنزيمات، حددوا كينازاً يُدعى BMX كالبروتين المضيف الذي يضع هذه الوسمة. عندما تم حجب BMX جينياً أو بمثبط جزيئي صغير، انخفض فسفرة E1، وجمعت المضخة بشكل أكثر كفاءة على أغشية الليسوسوم، وأصبحت الليسوسومات أكثر حمضية، وانخفض بقاء Mtb داخل البلاعم.
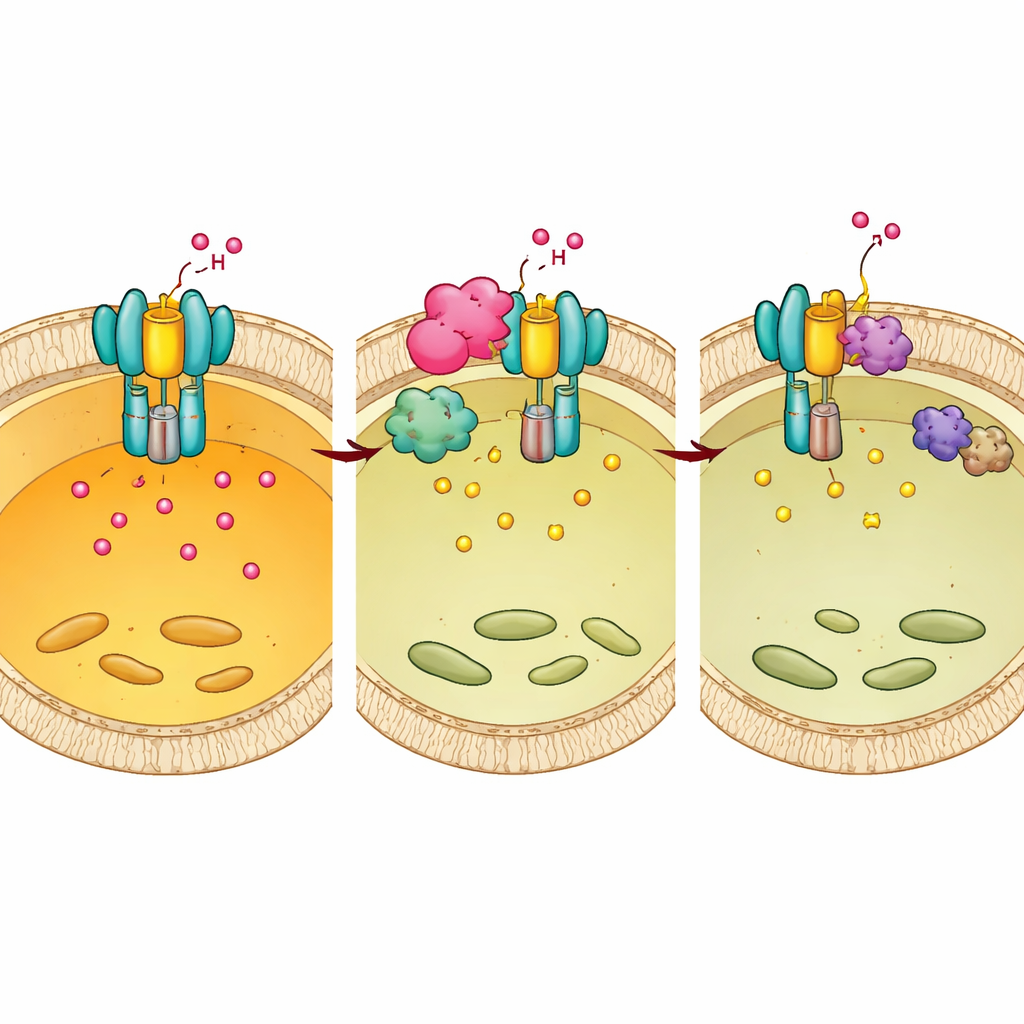
كيف تعيد Mtb برمجة مفتاح المضيف لصالحها
يتضح أن Chp2 وBMX يعمَلان معاً. أظهرت تجارب هيكلية وكيميائية حيوية أن Chp2 يعمل كحامل يقرّب E1 وBMX على سطح الليسوسوم، معزِّزاً فسفرة E1 في المواقع Tyr56/57. هذه الوسمة الإضافية تعطل التجميع الكامل للمضخة، ترفع الرقم الهيدروجيني للليسوسوم، وتخلق بيئة ألطف يمكن فيها لـ Mtb أن يستمر. عندما تم تثبيط BMX، اختفى أفضلية البقاء التي يوفرها Chp2، سواء في الخلايا المزروعة أو في الفئران المصابة. ومن الأهمية أن علاج الفئران بمثبط BMX بعد العدوى خفض الحمولات البكتيرية وتلف الرئة في الحيوانات العادية، ولكن ليس في الفئران ذات E1 الضعيف، ما يشير إلى أن الدواء يعمل عن طريق استعادة التحميض الفعال المدفوع بـ E1.
تحويل خدعة الممرض إلى فكرة علاجية
بعبارات مبسطة، تُظهر هذه الدراسة أن بكتيريا السل تدخل بروتين مساعداً إلى خلاينا يتدخل في "مضخة الحمض" في جهاز التخلص من النفايات، ويخفضها بما يكفي ليتمكن الميكروب من النجاة من التدمير. من خلال تحديد وحدة المضخة التي تعمل كقُبضة تحكم (E1) والإنزيم المضيف الذي يقلبها (BMX)، يكشف المؤلفون عن نقطة دقيقة يمكن للعلاج أن يتدخل عندها. إن تثبيط BMX في الفئران يعيد فعلياً تشغيل الحمّام الحمضي الداخلي للخلايا ويحسّن تطهير البكتيريا. تفتح هذه النتائج الباب أمام علاجات موجهة للمضيف تجعل خلايانا أكثر عدائية تجاه Mtb، ويمكن أن تعمل إلى جانب المضادات الحيوية وتساعد في مكافحة السل المقاوم للأدوية.
الاستشهاد: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
الكلمات المفتاحية: السل, الليسوسومات, علاج موجه للمضيف, المتفطرة السلية, V-ATPase