Clear Sky Science · ar
زيادة لاكتلة الهيستون تزيد تعبير CXCL1 لاختراق العدلات والهروب المناعي في سرطان البنكرياس
لماذا تهم هذه الدراسة السرطانية
يعد سرطان البنكرياس من أخطر أنواع السرطان، جزئياً لأنه غالباً ما يقاوم العلاجات المناعية الحديثة الفعالة في أورام أخرى. تكشف هذه الدراسة كيف تعيد أورام البنكرياس برمجة استقلاب السكر داخلها لتعطيل الجهاز المناعي بهدوء، وكيف أن حجب تلك العملية قد يعيد فتح طريق لرد فعل الدفاعات الجسمية — ولأدوية موجودة — لمحاربة الورم.
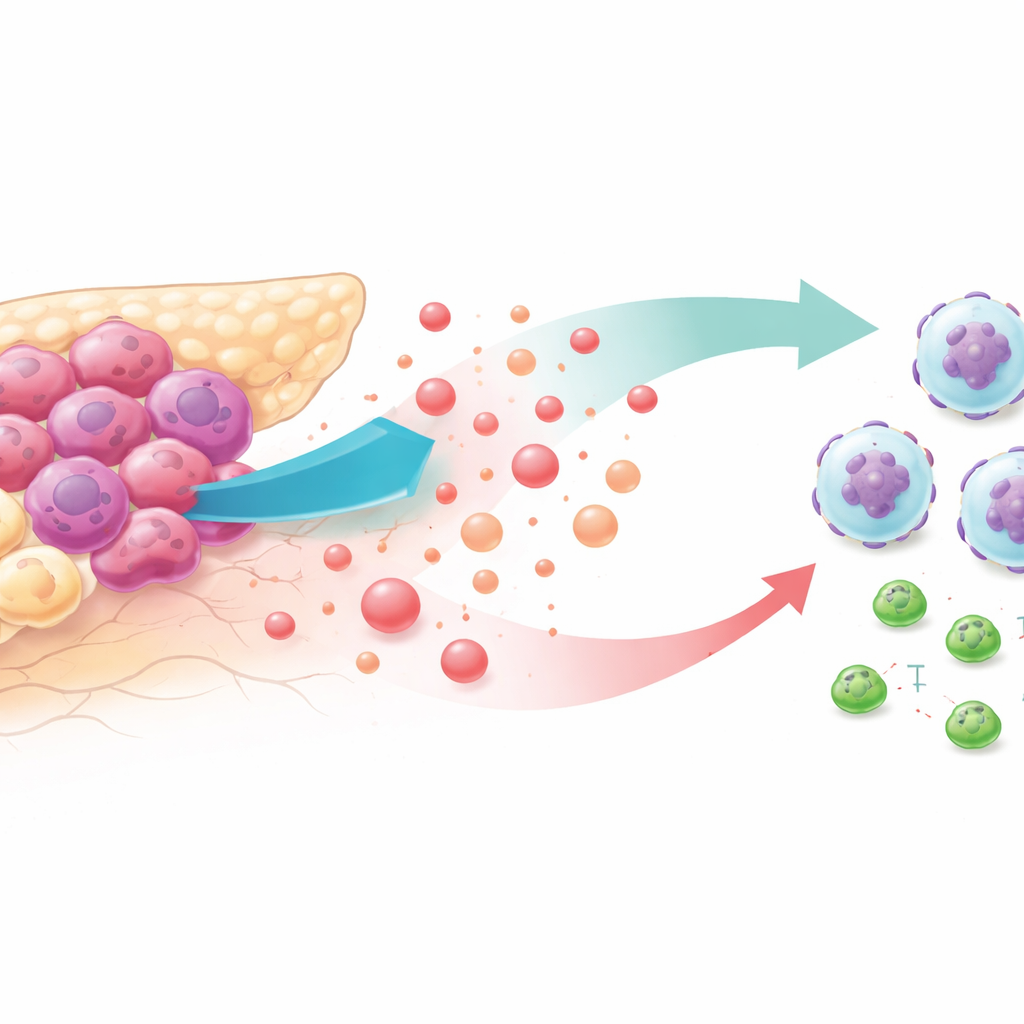
أورام نهمة للسكر وجوار عدائي
تشتهر الخلايا السرطانية بحرق الجلوكوز بوتيرة عالية، حتى عندما يتوفر الأكسجين. هذا النمط «عالي الاستقلاب السكري» يفيض الحي المحيط بالورم باللاكتات، وهو ناتج ثانوي كان يُعتبر نفاية استقلابية. من خلال تحليل قواعد بيانات أورام المرضى ونماذج الفئران، وجد الباحثون أن سرطانات البنكرياس ذات الاستقلاب السكري الأكثر شدة كانت مملوءة بالعدلات — خلايا دم بيضاء تساعد الورم على النمو في هذا السياق — وكان فيها عدد خلايا CD8 القاتلة للسرطان أقل. وارتبط وجود هذا النمط في أورام المرضى بحدوث فترة بقاء أقصر، مما يشير إلى ترابط وثيق بين الاستقلاب المعدّل والهروب المناعي.
كيف تستخدم الأورام اللاكتات لاستدعاء المساعدة الخاطئة
لفهم كيف يجذب الاستقلاب السكري العدلات، خفّض الفريق مستوى الاستقلاب السكري في خطوط خلايا سرطان البنكرياس والفئران باستخدام أدوية أو حيل جينية. عندما جرى حجب تكسير السكر، أطلقت خلايا الورم كمية أقل بكثير من إشارة كيميائية تسمى CXCL1، وانخفضت مستويات هذه الإشارة في الدوران لدى الفئران وفي عينات المرضى. في اختبارات الهجرة المخبرية، تحرّكت العدلات بحماسة نحو وسط من خلايا سرطانية عالية الاستقلاب السكري لكن لم تتحرك نحو وسط خلايا تمت فيها إعاقة الاستقلاب — ما لم يضف الباحثون CXCL1 المصفى. في الفئران الحية، أعاد إعادة CXCL1 إلى الأورام التي خفّضت استقلابها السكري أعداد العدلات إلى السابق وضعف التأثير المضاد للورم الناتج عن تثبيط الاستقلاب.
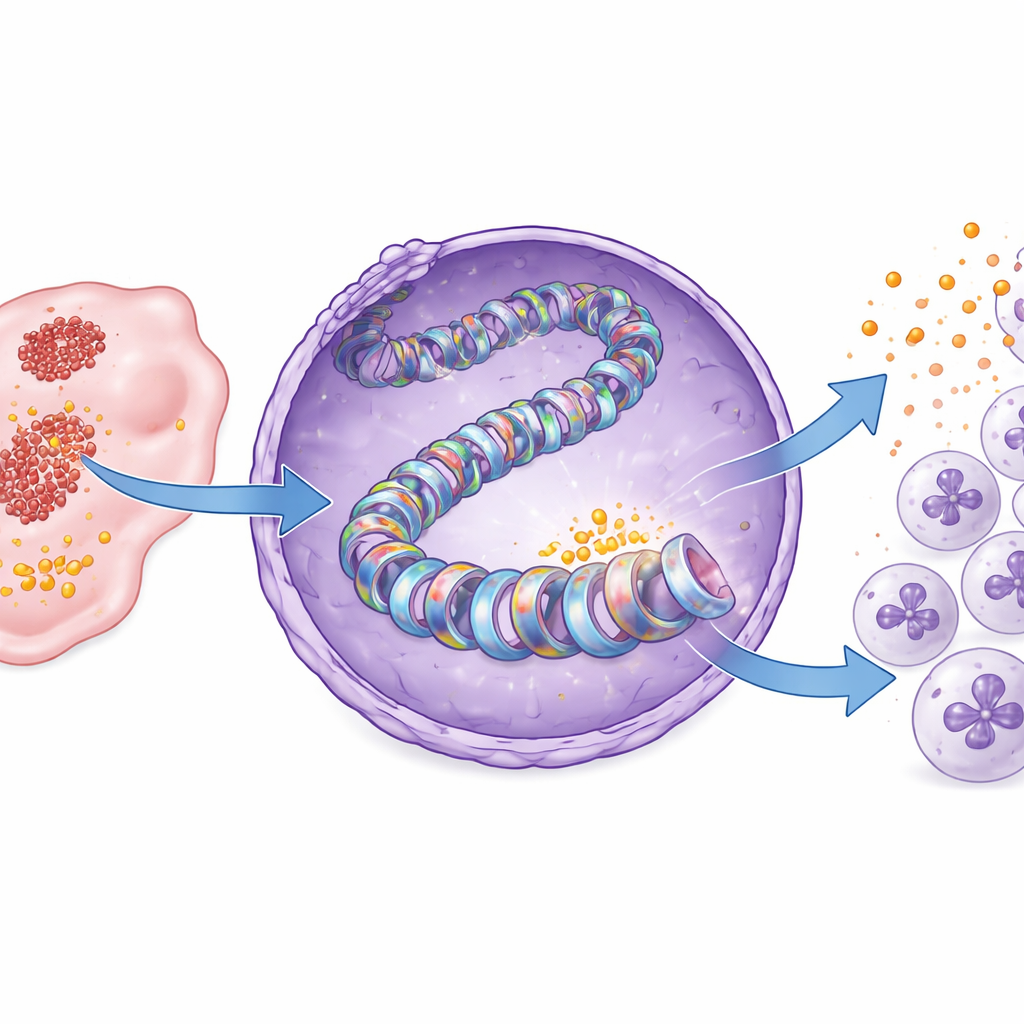
مفتاح إبجينيتي جديد تقوده اللاكتات
ثم زَجَت الدراسة إلى مستوى تغليف الحمض النووي. جيناتنا ملتفة حول بروتينات تشبه البكرات تسمى الهيستونات، وعلاماتها الكيميائية تعمل كمفاتيح تشغيل/إيقاف لنشاط الجينات. يُظهر المؤلفون أنه في سرطان البنكرياس، تضيف اللاكتات الناتجة عن التحلل السكري وسم «لاكتيل» محدداً إلى موضع واحد في الهيستون يعرف باسم H3K18. كان هذا التعديل، المسمى لاكتلة الهيستون H3K18، أعلى بكثير في أنسجة الورم منه في البنكرياس الطبيعي. عندما جرى حجب التحلل السكري، انخفضت اللاكتلة عند H3K18، خصوصاً بالقرب من منطقة التحكم في جين CXCL1، وانخفض إنتاج CXCL1. أعاد إضافة اللاكتات كلاً من علامة الهيستون وتعبير CXCL1. عبر عينات المرضى، أظهرت الأورام التي كانت فيها لاكتلة H3K18 أعلى أيضاً مستويات CXCL1 أعلى، رابطين هذه العلامة الجزيئية بمشهد مناعي مؤيد للورم.
تحديد الإنزيم ونقطة ضعف قابلة للعلاج
تُكتب علامات الهيستون بواسطة إنزيمات متخصصة. من خلال فحص مثبطات للبروتينات المعروفة بتعديل الهيستون، حدّد الباحثون إنزيماً اسمه PCAF ككاتب رئيسي لعلامة لاكتلة H3K18 في سرطان البنكرياس. أشارت نمذجة بنيوية إلى أن PCAF يمكنه الارتباط باللاكتيل-CoA، الشكل المنشط للاكتات المستخدم في الوسم، وأكدت تجارب بيوكيميائية أن PCAF المنقى يمكنه مباشرةً إضافة مجموعات لاكتيل إلى الهيستون H3. أدى حجب PCAF بمركب صغير، بروموسبورين، إلى خفض لاكتلة H3K18 وإنتاج CXCL1 في خلايا السرطان وفي أورام الفئران. ونتيجة لذلك، دخلت عدلات أقل إلى الأورام، تراكمت خلايا CD8 أكثر، وتباطأ نمو الورم، وكل ذلك من دون فقدان وزن واضح أو سمية ملحوظة في الفئران.
تحويل ورم بارد إلى حار بالعلاج المركب
بما أن أدوية نقاط التفتيش المناعية القياسية مثل الأجسام المضادة المضادة لـ PD-1 أظهرت نجاحاً محدوداً في سرطان البنكرياس، اختبر الفريق ما إذا كان تفكيك مسار اللاكتات–PCAF–CXCL1 يمكن أن يجعل هذه الأورام أكثر استجابة. في نماذج فئران تحت الجلد ونماذج أورام بنكرياس موضعية، قلّل الجمع بين بروموسبورين وعلاج مضاد–PD-1 حجم الأورام أكثر من أي علاج وحده، وقلل تسلل العدلات، وعزز خلايا CD8 النشطة، ومدد البقاء بشكل ملحوظ. يشير هذا إلى أن قطع «صفارة إنذار» الورم الاستقلابية للعدلات يساعد على تحويل الورم من حالة مناعية «باردة» إلى حالة «أكثر حرارة» يمكن لعلاج نقاط التفتيش المناعية التعامل معها بشكل أفضل.
ما معنى هذا للعلاج المستقبلي
بعبارات بسيطة، تكشف الدراسة عن سلسلة تفاعلات: تحرق أورام البنكرياس السكر، تطلق اللاكتات، تستخدم تلك اللاكتات لقلب مفتاح إبجينيتي على بروتينات تغليف الحمض النووي، ترفع CXCL1، وبالتالي تستدعي العدلات التي تساعدها على الاختفاء من خلايا T القاتلة. إن مقاطعة هذه السلسلة عند خطوة PCAF بواسطة دواء لا يبطئ الأورام فحسب، بل يجعل أيضاً العلاج المناعي الحالي أكثر فعالية في الفئران. بينما يلزم المزيد من العمل لضمان السلامة وإيجاد أفضل طريقة لاستهداف هذا المسار لدى البشر، تسلط هذه النتائج الضوء على استراتيجية واعدة: إعادة برمجة استقلاب الورم ومفاتيح الجينات لمنح الجهاز المناعي فرصة عادلة للمواجهة.
الاستشهاد: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
الكلمات المفتاحية: سرطان البنكرياس, استقلاب الورم, لاكتلة الهيستون, البيئة الميكروية للورم, العلاج المناعي للسرطان