Clear Sky Science · ar
استهداف NHEJ يُفعّل إشارة STING عبر تحطيم MYC لتعزيز المناعة المضادة للأورام في سرطان الرئة صغير الخلايا
لماذا تهم هذه الدراسة
يعد سرطان الرئة صغير الخلايا من أخطر أنواع السرطان، حيث يعيش معظم المرضى أقل من سنة بعد التشخيص. والمثير للدهشة أن هذه الأورام تحمل العديد من الطفرات في الحمض النووي التي من المفترض أن تجعلها أهدافًا سهلة للجهاز المناعي، ومع ذلك تستجيب عمليًا بشكل ضعيف لأدوية المناعة الحديثة. تكشف هذه الدراسة عن فرامل جزيئية خفية تمنع الجهاز المناعي من التعرف على هذه الأورام وتوضح كيف أن تعطيل بروتين مفتاحي في إصلاح الحمض النووي يمكن أن يحول هذه السرطانات من «باردة» مناعيًا إلى «ساخنة»، مما يسمح للعلاجات الحالية بأن تعمل بشكل أفضل بكثير.
مفتاح إصلاح خفي في أورام الرئة
بدأ الباحثون بتنقيب بيانات جينية من أكثر من 179,000 ورم بشري عبر 24 نوعًا من السرطان. ركزوا على مسار إصلاح الحمض النووي المسمى الالتحام غير المتجانس للنهايات (nonhomologous end joining)، الذي يصلح الانقطاعات الخطرة في سلاسل الحمض النووي. تبين أن المتحكم المركزي في هذا المسار، بروتين يُدعى DNAPKcs (مشفر بواسطة جين PRKDC)، مرتفع بشكل غير عادي في سرطان الرئة صغير الخلايا. ضمن آلاف عينات أورام الرئة، أظهرت حالات صغيرة الخلايا أعلى نشاط لهذا المفتاح الإصلاحي. عاش المرضى الذين كانت أورامهم ذات مستويات PRKDC الأعلى لفترة زمنية أقصر وكانوا أقل احتمالًا للاستفادة من العلاج الكيميائي القياسي وأدوية نقاط التفتيش المناعية، ما يشير إلى أن DNAPKcs يساعد الأورام على النجاة من كل من ضرر الحمض النووي والهجوم المناعي.
من تلف الحمض النووي إلى إنذار داخلي
لمعرفة ما يحدث عند إيقاف هذا المفتاح الإصلاحي، استخدم الفريق أدوية وأدوات إسكات جيني لحجب DNAPKcs في مجموعات من خلايا سرطان الرئة صغير الخلايا ونماذج أورام في الفئران. في العديد من هذه النماذج، وخاصة تلك المشابهة للأنواع الفرعية البشرية ذات النشاط العالي لجين الأورام MYC، قلّصت مثبطات DNAPKcs نمو خلايا الورم بشدة وحتى قلّصت أورامًا مشتقة من مرضى في الفئران. على المستوى الخلوي، أدى حجب DNAPKcs إلى تراكم الحمض النووي المكسور، مظهرًا على شكل بقع لمؤشر الضرر داخل النواة وحُبيبات صغيرة مملوءة بالحمض النووي تُدعى الأنوية الصغرى (micronuclei). تسربت هذه شظايا الحمض النووي إلى سيتوبلازم الخلية، حيث يمكن استشعارها كإشارات خطر.
تشغيل نظام الإنذار «الفيروسي» في الخلية
الحمض النووي الحر في مكان خاطئ عادة ما يكون علامة على عدوى فيروسية. تكتشف الخلايا ذلك باستخدام مستشعر يُدعى cGAS، الذي يُفعّل مسار إنذار لاحق يُسمى STING. أظهر المؤلفون أنه بعد تثبيط DNAPKcs، تجمّع cGAS على الأنوية الصغرى، وتنشىء STING، وتفعلت سلسلة من الجزيئات المحفزة للمناعة. أنتجت الخلايا مزيدًا من الإنترفيرونات من النوع الأول والنوع الثاني والكينوكينات التي تجذب الخلايا المناعية. كما زاد عرض بروتينات «الراية» الرئيسية على السطح (جزيئات MHC من الصنف الأول) التي تساعد الخلايا المناعية على التعرف على مولدات المستضدات الورمية. عندما تم حجب مسار STING كيميائيًا أو إسكاتُه جينيًا، اختفت هذه التغيرات إلى حد كبير وضعفت التأثيرات المضادة للأورام لمثبطات DNAPKcs، ما يؤكد أن هذا النظام الداخلي للإنذار ضروري للاستجابة.
تعطيل MYC لكشف الورم
تربط الدراسة أيضًا DNAPKcs بمحرك النمو القوي MYC، وهو بروتين يعتبر منذ زمن بعيد «غير قابل للعلاج الدوائي». في الأورام ذات النشاط العالي لـ MYC، أدى تثبيط DNAPKcs إلى تقليل إشارة AKT النشطة وإطلاق فرامل جزيئية على إنزيم آخر، GSK3β. بمجرد تنشيط GSK3β، علّم MYC ليُدمر، مما تسبب في انخفاض مستويات بروتين MYC. خفض MYC مباشرةً باستخدام أدوات جينية قلد العديد من التأثيرات المنشطة للمناعة الناتجة عن حجب DNAPKcs: ارتفعت إشارة STING، وتفعّلت جينات الإنترفيرون، وزاد MHC من الصنف الأول. وبالعكس، أدت إجبار الخلايا على إنتاج كميات زائدة من MYC إلى محو الأثر المعزز للمناعة لمثبط DNAPKcs إلى حد كبير. هذا يقترح أن DNAPKcs يساعد عادةً في تثبيت MYC، وأن دفع MYC نحو التحلل هو خطوة رئيسية في إيقاظ المناعة المضادة للأورام.
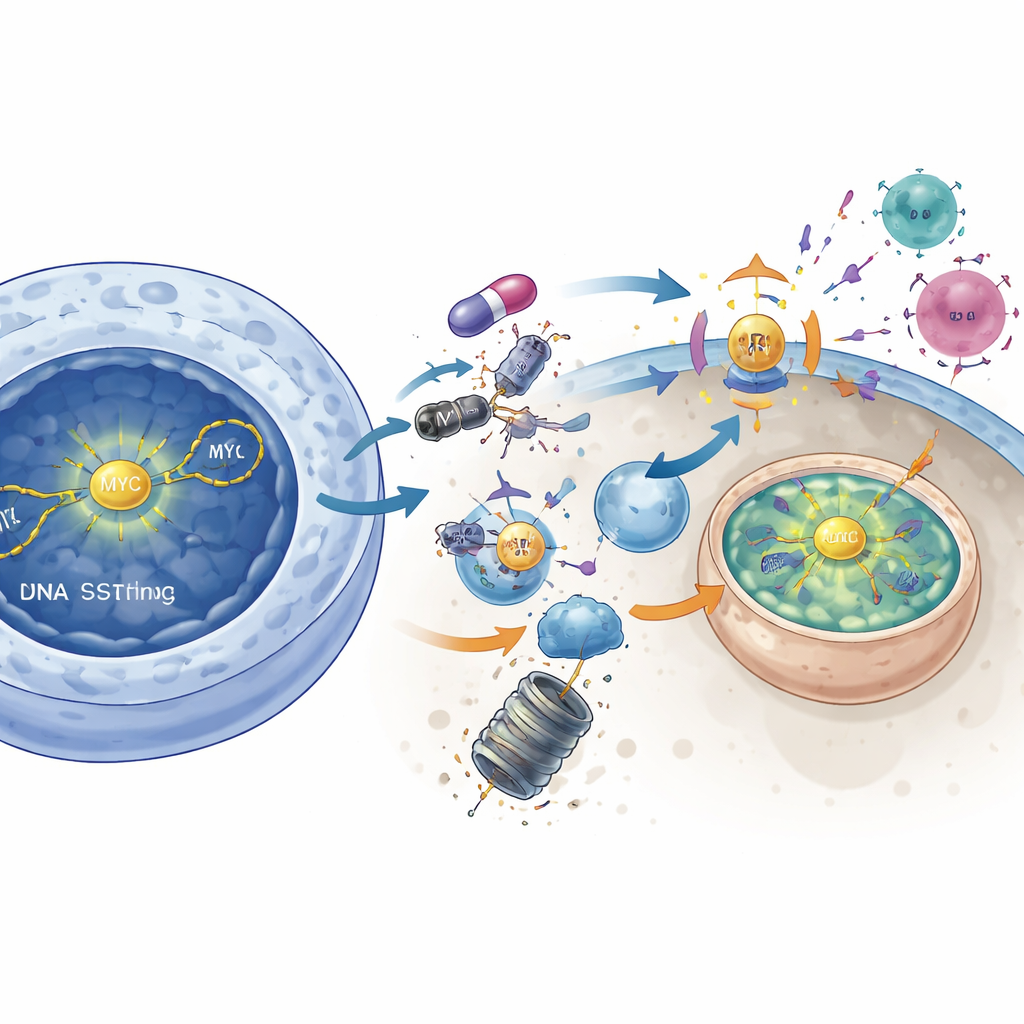
من أورام «باردة» إلى «ساخنة» في نماذج حية
في نماذج فئران ذات مناعة سليمة تحاكي عن كثب سرطان الرئة صغير الخلايا لدى البشر، أدى علاج بمثبط DNAPKcs بمفرده إلى إبطاء أو تقليص الأورام بشكل ملحوظ. والأهم من ذلك، أن الجمع بين هذا المثبط ودواء نقاط تفتيش مضاد لـ PD-L1 حول الأورام التي كانت مقاومة سابقًا، ما أدى إلى تراجع دراماتيكي للأورام وفي بعض الحالات إلى زوال كامل. أظهر التحليل المناعي المفصّل أن حجب DNAPKcs زاد من خلايا CD8 القاتلة للسرطان، وعزّز الحطاطات M1 المحفزة للالتهاب، وقَلّل الخلايا كابحة المناعة، وزاد مستويات MHC من الصنف الأول في الأورام. عكس إزالة خلايا CD8 أو تعطيل STING هذه الفوائد، مما يؤكد أن العلاج يعمل عن طريق تحويل الورم إلى منارة تجذب الهجوم المناعي بدلاً من قتل الخلايا السرطانية مباشرة بمفرده.
ماذا يعني هذا للمرضى
تكشف النتائج مجتمعة أن DNAPKcs هو منسق مركزي لكل من إصلاح الحمض النووي والتهرب المناعي في سرطان الرئة صغير الخلايا. من خلال حجب DNAPKcs تتراكم أضرار الحمض النووي، ويُزعزع استقرار MYC، وينطلق إنذار cGAS–STING، وتُفعّل مسارات الإنترفيرون والعرض المستضدي. يحول هذا التسلسل من الأحداث الأورام الصامتة مناعيًا إلى أورام تستجيب بقوة لحصار نقاط التفتيش والعلاج الكيميائي في نماذج قبل سريرية. وبينما لا تزال التجارب السريرية مطلوبة، تشير الدراسة إلى أن مثبطات DNAPKcs الحالية قد تُستخدم بالاشتراك مع العلاج المناعي لمنح المرضى المصابين بهذا السرطان العدواني فرصة أفضل للسيطرة الطويلة الأمد.
الاستشهاد: Chakraborty, S., Elliott, A., Sen, U. et al. Targeting NHEJ activates STING signaling through MYC degradation to boost antitumor immunity in SCLC. Nat Commun 17, 2597 (2026). https://doi.org/10.1038/s41467-026-69262-x
الكلمات المفتاحية: سرطان الرئة صغير الخلايا, كبح إصلاح الحمض النووي, مسار STING, تحطيم MYC, مناعة الأورام