Clear Sky Science · ar
نماذج التعلم العميق القابلة للتفسير والتوليد توضح فصل الطور بواسطة وحدات بروتينية غير منظّمة ذاتية
لماذا تهم مقاطع البروتين الصغيرة
داخل كل خلية من خلايانا، تتجمع جزيئات حيوية أساسية أحياناً على شكل بقع شبيهة بالقطرات تُسمى المكثفات البيومولكولية. تساعد هذه القطرات على تنظيم التفاعلات الكيميائية من دون جدران غشائية، مما يؤثر في كيفية تشغيل الجينات، وكيفية انتقال الإشارات، وكيف تستجيب الخلايا للإجهاد. تتكوّن العديد من هذه القطرات من مناطق مرنة في البروتينات تُعرف بالمجالات غير المنظمة ذاتياً. ومع ذلك، لا يزال علماء الأحياء يواجهون صعوبة في تحديد المقاطع القصيرة من التسلسل التي تجعل هذه القطرات تتكوّن فعلاً. تقدم هذه الدراسة إطار عمل للتعلم العميق، PhaSeMotif، يستطيع العثور على هذه المقاطع الأساسية وتصميم مقاطع جديدة، مما يمنح الباحثين أداة قوية لاستكشاف وإعادة توجيه المكثفات الخلوية.
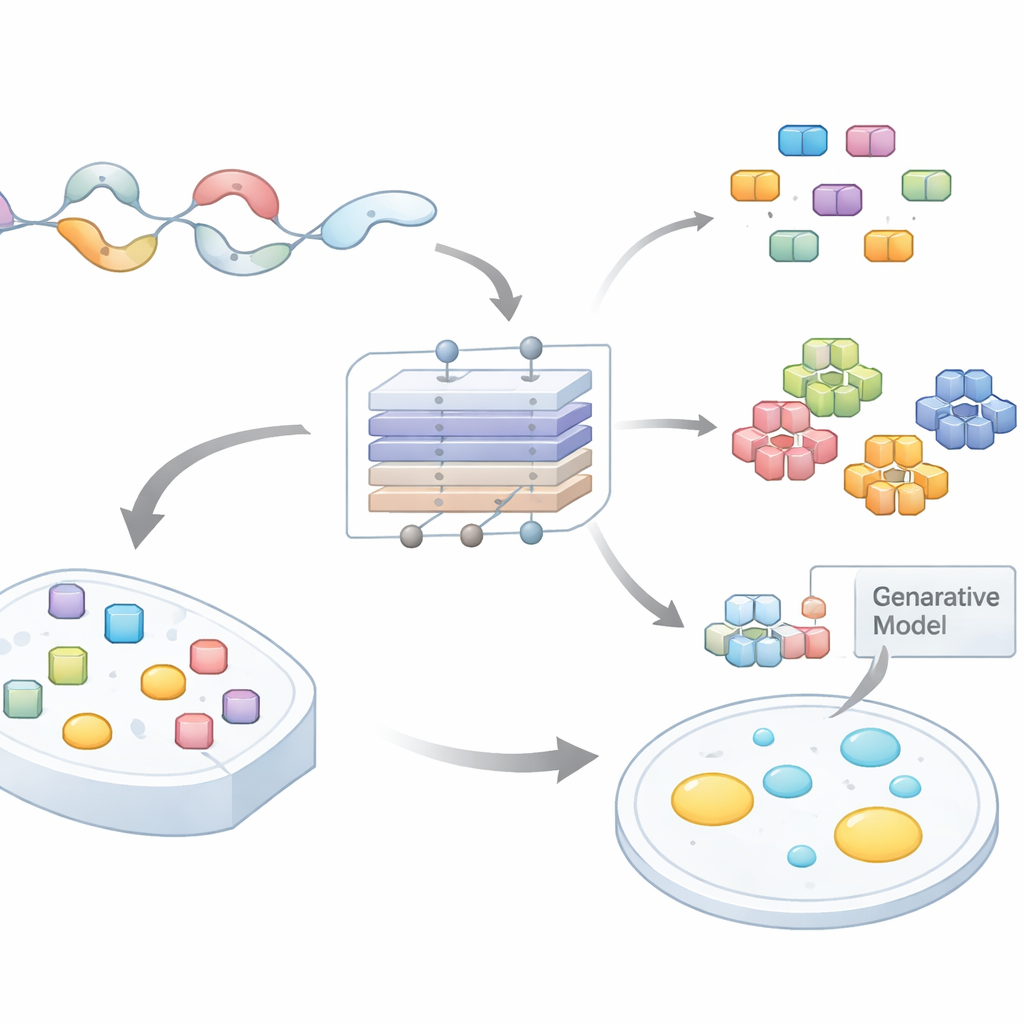
من ذيول بروتينية فوضوية إلى أفكار قابلة للاختبار
تحتوي العديد من البروتينات على ذيول طويلة ومرنة لا تنطوي على طي ثابت. تكون هذه المناطق غير المنظمة غنية بأحماض أمينية معينة وغالباً ما تحتوي على أنماط مكررة أو وحدات قصيرة. تُظهر أعمال متزايدة أن مثل هذه الوحدات تدفع التكثف عبر تمكين العديد من التفاعلات الضعيفة في آن واحد. ومع ذلك، كان مسح البروتيوم بأكمله لتحديد المقاطع القصيرة الهامة ولماذا يشكل عنق زجاجة كبير. الأدوات الحاسوبية الحالية عادةً ما تقدّر البروتين بأكمله أو مناطق كبيرة، مع تقديم إرشاد قليل حول مكان التغيير أو ما ينبغي اختباره في المختبر. سعى المؤلفون لبناء نموذج يتنبأ ليس فقط بما إذا كانت المنطقة غير المنظمة قادرة على تكوين قطرات، بل وأيضاً أي التسلسلات الفرعية بالضبط تقوم بالعمل الشاق.
خريطة تعلم عميق للوحدات المسببة للقطرات
جمعت الفريق مجموعات بيانات كبيرة من المناطق غير المنظمة عبر عدة أنواع وصنّفوها وفقاً لما إذا كانت البروتينات الحاضنة من المحتمل أن تخضع لفصل الطور. بعد ذلك درّبوا شبكة عصبية مبنية على الانتباه، PhaSeMotif، تقبل تسلسلاً من الأحماض الأمينية بأي طول وتنتج درجة لتشكيل القطرات. والأهم أن الشبكة تستخدم مزيجاً من طبقات الالتفاف وآليات الانتباه لتقييم مدى مساهمة كل نافذة قصيرة من التسلسل في تلك الدرجة. من خلال التتبع العكسي عبر النموذج (باستخدام تقنيات شبيهة بالانتشار العكسي الموجّه)، استخرج المؤلفون بقعاً عالية الأهمية — وحدات قصيرة غالباً أقل من 20 حمض أميني — اعتبرها النموذج أساسية لتكوين القطرات.
وضع التنبؤات على المحك في خلايا حية
لاختبار ما إذا كانت هذه الوحدات مهمة فعلاً، لجأ الباحثون إلى نظام مفعل بالضوء في خلايا بشرية. ربطوا المناطق غير المنظمة المتوقعة لتشكيل القطرات بوحدة تآزر حساسة للضوء ووسم فلوري. تحت ضوء أزرق، تكثفت هذه التركيبات بسرعة إلى نقاط ساطعة، مما أظهر فصل الطور في الوقت الحقيقي. ثم استأصل الفريق الوحدات الفردية جراحياً عن طريق استبدالها بروابط مرنة محايدة بنفس الطول. في 82% من بين 17 تسلسلاً معدلًا مُختبَراً، ضعُف تكوّن القطرات بشكل كبير أو اختفى تماماً، في حين أن الطفرات الضابطة خارج مقاطع PhaSeMotif غالباً ما لم تُحدث تأثيراً كبيراً. من المهم أن العديد من هذه الوحدات الأساسية تداخلت مع مواقع معروفة لوجود طفرات مرتبطة بالأمراض تعطل التكثف، مما يؤكد صلتها البيولوجية.
الكشف عن مفردات لأنواع الوحدات
مع أكثر من 17,000 وحدة بين أيديهم، سأل المؤلفون بعد ذلك ما إذا كانت هناك "نكهات" شائعة للمقاطع المسببة للقطرات. حلّلوا تركيب الأحماض الأمينية ونمطها، ثم جمعوا الوحدات في تسعة مجموعات. كانت بعض المجموعات غنية ببقايا عطرية والجليسين، بما يتوافق مع تفاعلات π–π والتفاعل الكاتيوني–π اللاصقة. احتوت مجموعات أخرى على رقع متفرقة من الشحنات الموجبة والسالبة، ما يفضّل الجذب الكهربائي والتجزئة الانتقائية إلى مكثفات معينة. سيطرت مجموعات إضافية على البرولين والجليسين، اللذين يدعمان المرونة، أو على سلاسل طويلة من الجلوتامين التي يمكن أن تشكل شبكات كثيفة من روابط الهيدروجين. أظهرت المقصورات الخلوية وأنواع المكثفات المختلفة خلطات مميزة من هذه الفئات، مشيرة إلى أن تركيب الوحدات يساعد في تحديد أين ومع أي شركاء سيكثف البروتين.
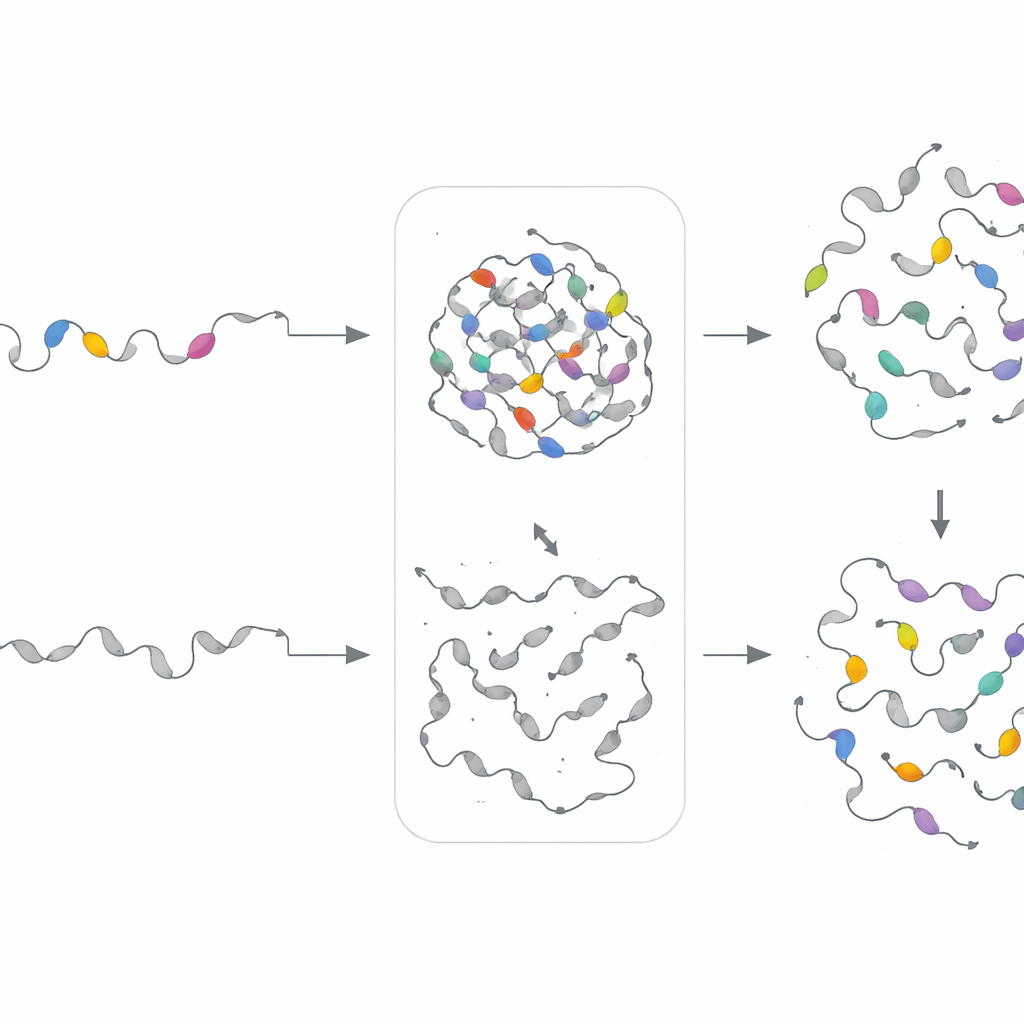
تصميم وحدات جديدة لإثبات القواعد
لاختبار ما إذا كانت "وصفات" الوحدات — بدلاً من التسلسلات الدقيقة — تحكم سلوك القطرات، بنى الفريق نماذج توليدية منفصلة لكل مجموعة وحدات. تعلمت هذه المشفرات التلقائية الاختلافية الأنماط الإحصائية لمجموعة معينة ثم أنتجت تسلسلات جديدة صناعية تشترك في نفس البصمات التركيبية لكن بترتيب مختلف. استبدل الباحثون هذه الوحدات الاصطناعية تجريبياً في بروتينات حُذفت منها المقاطع الأصلية. ولافت للانتباه، في 18 من أصل 21 حالة، أعادت الوحدات المصممة تكوين فصل الطور في الخلايا، وأحياناً ضبطت سرعة أو كثافة تكوّن القطرات. هذا يُظهر أن PhaSeMotif يلتقط قواعد تصميم أساسية يمكن إعادة استخدامها لبناء أو إصلاح مناطق مكونة للقطرات.
ما يعنيه هذا للبيولوجيا والمرض
بربط التعلم العميق القابل للتفسير مع التصميم التوليدي والاختبارات الخلوية المباشرة، يحول هذا العمل الفكرة الغامضة عن "المناطق غير المنظمة المسببة للقطرات" إلى مجموعة ملموسة من وحدات قصيرة قابلة للتجميع. للخارجين عن التخصص، الاستنتاج هو أن العلماء بات بإمكانهم الآن قراءة وكتابة المقاطع البروتينية الصغيرة التي تتحكم في كيفية تجمّع وامتزاج وعطل المكثفات الخلوية. يفتح هذا الباب أمام اكتشاف أسرع للطفرات المسببة للأمراض في هذه المقاطع، ودراسات آلية أوضح عن كيفية تنظيم المكثفات للفسيولوجيا الخلوية، وما قد يؤدي في نهاية المطاف إلى هندسة عقلانية للبروتينات التي توجه القطرات لتطبيقات علاجية أو في علم الأحياء التركيبية.
الاستشهاد: Yang, H., You, K., Ma, L. et al. Interpretable and generative deep learning models explicate phase separating intrinsically disordered motifs. Nat Commun 17, 2571 (2026). https://doi.org/10.1038/s41467-026-69252-z
الكلمات المفتاحية: المكثفات البيومولكولية, البروتينات غير المنظمة ذاتياً, فصل الطور, التعلم العميق, وحدات البروتين