Clear Sky Science · ar
خلايا الكبد المعاد برمجتها وظيفياً بواسطة خلايا سرطان القولون والمستقيم ذات مستوى عالي من KIAA1199 تفضّل تراكم العدلات Egr1+ المحفزة للانبثاث
عندما يستهدف سرطان القولون الكبد
يعتقد معظم الناس أن انتشار السرطان يكون ببساطة عبر خلايا منبوذة تنفصل وتنتقل إلى أعضاء جديدة. تُظهر هذه الدراسة صورة أكثر إثارة للقلق: يمكن لأورام القولون والمستقيم أن تعيد برمجة الكبد بهدوء قبل وصول أي خلايا سرطانية، وتبني «تربة» مرحّبة يمكن أن تتجذر فيها الأورام المستقبلية بسهولة. فهم هذه المرحلة التحضيرية الخفية قد يفتح الباب لعلاجات تمنع حدوث الانبثاث الكبدي — السبب الرئيسي للوفاة في سرطان القولون والمستقيم — قبل أن يبدأ.
إعداد متخفٍ قبل وصول الأورام
غالباً ما ينتشر سرطان القولون والمستقيم إلى الكبد، لكن بعض الأورام فقط تفعل ذلك بشكل عدواني. ركز الباحثون على جزيء يسمى KIAA1199، الذي يكون وفيراً في السرطانات الشديدة الخطورة. في نماذج الفئران وعيّنات المرضى، لم تقتصر خلايا الأورام ذات مستوى KIAA1199 العالي على النمو السريع فحسب؛ بل كانت أيضاً تهيّئ الكبد ليصبح «مكانة سابقة للانبثاث»، أي بيئة مواتية بشكل غير عادي لخلايا السرطان الواردة. حتى عندما تم زرع أورام كبدية تجريبياً من مصدر منفصل، طورت الحيوانات التي تحمل أورام قولون عالية KIAA1199 عددًا أكبر بكثير من الانبثاثات الكبدية وتوفيت مبكراً. هذا أظهر أن إشارات من الورم الأساسي، وليس فقط خلايا السرطان المتجولة، كانت تعيد تشكيل الكبد مسبقاً.
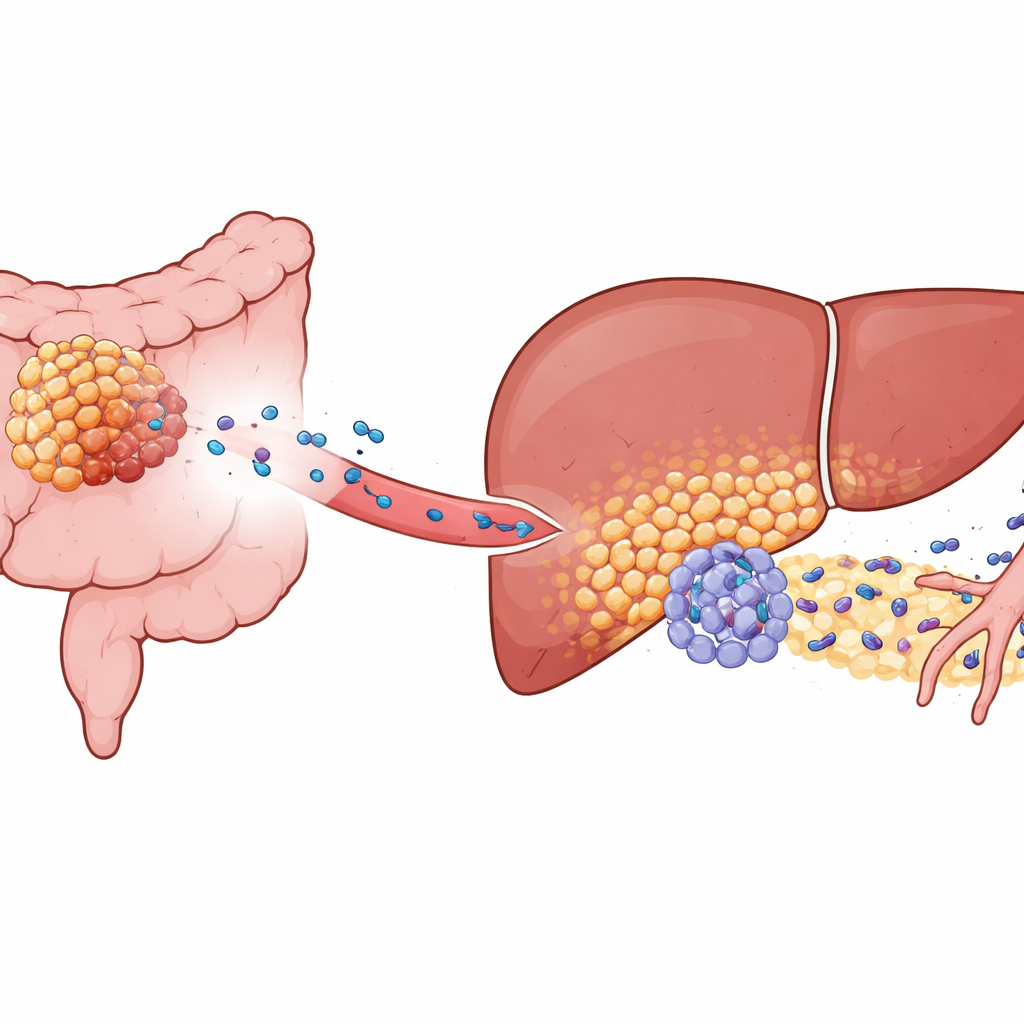
خلايا كبدية أُعيدت برمجتها لتصبح مساعدات للورم
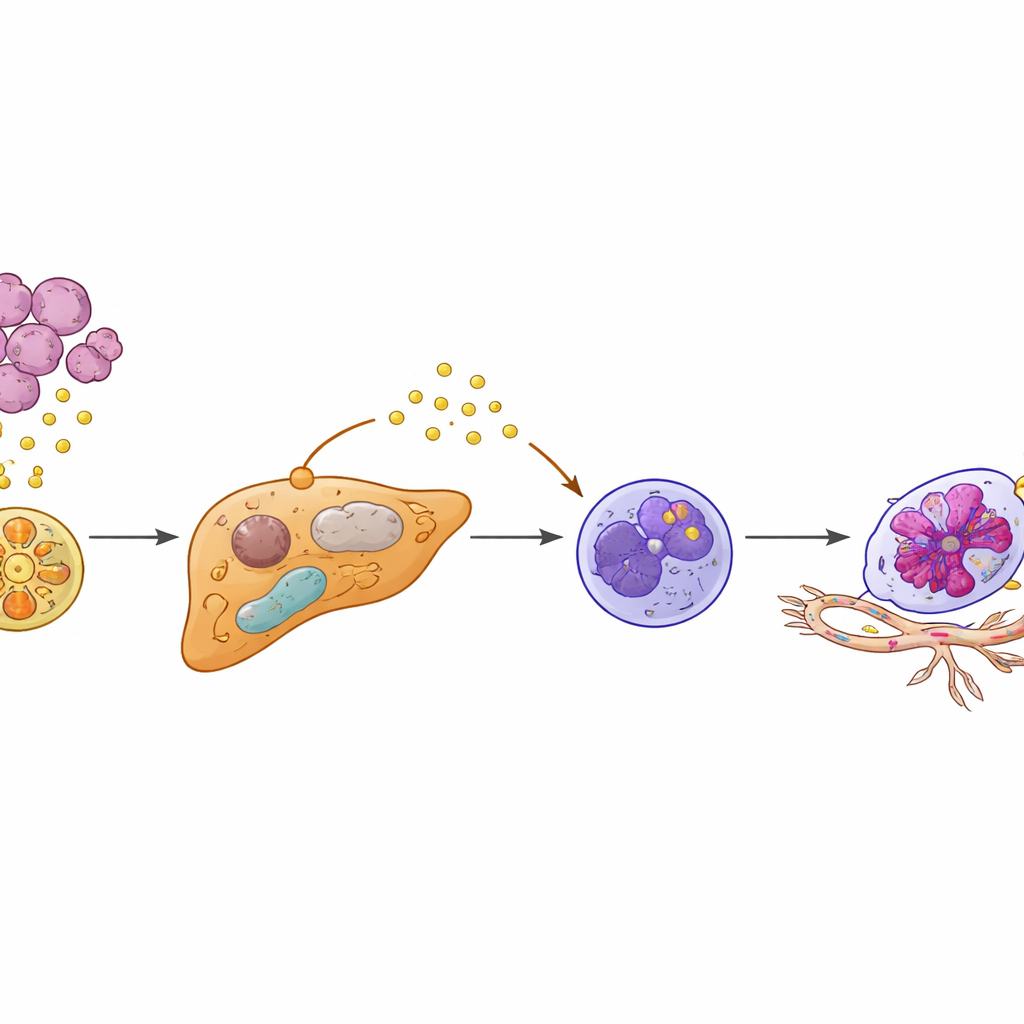
بتعمق أكبر، استخدم الباحثون التسلسل أحادي الخلية والخرائط المكانية لفحص نسيج الكبد بدقة عالية. اكتشفوا فئة مميزة من الخلايا الكبديّة — التي عادةً ما تكون خلايا عاملة للكبد — والتي تم «إعادة برمجتها وظيفياً». ظهرت هذه الخلايا فقط في وجود أورام عالية KIAA1199. بدلاً من إدارتها الهادئة للأيض، تحولت الخلايا الكبدية المعدّلة إلى نمط أيضي أشد شبهاً بالسطحية الخبيثة وخفّضت نشاط منظم وقائي يسمى PPARγ، الذي يساعد عادةً في ضبط الالتهاب واستجابات الإجهاد. مع كبت PPARγ، بدأت هذه الخلايا الكبدية في إنتاج مستويات عالية من بروتين يسمى SAA2، وأطلقته في محيطها، لا سيما على الحافة حيث يلتقي نسيج الكبد بالخلايا الورمية الغازية.
تحويل المدافعين العاديين إلى عدلات محفزة للانبثاث
العدلات — خلايا الدم البيضاء المعروفة بمحاربة العدوى — تصرفت أيضاً بشكل غريب في هذا الكبد المهيأ. وجد المؤلفون فئة مميزة تحمل توقيع «Egr1+»، سُميت نسبةً لعامل نسخ يعيد تشكيل كيفية عمل هذه الخلايا. بدلاً من أن تصل من مجرى الدم مُعدَّلة بالفعل، بدا أن العدلات تُعاد تثقيفها محلياً بواسطة الخلايا الكبدية المعاد برمجتها. ارتبط SAA2 المُطلَق من الخلايا الكبدية بمستقبل يسمى FPR2 على العدلات القريبة، مُفعّلاً دائرة إشارات داخلية عبر PI3K‑AKT التي ثبتت نشاط Egr1. النتيجة كانت عدلة طويلة العمر ونشطة للغاية تُفرز كميات كبيرة من VEGFA، وهو مُحرِّك قوي لتكوين أوعية دموية جديدة. تكتلت هذه العدلات Egr1+ على واجهة الورم‑الكبد، تماماً حيث كانت الأوعية الدموية الجديدة الهشة تنبثق.
بناء أوعية دموية ترحب بخلايا الورم
تظهر الدراسة أن هذه العدلات المعاد تثقيفها ليست ممثلين سلبيين — بل تعيد تشكيل أوعية الكبد فعلياً. في ثقافات خلوية، جعلت العوامل التي تفرزها العدلات Egr1+ الخلايا البطانية تنمو وتهاجر وتشكل هياكل أنبوبية تشبه الأوعية الجديدة. في الفئران، أدى إضافة العدلات Egr1+ إلى زيادة الانبثاثات الكبدية وتسريع الوفاة. إن حجب خطوات رئيسية في هذه السلسلة — إما إشارة SAA2–FPR2 إلى العدلات أو مسار PI3K‑AKT السفلي — أوقف بقاء العدلات وإنتاج VEGFA، مما قلل من نمو الأوعية وانتشار الانبثاث. وبالمثل، أدى استعادة نشاط PPARγ في الخلايا الكبدية باستخدام دواء السكري روزيغليتازون إلى خفض مستويات SAA2، وكبح ظهور العدلات Egr1+، وتقليل الانبثاث الكبدي بشكل حاد في النماذج قبل السريرية.
من الآلية إلى التنبؤ والوقاية
لأن KIAA1199 في الأورام وSAA2 في الكبد يقعان قرب قمة هذه الشلالية، اختبر المؤلفون ما إذا كانت هذه البروتينات قد تساعد في تمييز المرضى ذوي الخطر العالي للانبثاث الكبدي. في عدة مجموعات من المرضى، كان الأشخاص ذوو المستويات الدموية العالية لكلا العلامتين أكثر عرضة بكثير لتطوير الانبثاثات الكبدية ولحدوثها في وقت أقرب. تفوّق مقياس مركب بسيط يجمع KIAA1199–SAA2 على كل علامة على حدة في توقع الخطر، وتم تعبئته ضمن «نوموغرام» سريري يقدّر احتمال انتشار الكبد لدى مريض معين خلال العامين القادمين. ترسم النتائج معاً صورة واضحة: ترسل سرطانات القولون عالية KIAA1199 إشارات محمولة في الحويصلات تعيد توصيل الخلايا الكبدية، والتي بدورها تحول العدلات القريبة إلى شركاء طويلَي العمر وبانِي الأوعية. من خلال استهداف محور KIAA1199–PPARγ/SAA2–Egr1 هذا — عبر أدوية أيضية، عوامل مُعدّلة للمناعة، أو كليهما — قد يكون من الممكن ليس فقط علاج الانبثاثات الكبدية القائمة، بل منعها من التمكُّن أصلاً.
الاستشهاد: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
الكلمات المفتاحية: انبثاث سرطان القولون والمستقيم إلى الكبد, المكانة السابقة للانبثاث, العدلات, إعادة برمجة الخلايا الكبدية, البيئة الميكروية للورم