Clear Sky Science · ar
تقليل مثيلة الهيستون 3.3 لايزين 4 في النتوء العقدي الإنسي وتحت المهاد يعيد إنتاج أنماط اضطرابات التطور العصبي
كيف تشكل العلامات الكيميائية الصغيرة الدماغ والجسم
لماذا تتسبب بعض الطفرات الجينية في مشاكل تعلمية مع نمو غير اعتيادي، مثل أن يكون الفرد صغير الحجم في الطفولة ثم يعاني من السمنة في البلوغ؟ تبحث هذه الدراسة في علامات كيميائية صغيرة على بروتينات تغليف الحمض النووي في الدماغ وتبين كيف أن تعطيلها في منطقتين أساسيتين فقط يمكن أن يتسع تأثيره إلى نوبات صرع، سلوك يشبه القلق، اضطرابات في الذاكرة، وتغيرات دراماتيكية في حجم الجسم لدى الفئران.
مفاتيح ضبط شدة الجينوم
داخل كل خلية دماغية، يلتف الحمض النووي حول بروتينات شبيهة بالبكرات تسمى الهيستونات. تعمل العلامات الكيميائية الموضوعة على هذه الهيستونات كمفاتيح ضبط شدة، ترفع أو تخفض نشاط مجموعات من الجينات. إحدى هذه العلامات، المضافة في موضع يسمى H3K4، مرتبطة بقوة بتشغيل الجينات. كشفت دراسات جينية بشرية أن الأشخاص المولودين بعيوب في الإنزيمات التي تضيف أو تزيل هذه العلامة غالبًا ما يعانون اضطرابات نمائية عصبية تجمع بين إعاقة عقلية، صرع، ونمو جسدي غير طبيعي. ومع ذلك، لم يكن واضحًا أي خلايا دماغية هي الأكثر حساسية لهذا الاضطراب وكيف يمكن لخللها ربط فرط نشاط الدماغ بالتمثيل الغذائي للجسم بأكمله.
استهداف محورين دماغيين حاسمين
صمم الباحثون فئرانًا هندسية شغّلوا فيها نسخة متحورة من بروتين هيستون (H3.3K4M) فقط في الخلايا الناتجة عن منطقتين دماغيتين جنينيتين: النتوء العقدي الإنسي، الذي يولد العديد من خلايا الكبح التثبيطية في الدماغ، وتحت المهاد النامي، الذي يساعد على تنظيم الشهية والهرمونات وتوازن الطاقة. تمنع هذه الطفرة تحديدًا مثيلة H3K4 دون إزالة الهيستونات نفسها. أكدت الاختبارات وجود البروتين المتحور على نطاق واسع في المناطق المستهدفة وأن العلامات الطبيعية لـ H3K4 انخفضت هناك بينما ظلت مستويات الهيستون الإجمالية مستقرة. يحاكي هذا التصميم العديد من الحالات البشرية التي يكون فيها أحد نسختي الجين المرتبط بـ H3K4 معيبًا، بدلاً من أن يكون مفقودًا تمامًا.
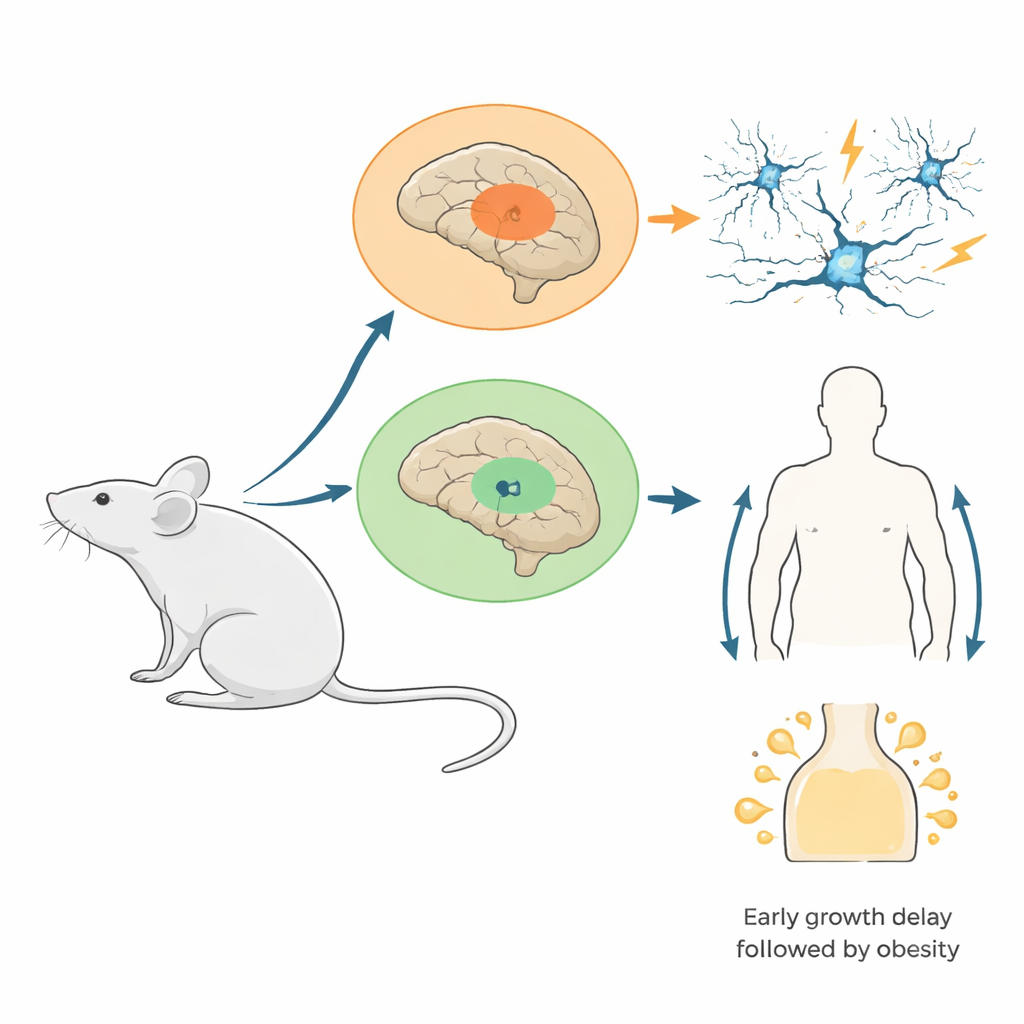
من نقص خلايا الكبح إلى دوائر عرضة للصرع
مع نمو هذه الفئران، اتضح تأثير ذلك على الدوائر الدماغية. كان لدى الصِغار المتحورين خلايا بينية تثبيطية أقل في القشرة والحصين، لا سيما نوع سريع الإطلاق الذي يحافظ عادة على توقيت الإيقاعات العصبية. أظهرت التسجيلات المفصلة أن الخلايا البينية المتبقية موجودة لكن ميزاتها الكهربائية كانت أكثر تذبذبًا، ما يوحي بتعطل نضجها. عند تحفيز الحصين في شرائح دماغية، كانت الاهتزازات عالية التردد المعروفة باسم «جاما»—وهي إيقاعات كهربائية مرتبطة بمعالجة المعلومات—أضعف وأبطأ، وظهرت أحداث متفجرة غير طبيعية. في الحيوانات الحية، طورت العديد من المتحورات، خاصة الإناث، نوبات عفوية وكانت أكثر حساسية بكثير للنوبات المحفزة دوائيًا. في المراحل المبكرة من التطور، تبع الفريق أن فقدان الخلايا كان في المقام الأول نتيجة هجرة ضعيفة للخلايا البينية إلى القشرة، وليس بسبب زيادة موت الخلايا أو انخفاض انقسامها.
إعادة توصيل نشاط الجينات في الخلايا المرتبطة بالصرع
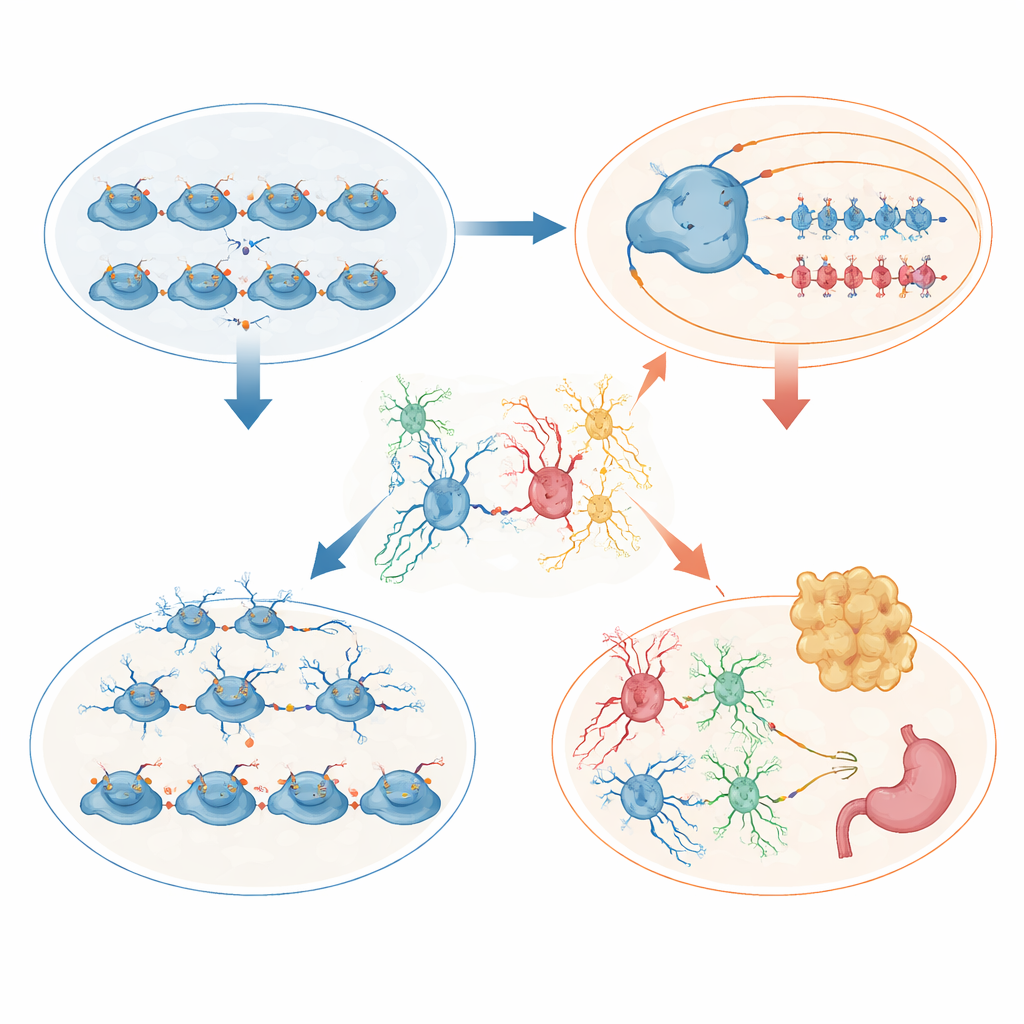
لربط هذه التغييرات المادية بتحكم الجينات، استخدم الفريق تسلسل نواة وحيدة يقرأ كلًا من نشاط الجينات وإتاحة الحمض النووي من خلايا فردية. في النتوء العقدي الإنسي الجنيني، كانت معظم الجينات المتغيرة في المتحورات منخفضة التعبير، بما في ذلك منظمات رئيسية توجه الخلايا نحو مصائر تثبيطية محددة. في الخلايا البينية البالغة، تغير التوازن بين الأنواع الفرعية، وكانت مجموعات من الجينات المشاركة في تشكيل الوصلات والتحكم في تيارات البوتاسيوم—تدفقات تساعد على تحديد سرعة الإطلاق—غير منظمة. أبرز تحليل الشبكات تعطّلًا منسقًا في جينات قنوات البوتاسيوم المعروفة بالفعل بتأثيرها على الصرع وإيقاعات الدماغ، مما يوفر رابطًا جزيئيًا مباشرًا بين فقدان علامة الهيستون، تغير هوية الخلايا البينية، وحساسية الصرع.
اختلال تحت المهاد ومنحنى نمو من مرحلتين
روى تحت المهاد قصة مكملة تركزت على نمو الجسم. كجِراء، كان الفئران المتحورة أصغر وحصة كبيرة منها ماتت مبكرًا. الناجون، مع ذلك، أكلوا لاحقًا أكثر، تراكمت لديهم الدهون، وارتفعت مستويات هرمون اللبتين، مما يشير إلى السمنة ومقاومة محتملة للّبتين. كشف تحليل الخلايا المفردة لتحت المهاد الجنيني عن عدد أكبر من الخلايا الجذعية المنقسمة لكن عددًا أقل من الخلايا المقررة لنوى رئيسية متعلقة بالتغذية، وخاصة المناطق التي عادة ما تستشعر الحالة الغذائية وتنظم هرمون النمو. في تحت المهاد البالغ، تغيرت التركيبة الخلوية: زادت النجميات بشكل حاد، انخفضت الخلايا قليلة التغصن، وفقدت خلايا حاجز متخصصة تُدعى التانيسايتس والخلايا الداعمة المجاورة انتظامها عند واجهة الدماغ مع الهرمونات والمواد المغذية الدائرة. من المحتمل أن تشوهات التركيب هذه وتغيرات التعبير الجيني تضعف الطريقة التي يستشعر بها الدماغ مخزون الطاقة وينظم الشهية.
صدى سلوكي لاضطرابات النمو العصبي البشرية
عكست سلوكيات الفئران أعراضًا تُرى في العديد من حالات اضطرابات النمو العصبي. أظهرت سلوكًا يشبه القلق أقوى، مشية متغيرة، نشاطًا تلقائيًا منخفضًا في المنزل، وأداء ضعيفًا في مهام تقيس الذاكرة والتعرُّف على الأشياء وتنقية الأصوات المفاجئة. كشفت بعض الاختبارات عن زيادة في السلوكيات الاندفاعية. عبر مقاييس متعددة، بدا أن الإناث تتأثر أكثر من الذكور، مما يوحي بتفاعل أنظمة هرمونات الجنس وتنظيم الجينات مع علامات الهيستون لتشكيل قابليات خاصة بالجنس.
ماذا يعني هذا لصحة الإنسان
تُظهر النتائج معًا أن إضعاف مجموعة من علامات الهيستون في محوري دماغ جنينيين فقط يكفي لإعادة إنتاج مجموعة واسعة من المشاكل: قلة «مكابح» تثبيطية، شبكات دماغية غير مستقرة، نوبات صرع، دوائر تغذية مضطربة، ونمو جسدي غير طبيعي. للقراء غير المتخصصين، الرسالة الأساسية أن العلامات فوق الجينية مثل مثيلة H3K4 ليست إضافات غامضة بل هي مقابض تحكم دقيقة تساعد خلايا الدماغ النامية على أن تصبح النوع الصحيح، في المكان الصحيح، وفي الوقت المناسب. عندما تُضبط هذه المقابض خطأ، كما في العديد من المتلازمات الجينية النادرة، قد تكون النتيجة توليفة مترابطة من الأعراض المعرفية والسلوكية والتمثيلية. قد يوجه فهم هذه الجذور المشتركة في النهاية علاجات تصحح ليس عرضًا واحدًا مثل النوبات أو السمنة، بل النظام المترابط الذي ينشأ منهما.
الاستشهاد: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
الكلمات المفتاحية: علم التخلق فوق الجيني, الخلايا البينية, تحت المهاد, نوبات صرع, السمنة