Clear Sky Science · ar
فصل الطور عن التليف يحافظ على نشاط المكثفات البيومولكولية
لماذا هذا مهم لصحة الدماغ
تشمل العديد من أمراض الدماغ، بما في ذلك مرض الزهايمر، بروتينات تتكتل مع مرور الوقت إلى تشابكات صلبة وألياف ليفية. نفس هذه البروتينات يمكن أن تشكل أيضاً هياكل أكثر ليونة على شكل قطرات داخل الخلايا تساعد في تنظيم الكيمياء، تشبه محطات عمل سائلة صغيرة. تطرح هذه الدراسة سؤالاً جوهرياً: هل يمكننا إيقاف تصلب هذه القطرات الضارة إلى ألياف دون تدمير وظيفتها المفيدة اليومية؟ يظهر المؤلفون أن ناتج أيض خلوي شائع، الحمض الأميني إل-أرجينين، قادر تماماً على فعل ذلك لبروتين رئيسي مرتبط بمرض الزهايمر يُدعى تاو.
من بروتين طافٍ إلى قطرات دقيقة
داخل الخلايا، بعض البروتينات لا تبقى دائماً مخلوطة بشكل متساوٍ في السائل الداخلي. بدلاً من ذلك، يمكنها التجمع إلى قطرات تُسمى مكثفات بيومولكولية، تتصرف مثل جيلاتين ناعم جداً أو سوائل لزجة. ركز الفريق على تاو، وهو بروتين يساعد عادة في بناء وتثبيت الأنابيب الدقيقة—خيوط مجوفة تعمل كطرق داخل الخلايا العصبية. كما يشتهر تاو بتشكيل الألياف الأميلويدية الصلبة الموجودة في التشابكات المرتبطة بالعديد من أمراض التنكس العصبي. لدراسة كيف تتطور قطرات تاو مع الزمن، صمّم الباحثون نسخة من البروتين أطلقوا عليها اسم SynTag-Tau، والتي تكون مكثفات نشطة تتقدم إلى ألياف أميلويدية على مقياس زمني مناسب للتجارب، دون الحاجة إلى إضافات قاسية.
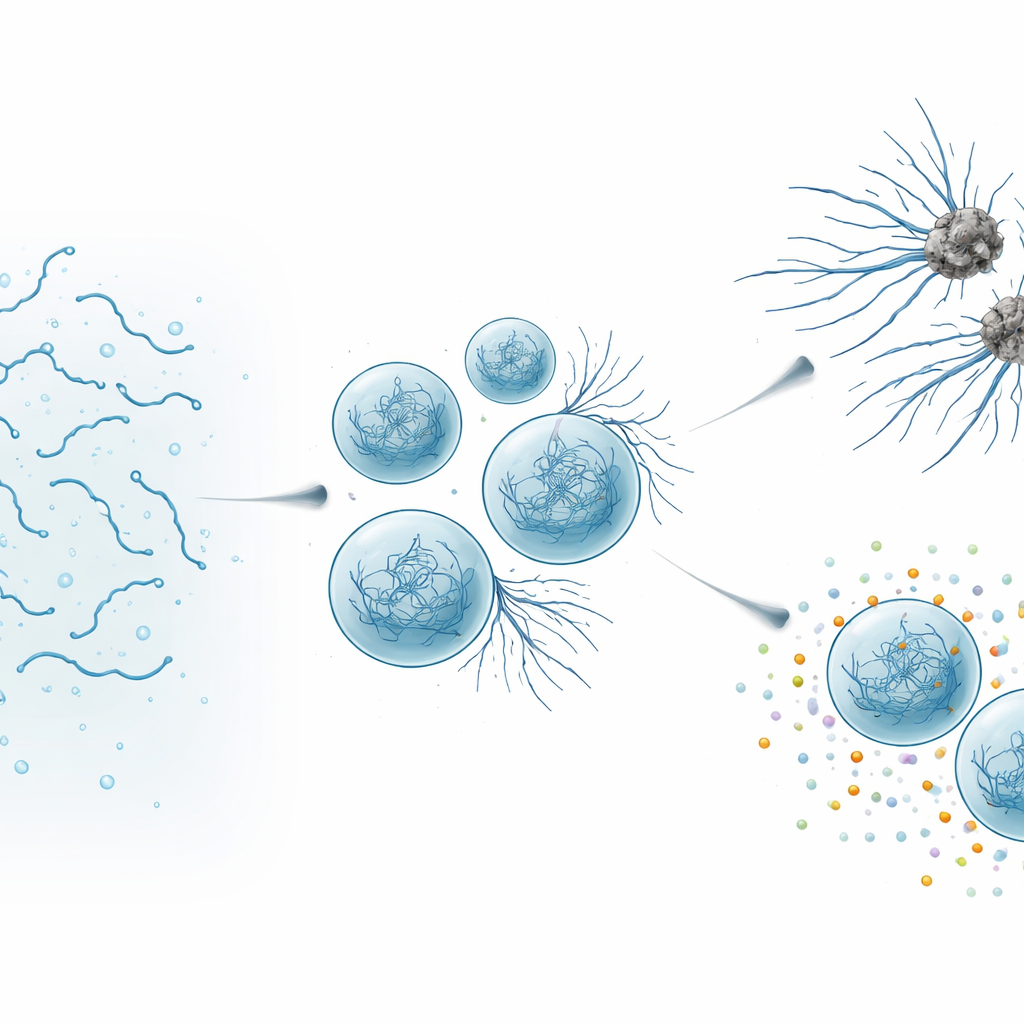
عندما تتحول القطرات المفيدة إلى ضارة
باستخدام مجهر عالي الدقة وقياسات فيزيوكيميائية، راقب المؤلفون قطرات SynTag-Tau وهي تتغير على مدى ساعات. تصرفت القطرات الطازجة كسوائل: اندمجت بسهولة، وكانت جزيئاتها تتحرك بسرعة، ولم يظهر أي دليل على بنية مرتبة. مع مرور الوقت، تباطأت القطرات وتصلبت، وبدأت ألياف رفيعة تنبت من أسطحها إلى الوسط المحيط. أظهرت أساليب بصرية حساسة أن هذه الألياف احتوت على الهندسة المكدسة الضيقة "عبر-بيتا" النموذجية للأميلويد. ومن المهم أن واجهة القطرات—الحد الفاصل بين الكتلة الكثيفة والسائل المحيط—عملت كبقعة ساخنة حيث ظهرت الألياف أولاً. ومع شيخوخة القطرات ونمائها للمزيد من الألياف، تضررت وظيفة تاو المعتادة: أصبحت المكثفات أقل قدرة على جذب التوبيولين، وحدة بناء الأنابيب الدقيقة، وفقدت في نهاية المطاف قدرتها على دعم تجميع الأنابيب الدقيقة تماماً.
جزيئات صغيرة تحرّك الميزان
سأل الباحثون بعد ذلك ما إذا كانت المستقلبات البسيطة يمكن أن تبطئ أو تمنع هذا الانتقال من سائل إلى ألياف مع إبقاء القطرات نفسها سليمة. من خلال فحص عدة جزيئات صغيرة موجودة طبيعياً، وجدوا أن الأحماض الأمينية موجبة الشحنة مثل إل-أرجينين وإل-لايسين تؤخر أو تمنع بقوة تكوّن الألياف الأميلويدية من قطرات SynTag-Tau، لكنها لا تقمع تكون القطرات عند تراكيز منخفضة قابلة للتصديق في الميليمول. بالمقابل، سرّعَت الأحماض الأمينية سالبة الشحنة مثل الجلوتامات والاسبارتات تشكيل الألياف، والكيميائيات العامة التي تعطل البروتينات إما فشلت في المساعدة أو أضرت بالقطرات نفسها. كشف نظير فلوري للإل-أرجينين أن هذا الجزيء يفضّل التواجد داخل مكثفات تاو أكثر من خارجها، مما يوحي بأنه يعمل حيث يكون مطلوباً بشدة.
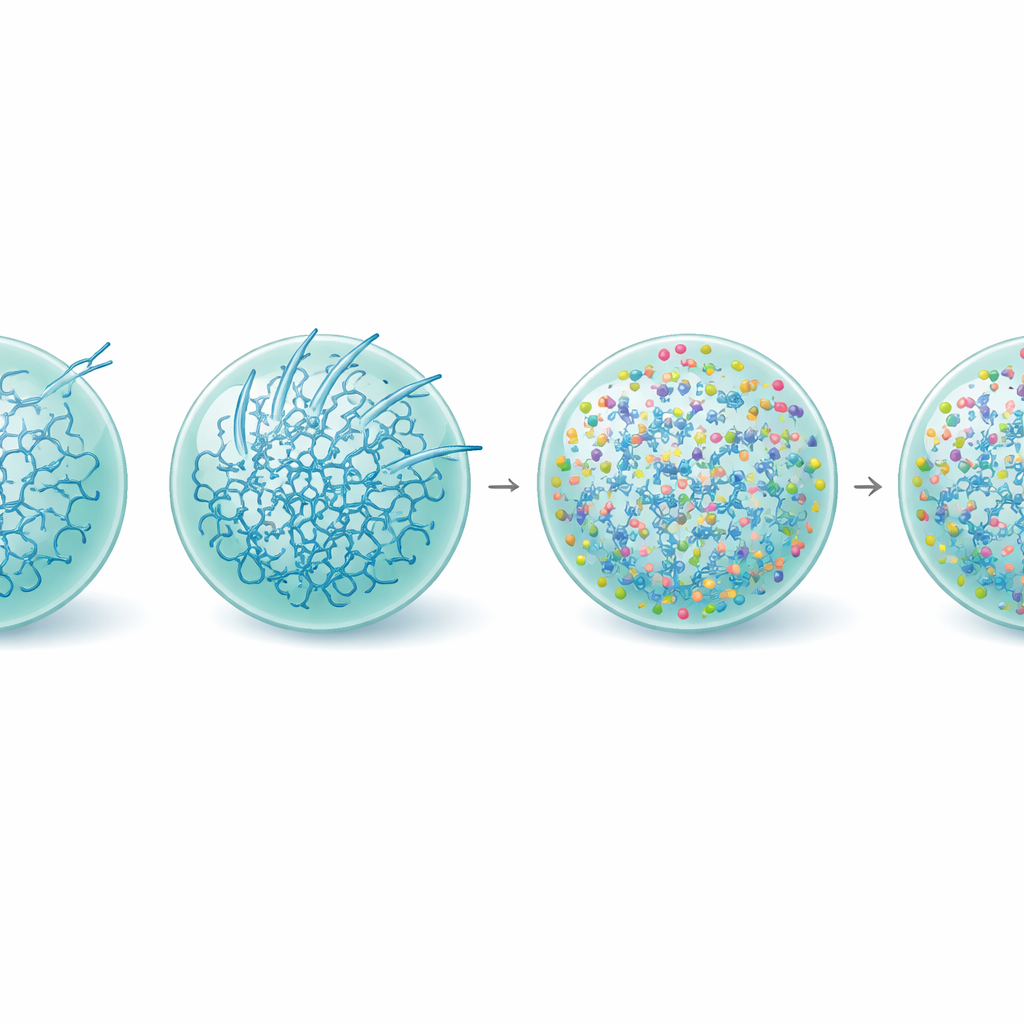
تصلب القطرات، وإنقاذ الوظيفة
بتعمق أكبر، فحص الفريق كيف يعيد إل-أرجينين تشكيل الحياة الداخلية لقطرات تاو. أظهرت قياسات بنية البروتين أنه بوجود إل-أرجينين، انخفضت نسبة جزيئات تاو التي تتبنى الأشكال الصلبة الغنية بالبيتا المرتبطة بالأميلويد، حتى في القطرات الأقدم. كشفت نانورولوجيا قائمة على الفيديو—تتبع حركة حبيبات صغيرة داخل المكثفات—أن إل-أرجينين جعل قطرات تاو أكثر لزوجة مرنة، بمعنى أن الشبكة الداخلية أصبحت أقوى وأكثر ترابطاً بينما ظلت تشبه السائل. يبدو أن هذا التقوية تبقي النظام في حالة مستقرة مؤقتاً ووظيفية وتزداد الحاجز الطاقي لتكوين الألياف، لا سيما عند سطح القطرات. تماشياً مع ذلك، استمرت المكثفات المعاملة بإل-أرجينين في تجنيد التوبيولين بشكل متساوٍ ودعمت نمو الأنابيب الدقيقة طويلاً بعد أن أصبحت القطرات غير المعاملة خاملة.
ما الذي يعنيه هذا للعلاجات المستقبلية
تُظهر الدراسة أن القوى التي تقود تشكيل قطرات البروتين وتلك التي تدفع تكوين الألياف الضارة مرتبطة لكنها قابلة للفصل. من خلال تعديل الكيمياء داخل المكثفات بمستقلب مثل إل-أرجينين، من الممكن الحفاظ على الحالة المفيدة الشبيهة بالسائل مع تأخير أو منع الانتقال إلى الألياف الأميلويدية المرتبطة بالمرض. على الرغم من أن هذه الدراسة تستخدم نظام تاو مُهندَساً خصيصاً في المختبر، فإنها تقدم دليل مبدئي: قد تساعد الجزيئات الصغيرة التي تعزز استقرار المكثفات بشكل انتقائي يوماً ما في حماية الخلايا من تراكم الأجسام البروتينية السامة تدريجياً دون منع الأدوار التنظيمية الطبيعية للمكثفات البيومولكولية.
الاستشهاد: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
الكلمات المفتاحية: بروتين تاو, المكثفات البيومولكولية, الألياف الأميلويدية, إل-أرجينين, التحلل العصبي