Clear Sky Science · ar
الأساس الجزيئي للغلاكتوزلة الكولاجين بواسطة GLT25D1
كيف تساعد وسمات السكر الصغيرة في بناء أنسجة قوية
يعد الكولاجين أكثر بروتين شائع في الجسم، ويشكّل السقالة للجلد والعظام والأوعية الدموية والعديد من الأنسجة الأخرى. لكن الكولاجين لا يعمل بمفرده: يجب تزيينه بجزيئات سكرية صغيرة في مواضع دقيقة ليكتسب الصلابة والمرونة المناسبتين. تكشف هذه الدراسة، بتفصيل ذري، كيف يقوم إنزيم أساسي واحد، GLT25D1، بإرفاق سكر معين بالكولاجين وكيف أن خللاً في هذه العملية قد يؤدي إلى أوعية هشة ومشاكل عضلية وربما إلى السرطان.
نظرة أقرب على التعديل الخفي للكولاجين
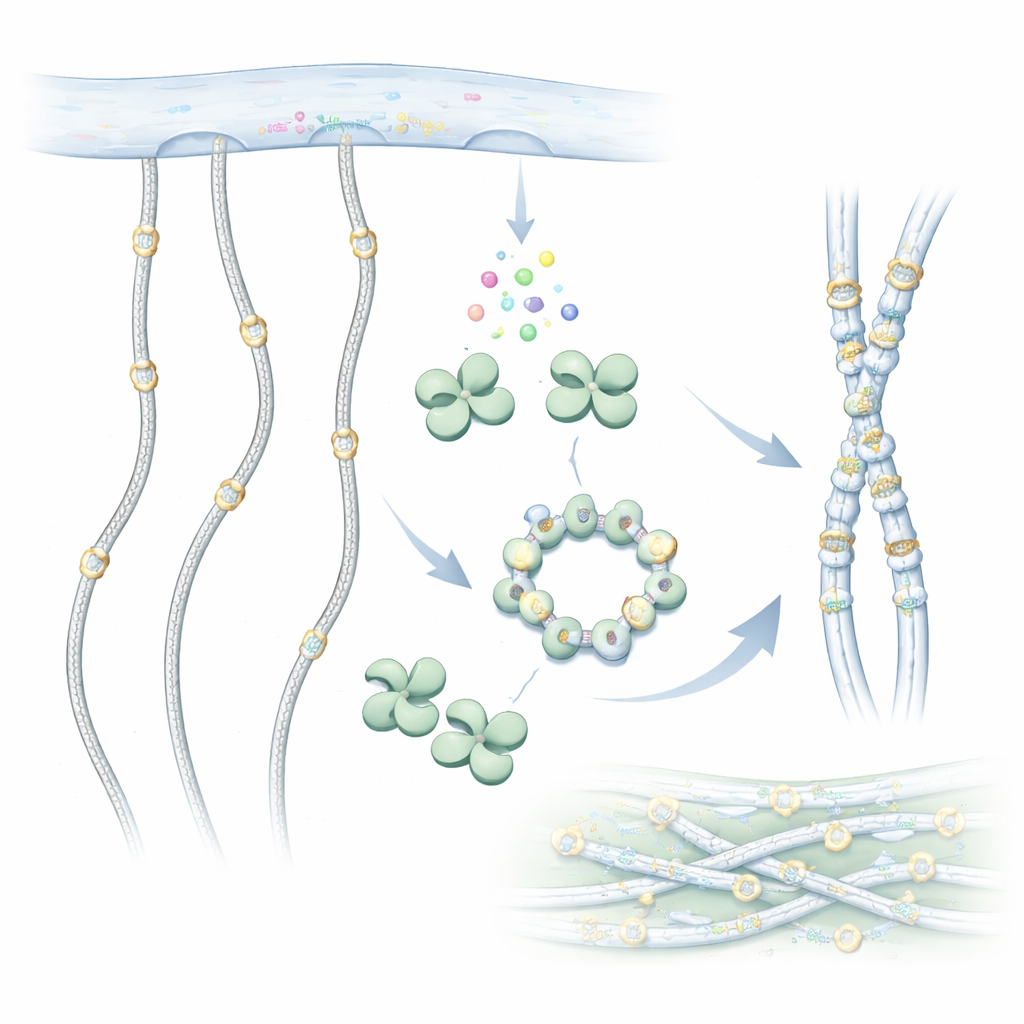
جزيئات الكولاجين طويلة وتشبه الحبال وتترتب لتكوّن أليافًا متينة خارج الخلايا. قبل خروجها من الخلية، تُجرى عليها تعديلات كيميائية. أحد التعديلات المهمة هو إضافة مجموعات سكرية إلى لبنات بناء خاصة تُسمى هيدروكسيليزينات على سلسلة الكولاجين. يقوم GLT25D1 بالخطوة الأولى في وسم السكر هذا، ناقلاً سكر الجالاكتوز من جزيء مانح إلى الهيدروكسيليزين. هذا التزيين السكري محفوظ عبر الكائنات من البسيطة إلى الإنسان ويساعد الكولاجين على الطي الصحيح والتفاعل مع الخلايا ومقاومة التلف والاهتراء.
كشف شكل مُزيّن الكولاجين
لفهم كيف يعمل GLT25D1، استخدم الباحثون المجهر الإلكتروني بالتجميد لتصوير الإنزيم البشري بدقة تقارب الذرية. اكتشفوا أن كل جزيء من GLT25D1 يحتوي على فصّين متشابهين، كلاهما مرتبط بطيّة إنزيمية شائعة تُرى في بروتينات ناقلة للسكريات. تتزاوج هذه الفصوص لتشكّل ثنائيات ممدودة، ويمكن لثلاث ثنائيات أن تتجمع أكثر لتكوّن سداسيًا على شكل حلقة. في هذه التجمعات، تقع مراكز النشاط — وهي الآلات الحقيقية — متباعدة إلى حد بعيد، وهو ترتيب قد يسمح لعدة مواقع إضافة سكر بالعمل على طول سلسلة كولاجين مشدودة في آن واحد.
الأجزاء العاملة: أين يحدث نقل السكر فعلاً
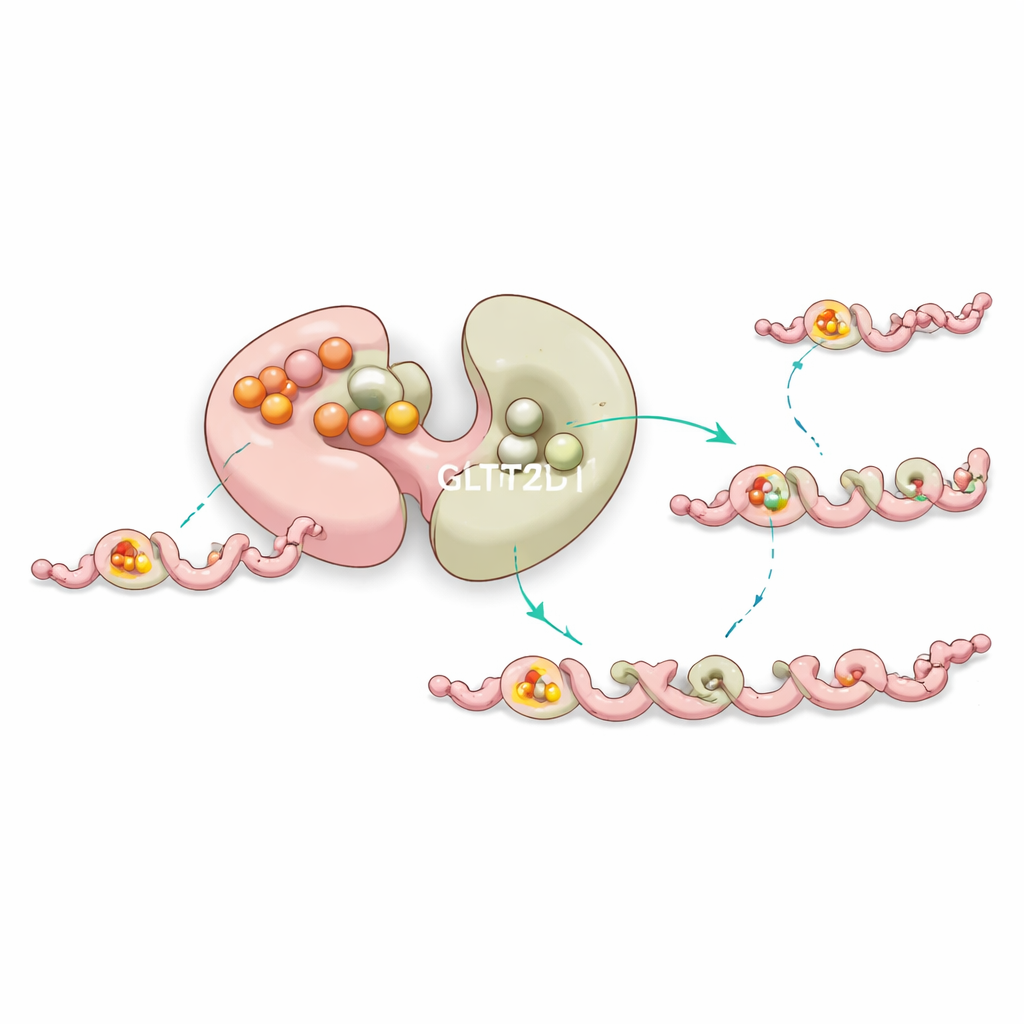
حل الفريق هياكل GLT25D1 مربوطًا بكل من المانح السكري وببتيد قصير شبيه بالكولاجين يحتوي على هيدروكسيليزين. أظهر هذا المعقد الثلاثي أن الفص الثاني فقط، المسمى المجال الطرفي-C، هو الذي يقوم بالفعل بالتفاعل الكيميائي. هناك يستقر جزيء المانح في جيب يُثبت بواسطة أيون معدني، بينما يستلقي الببتيد في أخدود ضيق يفرض نمطاً محلياً محدداً: هيدروكسيليزين يتبعه فوراً غليسين صغير. يعمل بقايا حمض الأسبارتيك المفرد كقاعدية كيميائية، مفعلة مجموعة الهيدروكسيل في الهيدروكسيليزين لتهاجم السكر وتتمم النقل. تؤدي التغيرات في أي من هذه الأحماض الأمينية الأساسية إلى تقليل النشاط كثيراً أو إلغائه، مما يؤكد أدوارها الحيوية.
مثبّت مدمج وتحكم على مدى بعيد
من الغريب أن الفص الأول من GLT25D1 يرتبط بجزيء مانح السكر بقوة كبيرة لكنه لا يجري النقل. بدلًا من ذلك، تشير التجارب والمحاكاة الحاسوبية إلى أن هذا الموقع «الصامت» يساعد على استقرار الإنزيم ويضبط بسلاسة سلوك الفص النشط عبر تواصل طويل المدى داخل البروتين. غالبًا ما تؤدي الطفرات القريبة من هذا الجيب غير التحفيزي إلى إضعاف استقرار الإنزيم أو تغيير كفاءته، ما يوحي بأن الطبيعة تستخدم موقع الارتباط الإضافي هذا كشكل من أشكال ضبط الجودة الداخلية للحفاظ على سير تعديل الكولاجين بسلاسة.
عندما يفشل المُزيّن: روابط مع المرض
من خلال وضع الطفرات المشتقة من المرضى على نموذجهم البنيوي، استطاع المؤلفون تفسير كيف تؤدي الأخطاء في GLT25D1 إلى أمراض بشرية. بعض الطفرات تقطع الفص التحفيزي تمامًا، وأخرى تزعزع استقرار نواة البروتين، وبعضها يهاجم مباشرة مواقع ربط السكر أو الكولاجين. تقلل هذه العيوب أو تقضي على إضافة السكر إلى الكولاجين وقد رُبطت بمرض أوعية دموية صغيرة في الدماغ ومشكلات إدراكية وعيوب عضلية وهيكلية. كما تتجمع الطفرات المرتبطة بالسرطان في مناطق حاسمة، ما يشير إلى أن تغيير تزيين الكولاجين قد يؤثر على نمو الورم وانتشاره.
لماذا يهم هذا للصحة والعلاجات المستقبلية
من خلال وضع مخطط ثلاثي الأبعاد مفصّل لـ GLT25D1 أثناء عمله، تشرح هذه الدراسة كيف تُضاف وسومات سكرية دقيقة إلى الكولاجين ولماذا هذه الخطوة مهمة جداً لسلامة الأنسجة. للغير متخصصين، الرسالة الرئيسية أن تغييرات كيميائية صغيرة على الكولاجين يمكن أن يكون لها تأثيرات كبيرة على الأوعية الدموية والعظام وربما على خطر السرطان. تُقدم الخريطة الهيكلية لـ GLT25D1 الآن دليلاً لتشخيص الطفرات الضارة ولتصميم علاجات — سواء جزيئات صغيرة تثبت الإنزيمات المعطوبة أو استراتيجيات قائمة على الجينات — التي قد تصل إلى تصحيح عيوب وسم الكولاجين من مصدرها يومًا ما.
الاستشهاد: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
الكلمات المفتاحية: جليكوزلة الكولاجين, GLT25D1, المصفوفة خارج الخلوية, أمراض الأوعية الدموية, بنية بالتجميد-الإلكترون (cryo-EM)