Clear Sky Science · ar
نقص السكليروستين يجعل الخلايا الدهنية البيضاء أكثر حساسية لإشارات إنتاج الحرارة التي تُحدث تحولًا إلى الدهون البيج في الفئران
لماذا تسخين دهنك قد يبرد المرض
معظمنا يفكر بالعظم والدهون الجسدية على أنهما عالمان منفصلان: أحدهما يمنحنا الهيكل، والآخر يخزن الطاقة. تكشف هذه الدراسة في الفئران أن العظم والدهون في محادثة كيميائية دائمة، وأن بروتينًا تصنعه خلايا العظام يمكنه أن يقرّر ما إذا كانت دهوننا «البيضاء» تظل مخزنةً للسعرات أم تتحول إلى دهون أكثر نشاطًا وحارقة للسعرات تُعرف بالـ«بيج». فهم هذا الحوار الخفي قد يفتح سبلًا جديدة لمواجهة السمنة والسكري وفقدان العظام معًا.
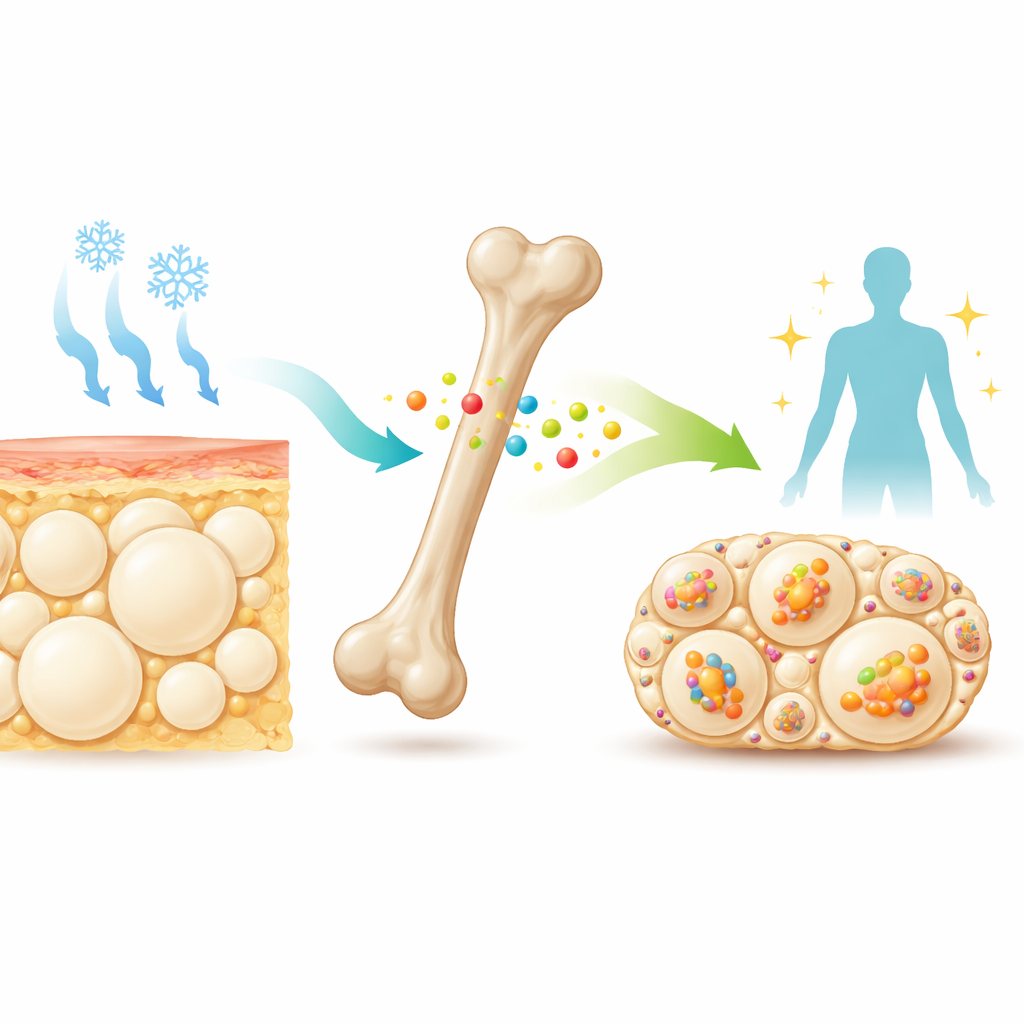
مُرسل هادئ من العظم
في أعماق العظام، تُفرز خلايا متخصّصة بروتينًا صغيرًا يُدعى السكليروستين إلى مجرى الدم. يهدف الأطباء بالفعل إلى السكليروستين بأدوية لتقوية العظام لدى المرضى المعرضين للكسور. أظهرت أعمال سابقة أن الفئران التي تفتقر إلى السكليروستين ليست قوية العظام فحسب، بل أضيق وزنًا وأكثر حساسية للإنسولين. دهونها تحت الجلد، خصوصًا حول الوركين (الدهون البيضاء الإربيّة)، تحتوي على خلايا دهنية صغيرة متعددة الحجيرات تشبه الدهون «البيج» القادرة على حرق الوقود لإنتاج الحرارة. قادت هذه الدلائل الباحثين إلى التساؤل عما إذا كان السكليروستين يعمل عادةً كفرامل لقدرة الجسم على تحويل الدهون البيضاء إلى بيج عند التعرض للبرد أو لأدوية تُحاكي إشارات الأعصاب إلى الدهون.
إشارات البرد، إشارات العظم، وإشعال الدهون
عرض الفريق فئرانًا طبيعية وفئرانًا تفتقر إلى جين السكليروستين (Sost-/-) لعقار ينشّط مستقبلًا محددًا في الخلية الدهنية (مستقبل β3-الأدرينيرجي)، أو لتعريضها لبرودة خفيفة. في الحيوانات الطبيعية، أدت هذه الإشارات الحرارية إلى زيادة إنتاج السكليروستين في العظم ورفع مستوياته في الدم. ارتبط هذا الارتفاع بفقدان في العظم الإسفنجي لكن بتغيرات متواضعة فقط في الدهون تحت الجلد. على النقيض من ذلك، أظهرت الفئران الخالية من السكليروستين استجابة أقوى بكثير: امتصت دهونها الإربيّة المزيد من الجلوكوز، وأطلقت أحماضًا دهنية أكثر، تقلص حجمها، وتمتلئ بخلايا شبيهة بالبيج مكدسة بالميتوكوندريا، مصانع طاقة الخلية. اشتغلت جينات حرارية رئيسية بقوة أكبر في هذه الفئران، خصوصًا في الدهون تحت الجلد، في حين أن الدهون البنية التقليدية لم تتغير إلى حد كبير.
ضبط حرق الدهون عبر مفتاح مشترك
لفهم كيف يمارس السكليروستين هذا التحكم، ركز الباحثون على بيتا-كاتينين، بروتين مشارك في مسار إشارة Wnt الذي يقمعه السكليروستين عادةً في العظم. في الدهون، أدت تنشيط بيتا-كاتينين بعد الولادة إلى دفع الخلايا البيضاء نحو حالة شبيهة بالبيج وزادت استجابتها لإشارات β3-الأدرينيرجي، لكن هذا التأثير اختفى عندما وُضعت الفئران في بيئة دافئة حراريًا حيث لم يعد الجسم بحاجة إلى حرارة إضافية. بالمقابل، محو بيتا-كاتينين تحديدًا في الخلايا الدهنية لدى الفئران الخالية من السكليروستين أزال دهون البيج لديها، وأعاد خلايا دهنية بيضاء أكبر، وعكس التحسّن في مستويات الإنسولين والأحماض الدهنية. تقترح هذه التجارب أنه عندما يكون السكليروستين منخفضًا، يصبح بيتا-كاتينين داخل الخلايا الدهنية رافعة داخلية مهمة تجعل الدهون البيضاء أكثر استجابة للإشارات الحرارية.
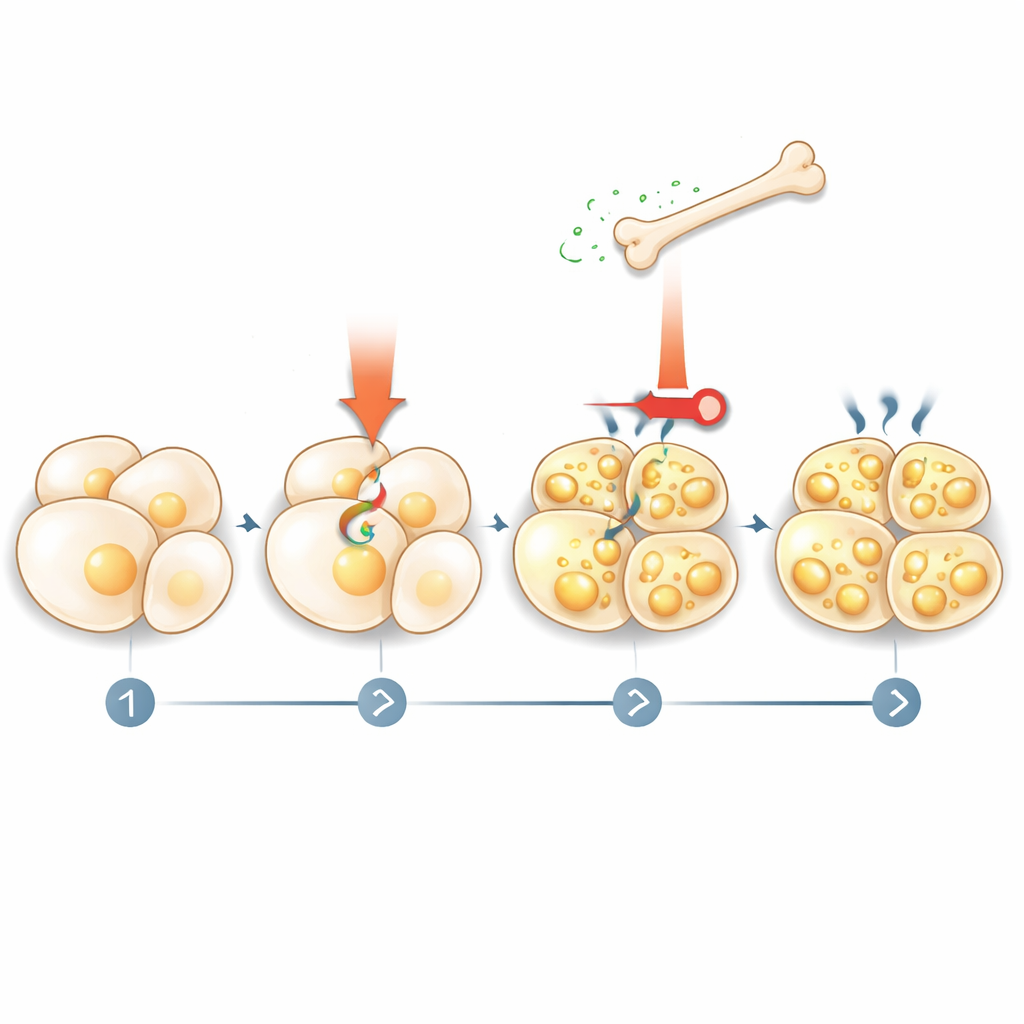
كيف ترد الدهون على العظم
لم تنتهِ القصة عند أن العظم يأمر الدهون بما عليها فعله. وجد الفريق أن التحفيز الحراري ينشّط تفتت الدهون (الليبوليزيز)، مطلقًا أحماضًا دهنية إلى الدم. تعمل هذه الأحماض الدهنية بدورها على خلايا العظم عبر مستقبل نووي يُدعى PPARγ، فتعزز إنتاج السكليروستين. عندما أعاق الباحثون الليبوليزيز في الخلايا الدهنية أو أزالوا PPARγ من خلايا العظم، لم تعد الأدوية المحاكية للبرد قادرة على رفع مستويات السكليروستين. يكشف هذا عن حلقة تغذية راجعة: الإشارات الحرارية تحفز الدهون على إطلاق الوقود، ويخبر هذا الوقود العظم بإفراز المزيد من السكليروستين، فيُعيد السكليروستين بدوره كبح مزيد من تفعيل الدهون وتحولها إلى بيج.
مزاوجة أدوية العظم والدهون للصحة الأيضية
أخيرًا، اختبر الباحثون ما إذا كان تعطيل هذه الحلقة قد يساعد في حالة تشبه المرض. تلقت الفئران السمنة على نظام غذائي عالي الدسم جرعة منخفضة من ميرابغرون (عقار β3-أدرينيرجي مستخدم بالفعل لمشاكل المثانة)، أو جسمًا مضادًا يعادل السكليروستين (روموسوزوماب، مصدق لعلاج هشاشة العظام)، أو كلاهما. بينما كان لكل دواء وحده تأثيرات متواضعة، قلّص المزيج كتلة الدهون في مواقع رئيسية، وحوّل الدهون نحو خلايا أصغر وأكثر نشاطًا، وخفض الإنسولين والدهون الثلاثية والكوليسترول، وحافظ على قوة العظم. الإسكان في بيئة دافئة، التي تقلل حاجة الجسم للحرارة، ألغى إلى حد كبير الفوائد الأيضية لفقدان السكليروستين، ما يؤكد أن هذا المسار يكون ذا أهمية أكبر عندما تكون الإشارات الحرارية حاضرة.
ماذا يعني ذلك للعلاجات المستقبلية
بعبارات بسيطة، تُظهر هذه الدراسة أن العظم ليس مجرد سقالة خاملة بل منظم فعال لمدى حرق خلايا الدهون للطاقة. يعمل السكليروستين كقِبْضَة تحكّم تبقي نشاط الدهون المولّدة للحرارة، وبالتالي استهلاك الوقود، تحت السيطرة. خفض هذه القِبْضَة — بالجينات أو بالأدوية — يجعل مخازن دهون بيضاء معينة أكثر ميلاً للتحول إلى وضعية توليد الحرارة عندما يُحفز الجسم بالبرد أو بأدوية محددة. وبما أن نفس التدخّل يمكن أن يقوّي العظام ويحسّن الصحة الأيضية في الفئران، فقد تساعد مجموعات مصممة بعناية من علاجات موجهة إلى العظم والدهون يومًا ما في معالجة السمنة والسكري وهشاشة العظام معًا، بدلًا من التعامل مع كل مرض على حدة.
الاستشهاد: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
الكلمات المفتاحية: السكليروستين, الدهون البيج, التواصل العظمي–الدهني, تكوّن الحرارة, الأمراض الأيضية