Clear Sky Science · ar
أفوريسيرتيب مع فولفيسترانت لسرطان الثدي المتقدم الإيجابي لمستقبلات الهرمونات وسالب HER2 بعد علاج سابق: تجربة المرحلة Ib
لماذا تهم هذه الدراسة المرضى والأسر
بالنسبة لعدد كبير من المصابين بسرطان الثدي المتقدم، يمكن لأدوية اليوم أن تُسيطر على المرض لفترة، لكن في كثير من الأحيان يتعلّم السرطان في نهاية المطاف كيف ينمو مجدداً. تختبر هذه الدراسة تركيبة دوائية جديدة تهدف إلى «إعادة قفل» بعض مفاتيح النمو التي تستخدمها الخلايا السرطانية بعدما تصبح مقاومة للعلاجات الهرمونية القياسية. فهم ما إذا كانت هذه الإستراتيجية فعالة، ومدى أمانها، قد يفتح خياراً إضافياً للمرضى الذين خضعوا لعدة جولات من العلاجات بالفعل.
شريك جديد للعلاج الهرموني
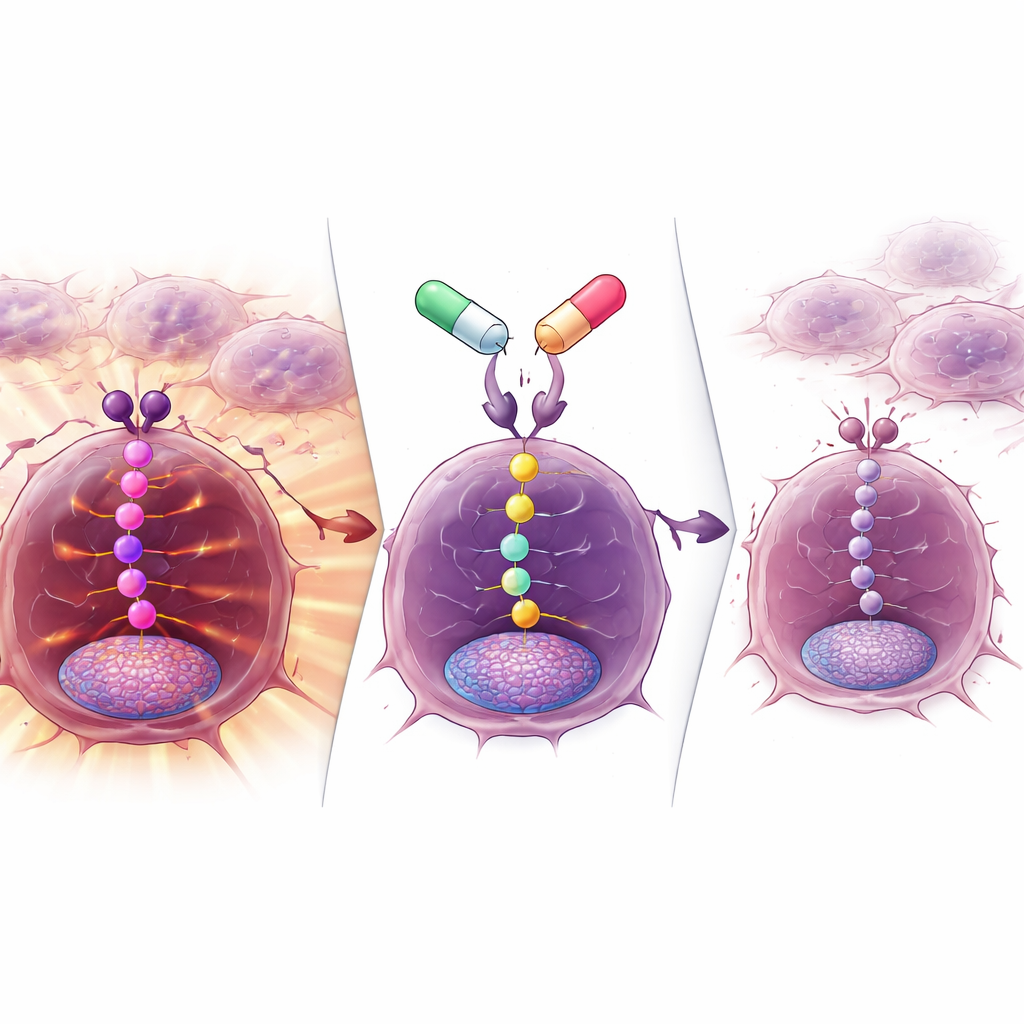
معظم سرطانات الثدي تحرّكها هرمونات مثل الإستروجين. تُسمى هذه الأورام موجَّهة مستقبلات الهرمونات وعادةً ما تفتقر إلى نسخ إضافية من بروتين يدعى HER2. يجمع العلاج القياسي لهذه الأورام المتقدمة بين أدوية حابسة للهرمونات وأدوية تُبطئ انقسام الخلايا، المعروفة بمثبطات CDK4/6. وعلى الرغم من أن هذه الإستراتيجية حسّنت البقاء على قيد الحياة، إلا أن العديد من الأورام في النهاية تتغلب عليها. تعلّم الباحثون أن أحد طرق الهروب الرئيسية يمر عبر سلسلة إشارات داخل الخلية تُعرف غالباً بمسار PI3K–AKT–PTEN، الذي يساعد الخلايا السرطانية على النمو والبقاء ومقاومة العلاج الهرموني. تستكشف الدراسة الحالية ما إذا كان حجب حلقة رئيسية في هذه السلسلة تُدعى AKT، بالتزامن مع دواء حابس للهرمونات هو فولفيسترانت، يمكن أن يستعيد السيطرة على أورام تقدمت بالفعل رغم العلاجات السابقة.
الأدوية قيد الاختبار
ركزت التجربة على أفوريسيرتيب، دواء فموي يحجب الأشكال الثلاثة الرئيسية لـAKT، وفولفيسترانت، علاج هرمي قابل للحقن يعمل على تحلل مستقبل الإستروجين داخل الخلايا السرطانية. أشارت أعمال المختبر إلى أن أفوريسيرتيب انتقائي بدرجة عالية تجاه AKT، مما قد يقلل من الآثار الجانبية مثل ارتفاع سكر الدم التي تُرى مع بعض الأدوية المشابهة. كما أنه يعمل جيداً بجرعة مرة واحدة يومياً. وبما أن أورام العديد من المرضى تحمل تغييرات جينية مرتبطة بمسار AKT (PIK3CA، AKT1، أو PTEN)، وبعضها يحمل تغييرات في جين مستقبل الإستروجين ESR1، كان الفريق مهتماً بشكل خاص بما إذا كانت هذه السمات الجينية تؤثر في فعالية الزوج الدوائي.
كيف جرت التجربة
كانت هذه الدراسة من المرحلة Ib تجربة مبكرة ذات ذراع واحد صُمِّمت أساساً لاختبار الأمان والبحث عن دلائل على الفائدة. شارك 31 بالغاً لديهم سرطان ثدي إيجابي مستقبلات الهرمونات وسالب HER2 انتشر خارج الثدي في مراكز بالصين والولايات المتحدة. تلقى تقريباً الجميع علاجاً هرمونياً سابقاً، وحوالي ثلثيهم عولجوا بمثبط CDK4/6، وحوالي ثلثهم تلقوا كيمياوياً لعلاج المرض المتقدم سابقاً. تناول المشاركون 125 ميلليغراماً من أفوريسيرتيب بالفم يومياً وتلقوا حقن فولفيسترانت بالجرعة القياسية وفق جدول شائع الاستخدام في الممارسة. استمر العلاج في دورات مدتها أربعة أسابيع حتى تفاقم السرطان أو أصبحت الآثار الجانبية غير مقبولة. قيس حجم الأورام بانتظام باستخدام قواعد التصوير القياسية، وأُجرِيت اختبارات على عينات دم أو نسيج للتحري عن تغيرات في جينات المسار وطفرات ESR1.
ما وجده الباحثون
بعد متابعة وسطية تقارب 17 شهراً، شهد 8 من بين 31 مريضاً (26 بالمئة) انكماشاً في أورامهم بما يكفي لأن يصنّف كاستجابة جزئية، وسجل 17 آخرون مرضاً مستقراً كأفضل نتيجة. إجمالاً، حقق 71 بالمئة من المرضى «فائدة إكلينيكية»، أي انكماش الورم أو مرض مستقر دام على الأقل 24 أسبوعاً. كان الوسيط الزمني قبل أن يبدأ السرطان بالنمو مجدداً 8.2 أشهر، مع بقاء نحو ثلث المرضى خالين من التقدم عند السنة. بين المرضى الذين حملت أورامهم تغييرات في PIK3CA أو AKT1 أو PTEN، كانت الاستجابات متكررة بعض الشيء مقارنة بمن لم تحمل هذه التغيرات، رغم أن المجموعتين أظهرتا فائدة. بدا أن المرضى ذوي الأورام الحاملة لطفرات ESR1، التي تكون غالباً مقاومة للعلاج الهرموني القياسي، يستجيبون على الأقل بنفس القدر كأولئك بدون هذه الطفرات، وأظهر من لديهم كل من طفرات ESR1 وتغييرات في مسار AKT معدلات استجابة وفائدة واعدة بشكل خاص.
السلامة والآثار الجانبية
تعرض جميع المشاركين لبعض الآثار الجانبية، وهو أمر متوقع عند اختبار أدوية تتداخل مع مسارات رئيسية للنمو والتمثيل الغذائي. كانت المشكلات الأكثر شيوعاً ارتفاع سكر الدم والإسهال والطفح الجلدي. والأهم أنه لم يُصب أي مريض بارتفاع سكر دم شديد، وكان أقل من واحد من كل عشرة يعاني من إسهال شديد أو اختلالات مخبرية متعلقة بالكبد. احتاج نحو ثلث المرضى إلى توقفات مؤقتة في العلاج، وطلب عدد قليل تعديلاً في جرعة أفوريسيرتيب، لكن لم يضطر أحد إلى إيقاف أي من الدوائين نهائياً بسبب الآثار الجانبية. لم تُسجَّل وفيات مرتبطة بالعلاج، وكانت المضاعفات الخطيرة نادرة، مما يشير إلى أن هذه التركيبة قابلة للإدارة لمعظم المرضى تحت مراقبة دقيقة.
ما الذي قد يعنيه هذا للمستقبل
لغير المتخصص، توحي هذه النتائج بأن مزج أفوريسيرتيب مع فولفيسترانت ساعد في كبح جماح سرطانات الثدي المتقدمة المعتمدة على الهرمونات لدى كثير من المرضى الذين استنفدوا خيارات الهرمونات القياسية، من دون التسبب بمشكلات أمان غير متوقعة. وعلى الرغم من أن التجربة كانت صغيرة وخالية من مجموعة مقارنة، فإن مستوى وديمومة السيطرة على الورم يبدوان مشابهين لما لوحظ مع دواء آخر معتمد يثبط AKT، وقد يقدم هذا الدواء مزايا في الآثار الجانبية لبعض المرضى. ستحتاج دراسات أكبر عشوائية من المرحلة III جارية الآن لتأكيد ما إذا كان أفوريسيرتيب يحسّن البقاء بالفعل وتحديد أي البروفايلات الجينية تستفيد أكثر من هذه الاستراتيجية. إذا تأكد ذلك، فقد تنضم هذه المقاربة إلى صندوق أدوات العلاجات الموجَّهة المتزايد الذي يطيل ويخصص العلاج للأشخاص الذين يعيشون مع سرطان الثدي المتقدم.
الاستشهاد: Zhang, P., Sun, T., Wang, Y. et al. Afuresertib plus fulvestrant for pretreated HR-positive, HER2-negative, advanced breast cancer: a phase Ib trial. Nat Commun 17, 2456 (2026). https://doi.org/10.1038/s41467-026-69225-2
الكلمات المفتاحية: سرطان الثدي المتقدم, إيجابي لمستقبلات الهرمونات, مثبط AKT, العلاج الموجَّه, تجربة سريرية