Clear Sky Science · ar
تخليق PI(4,5)P2 المحلي بواسطة أشكال PIPKIγ المرتبطة بالسبتين يتحكم في ارتباط centralspindlin بالـ midbody أثناء الانقسام الخلوي
كيف تُتم الخلايا الانقسام إلى قسمين
الانقسام السيتوبلازمي — القرص النهائي الذي يقسم خلية واحدة إلى خليتين — قد يبدو أمراً مفروغاً منه، لكن عندما يحدث فيه خلل يمكن أن يساهم في نشوء السرطان وأمراض أخرى. تكشف هذه الدراسة كيف تعمل مجموعة محددة من الجزيئات كـ"مشرفي بناء" عند الجسر الضيق الذي يربط خليتين حديثتي الولادة، للتأكد من أن الانقسام يكتمل بسلاسة بدلاً من أن يعود للخلف أو يتعثر.
الجسر النهائي بين الخليتين الابنتين
بعد أن تضاعفَت المادة الوراثية في الخلية وانفصلت الكروموسومات، يجب أن تنقسم الخلية فعلياً. يَضيق حلقة انقباضية من خيوط البروتين حول منتصف الخلية، مكوِّنةَ أخدوداً عميقاً يُدعى ثلم الانقسام. مع انقباض هذا الثلم إلى الداخل، تبقى الخليتان الابنتان مرتبطتين بواسطة جسر خلوي رقيق يحتوي على لب مُكثَّف يُسمى midbody. الـ midbody هي بنية صغيرة لكنها معقَّدة تتكوّن من ميكروتيوبيلات مجمّعة، وبروتينات هيكلية، ودهون إشارية، وتعمل كقيد ومركز تحكم ينسق الخطوات الأخيرة للانقسام والقطع النهائي بين الخليتين. 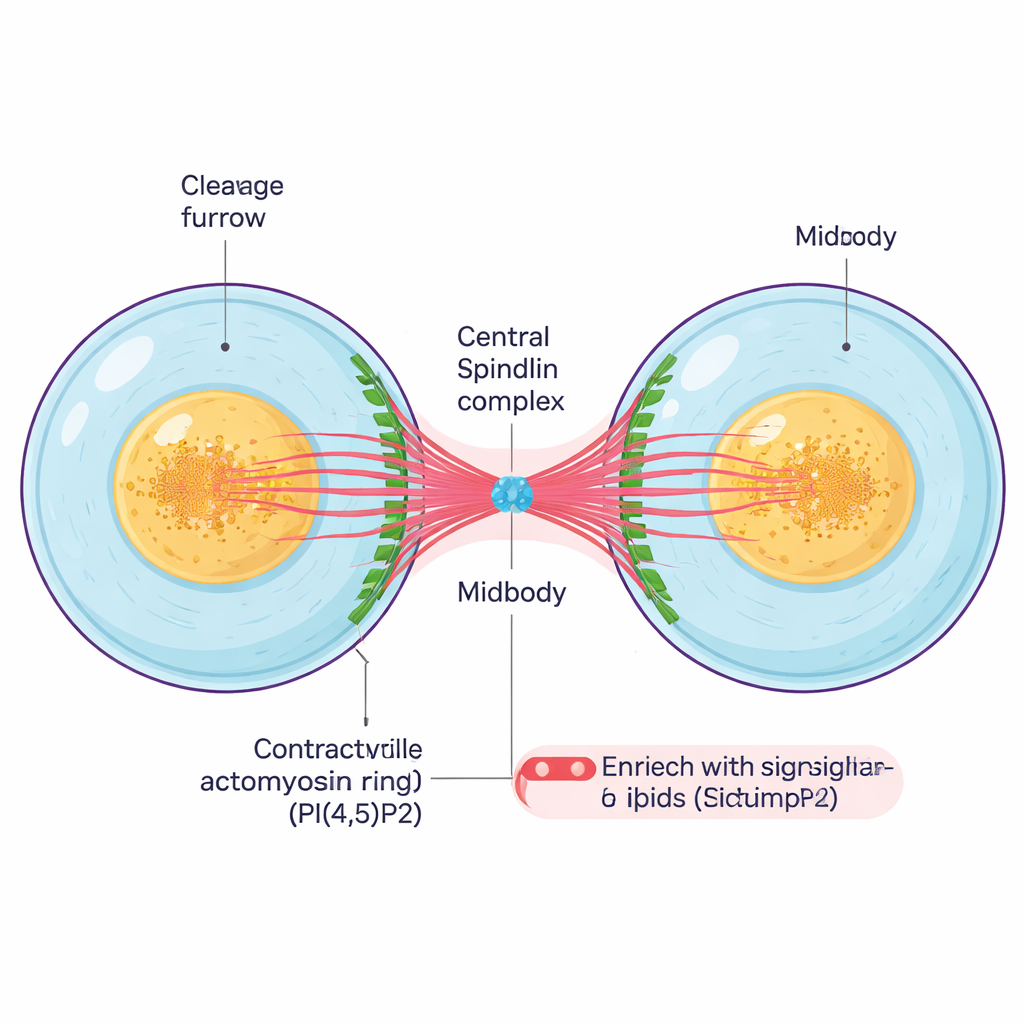
إشارة دهنية يجب أن تكون في المكان المناسب
لاعب رئيسي في هذه العملية هو جزيء دهني إشارِي في غشاء الخلية يُدعى PI(4,5)P2. تساعد هذه الشحوم في تثبيت العديد من البروتينات التي تبني وتُقلِّص الحلقة الانقباضية وتُثبّت الجسر. اللغز كان كيف تتحكّم الخلايا في مكان وزمان ظهور PI(4,5)P2، مع أنه يمكن أن ينتشر في الغشاء. ركز المؤلفون على إنزيمات تُسمى كينازات الفسفاتيد الوحيد من النوع الأول (type I PIP kinases)، والتي تصنع PI(4,5)P2، وعلى وجه الخصوص على جين واحد، PIPKIγ، الذي يوجد في عدة أشكال ترادفية (splice forms) تختلف فيما بينها بشكل طفيف. من خلال تقليل كل كيناز انتقائياً في خلايا بشرية ومراقبة الآثار باستخدام ميكروسكوب متقدم، وجدوا أن PIPKIγ له دور خاص في مراحل متأخرة من الانقسام السيتوبلازمي، عند تكوّن الجسر وmidbody، رغم أنه لا يغير بشدة مستويات PI(4,5)P2 الكلية على سطح الخلية.
الأطر السبتينية تستدعي إنزيمًا متخصصًا
اكتشف الفريق أن نسختين ترادفيتين من PIPKIγ، تُدعَيان i3 و i5، تعملان كأدوات دقيقة تُقاد إلى المكان الصحيح بواسطة بروتينات هيكلية تُعرَف بالسبتينات. تُشكّل السبتينات خيوطاً وحلقات تُساعد في تشكيل الجسر وتنظيم المكونات الأخرى. أظهرت تجارب السحب البيوكيميائية وتصوير الخلايا أن PIPKIγ-i3 وPIPKIγ-i5 يرتبطان فيزيائياً بمجمعات السبتينات ويزيّنان خيوط السبتين، في حين أن متغيرات PIPKIγ الأخرى لا تفعل ذلك. عندما شوه الباحثون حمضين أمينيين محددين في هذه الإضافات الترادفية، لم تعد الإنزيمات قادرة على ربط السبتينات. في الخلايا المنقسمة، تنتقل أشكال PIPKIγ-i3/i5 الطبيعية من نمط غشائي مشتت لتتركز عند ثلم الانقسام ثم تحدد محيط الجسر الخلوي والـ midbody بالتزامن مع السبتينات وبروتين هيكلي آخر يُدعى anillin. إزالة نسخ i3 و i5 فقط أبعدت anillin والسبتينات عن الـ midbody على طول الجسر، وفشل العديد من الخلايا في إتمام الانقسام السيتوبلازمي، مما أدى إلى خلايا متعددة النوى.
إنتاج دهون محلي يُثبّت آلية الانقسام
لاختبار ما إذا كانت هذه التأثيرات تعتمد على إنتاج PI(4,5)P2 المحلي، قاس المؤلفون PI(4,5)P2 حول الـ midbody وتلاعبوا بالإنزيمات التي تضيف أو تزيل هذه الشحوم. إنقاص PIPKIγ-i3/i5 خفّض مستوى PI(4,5)P2 عند الـ midbody، بينما حجب إنزيم يحرِّم PI(4,5)P2 أدى إلى التأثير المعاكس. والأهم من ذلك، أن إعادة إدخال شكل ترادفي طبيعي من PIPKIγ قادر على ربط السبتينات ونشطاً تحفيزياً أعادت التكتّل الملائم لـ anillin والسبتينات عند الجسر، في حين أن النماذج العديمة للنشاط الكينازي أو العاجزة عن ربط السبتينات لم تفعل ذلك. باستخدام تصوير حي وتقنية ميكروسكوب التوسيع التي تنفخ العينة فعلياً لتكشف التفاصيل الدقيقة، أظهر الفريق أنه في غياب PIPKIγ-i3/i5، لم تعد السبتينات تنتقل إلى ميكروتيوبيلات الجسر، وأصبح الجسر أقصر وأقل تجميعاً، وفشل مركب حاسم يُسمى centralspindlin في البقاء مرتبطاً بإحكام بالـ midbody. 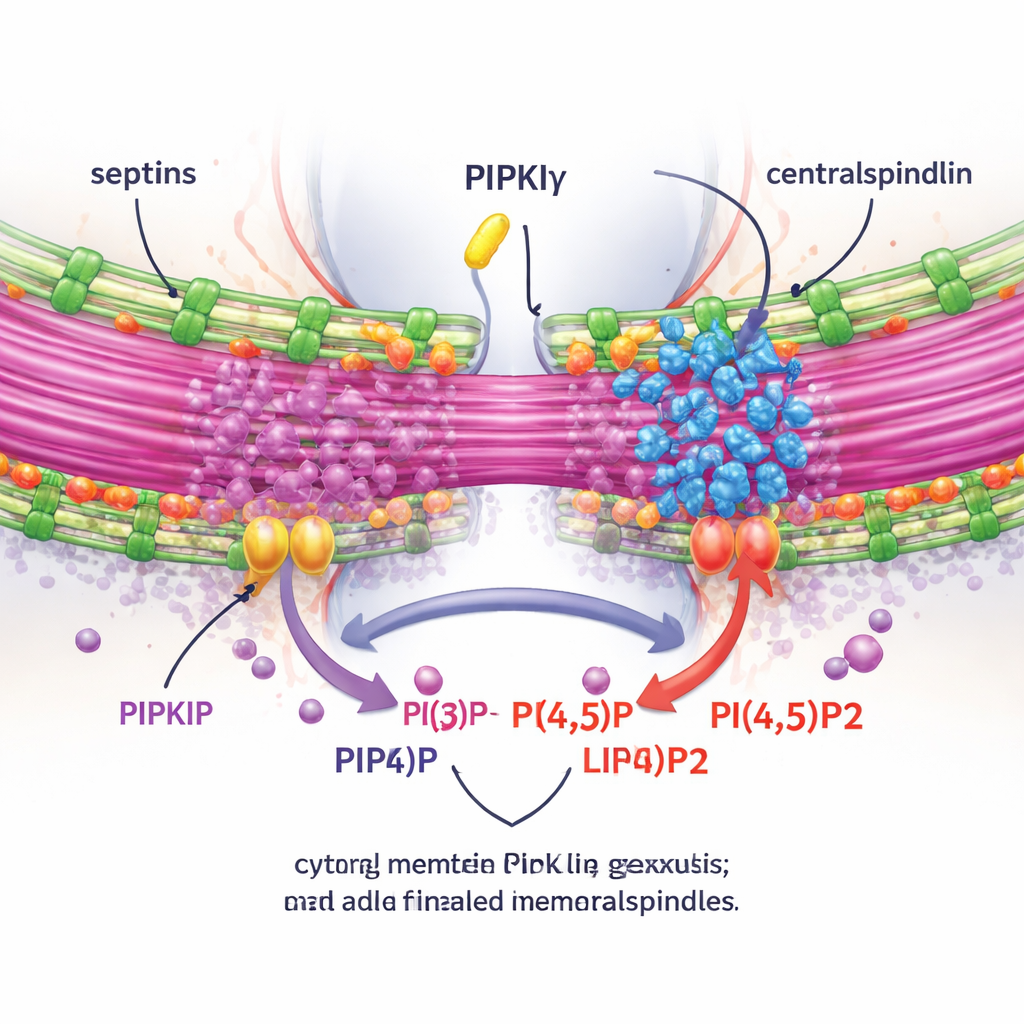
بناء نقطة تفتيش لقطع نظيف
يساعد centralspindlin في ربط ميكروتيوبيلات الـ midbody بالغشاء المحيط وينظّم مفاتيح جزيئية صغيرة تتحكم بشكل الخلية. تجد الدراسة أن centralspindlin يرتبط بكل من السبتينات وPIPKIγ، وأن فقدان أي من الشريكين يضعف تواجده عند الـ midbody بشكل مشابه. يقترح المؤلفون أن السبتينات تجذب PIPKIγ-i3/i5 إلى الثلم المنغمس، حيث تُنشئ هذه الإنزيمات رقعة مركّزة من PI(4,5)P2. هذه البقعة الدهنية المحلية، بدورها، تثبّت anillin وcentralspindlin والسبتينات قرب الـ midbody، وتعزّز تجميع واستقرار ميكروتيوبيلات الجسر، وتسمح لنضوج الجسر الخلوي حتى الحد النهائي للقطع يحدث. إذا تعرّض هذا النظام للخلل، يظهر PI(4,5)P2 في أماكن خاطئة، وتتفكك البروتينات الهيكلية، وتصبح الميكروتيوبيلات مجمّعة بشكل ضعيف، وغالباً ما يفشل الانقسام السيتوبلازمي.
لماذا يهم هذا الأمر خارج نطاق بيولوجيا الخلية الأساسية
من خلال تحديد كيف تتعاون أشكال PIPKIγ الترادفية والسبتينات لتوليد إشارة دهنية محلية عند الـ midbody، تشرح هذه الدراسة كيف تمنح الخلايا دقة مكانية لجزيء إشاري شديد الحركة. هذه الدقة ضرورية لإتمام انقسام الخلية بأمان، مما يساعد على منع فصل الكروموسومات بشكل خاطئ وزيادة أعداد الخلايا بصورة غير طبيعية التي قد تعزز تطور الأورام. تؤثر هياكل الـ midbody نفسها أيضاً في مصير الخلايا وتكاثرها بعد الانقسام، لذا فإن فهم كيفية تجميعها يفتح طرقاً جديدة لاستكشاف كيف قد تسهم الأخطاء في هذه السقالات النانومترية في السرطان وربما في التحكم بالخلايا الجذعية.
الاستشهاد: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
الكلمات المفتاحية: انقسام الخلايا, الانقسام السيتوبلازمي, دهون إشارية, السبتينات, بيولوجيا السرطان