Clear Sky Science · ar
مُثبِّط بان-RAF إكزارافينيب يستهدف BRAF من الفئة II/III في سرطان الرئة غير صغير الخلايا ويكشف مقاومة عبر ARAF‑KSR1 واستراتيجيات الجمع العلاجي
لماذا يهم هذا البحث لمرضى سرطان الرئة
معظم الناس سمعوا عن أدوية السرطان الموجَّهة التي تستهدف تغيّرات جينية محددة. لكن بالنسبة لكثير من مرضى سرطان الرئة، وخصوصاً أولئك الذين تحمل أورامهم طفرات أقل شيوعاً في جين يُدعى BRAF، الأدوية الموجَّهة الحالية لا تجدي فعلاً. تقدّم هذه الدراسة دواءً تجريبيّاً جديداً، إكزارافينيب، مصمَّماً لضرب مجموعة أوسع من الأورام المدفوعة بـBRAF وتوضح كيف تحاول الخلايا السرطانية التملّص منه — مكشوفة بذلك تراكيب علاجية تركيبية قد تُبقي هذه الأورام تحت السيطرة لفترة أطول.
أغلبية مخفية من الطفرات المُهملة
بدأ الباحثون بطرح سؤال أساسي: ما مدى شيوع أنواع طفرات BRAF المختلفة في السرطانات المتقدمة، وخاصةً في سرطان الرئة غير صغير الخلايا (NSCLC)؟ باستخدام قاعدة بيانات واسعة لفحص السائل الحيوي لأكثر من 160,000 مريض، حلّلوا شظايا DNA الورمي المتداولة في مجرى الدم. وجدوا أن طفرات BRAF في سرطان الرئة تحدث تقريباً لدى 4–5% من المرضى، وهو ما يترجم إلى آلاف الأشخاص حول العالم. والأهم أن نحو ثلثي هذه الأورام الرئوية حملت ما يُسمى طفرات BRAF من الفئتين II وIII — أنماط لا تستهدفها أدوية BRAF المعتمدة حالياً بفعالية. المرضى الذين لديهم إحدى هاتين الفئتين، وخصوصاً الفئة II، مالوا إلى فترات بقاء أقصر من أولئك الحاملين لطفرة الفئة I المعروفة، على الأرجح لأن مرضى الفئة I لديهم خيارات علاجية موجَّهة مثبتة بينما يتلقى مرضى الفئة II/III غالباً العلاج الكيميائي القياسي أو العلاج المناعي.
دواء من الجيل التالي يستهدف المسار بأكمله
يُعد BRAF جزءاً من سلسلة من البروتينات (مسار MAPK) التي تنقل إشارات النمو من سطح الخلية إلى النواة. صُممت العديد من أدوية BRAF الحالية لوقف شكل واحد طافِر فقط وقد تُحفّز بطريق الخطأ بروتينات مرتبطة في الخلايا الطبيعية. بُني إكزارافينيب بشكل مختلف: فهو مُثبِّط “بان‑RAF” مصمَّم لإيقاف عدة أعضاء من عائلة RAF (ARAF وBRAF وCRAF) في أشكالها المفردة والمزدوجة، مع تفادي معظم الإنزيمات الخلوية الأخرى. في اختبارات بيوكيميائية عبر مئات الكينازات البشرية، أعاق إكزارافينيب بقوة البروتينات الثلاثة من عائلة RAF لكن أظهر تأثيرات خارج الهدف قليلة، مما يشير إلى ملف سلامة أنقى مقارنة بمركبات بان‑RAF السابقة.
تأثيرات قوية في نماذج الأورام صعبة العلاج
اختبر الفريق إكزارافينيب في مجموعة من خطوط الخلايا ونماذج الفئران التي تحمل طفرات مختلفة في BRAF وRAS، بما في ذلك أورام مشتقة من مرضى حقيقية. في مزارع الخلايا، قلّل إكزارافينيب النمو وأوقف إشارة MAPK ليس فقط في خلايا السرطان الكلاسيكية الحاملة لطفرات BRAF V600E بل أيضاً في تلك الحاملة لطفرات الفئتين II وIII وفي العديد من خلايا RAS الطافرة التي تفتقر حالياً إلى خيارات موجَّهة جيدة. في الفئران الحاملة لأورام رئوية بهذه التغييرات، قلّص إكزارافينيب الأورام أو أبطأ نموها بشكل يعتمد على الجرعة وأظهر علاقات واضحة بين مستويات الدواء، كبح المسار، واستجابة الورم. البيانات السريرية المبكرة من مريضين مصابين بسرطان رئة متقدم طافِر BRAF — أحدهما لديه اندماج نادر في BRAF والآخر لديه طفرة موضعية من الفئة II — أظهرت استجابات جزئية وتخفيفاً ملحوظاً للأعراض، مما يدعم صلة العمل قبل السريري.
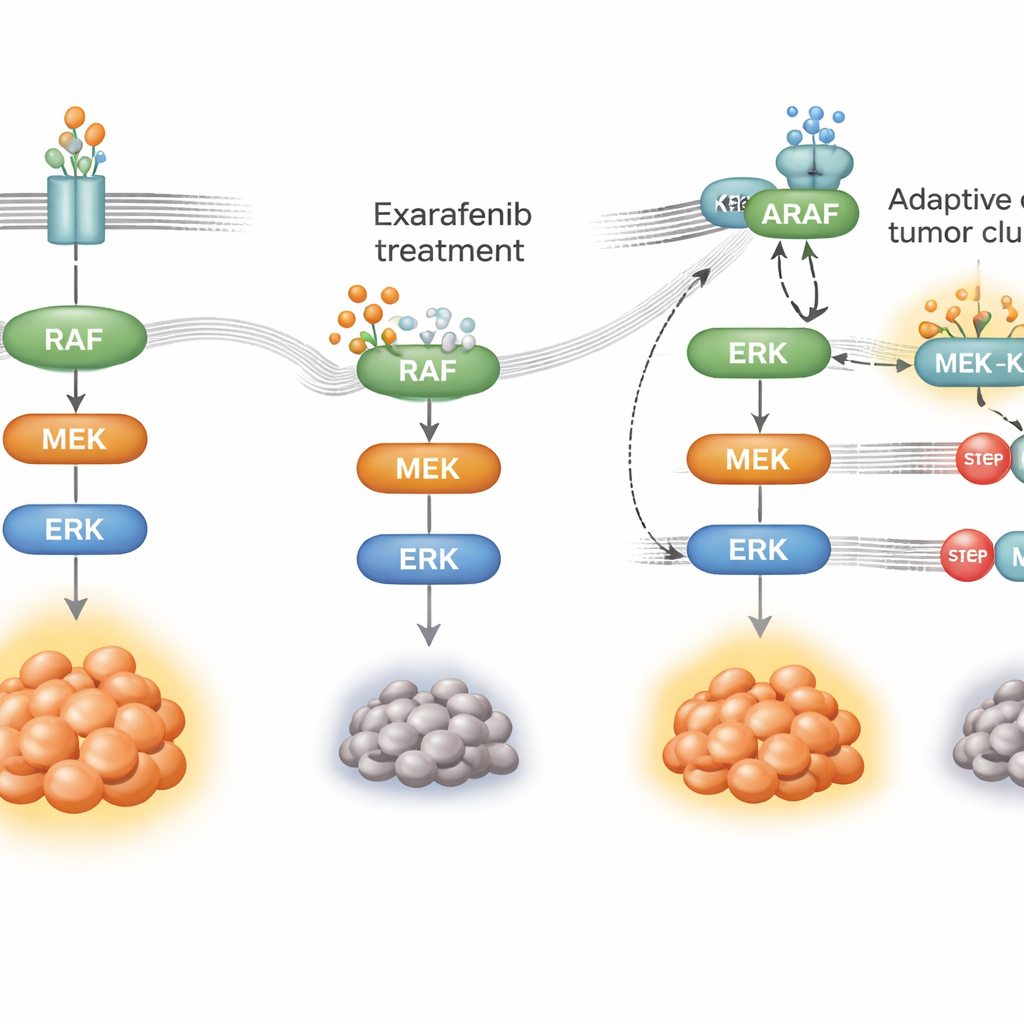
كيف تتعلّم السرطان التحايل على الدواء
لا ينجح أي علاج موجه إلى الأبد؛ تتكيّف الخلايا السرطانية. لرؤية كيف قد تقاوم الأورام إكزارافينيب، عرّض الباحثون خلايا سرطان رئة حاملة لـBRAF للدواء لعدة أشهر حتى ظهرت مجموعات مقاومة. بقيت هذه الخلايا معتمدة على نفس مسار النمو لكنها أعادت توصيل كيفية استخدامه. بدلاً من الاعتماد الأساسي على BRAF الطافر، ضَخَّمت نشاط مفتاح علوي يُدعى RAS وانتقلت إلى استخدام عضو آخر من العائلة، ARAF، مع بروتين هيكلي يُدعى KSR1. تحت ضغط الدواء، شكّلت ARAF وKSR1 مجمعات متماسكة ساعدت في إبقاء تتابع MAPK يعمل حتى مع ارتباط إكزارافينيب. عندما صمت العلماء ARAF أو KSR1 انتقائياً، أو خفّضوا نشاط RAS، عادت الخلايا المقاومة لتصبح حساسة مجدداً لإكزارافينيب وانهيارت إشارات البقاء.
استراتيجيات تركيبية لسبق المقاومة
مسلحين بهذه الخريطة الميكانيكية، بحث الفريق عن أدوية شريكة يمكن أن تُغلق المسار عند نقاط اختناق مشتركة بين الطريق الأصلي وطرق التفاف المقاومة. وجدوا أن إقران إكزارافينيب بأدوية تُثبّط MEK أو ERK — خطوات نزولية رئيسية في تتابع MAPK — أنتج تآزرًا قويًا عبر كثير من نماذج الخلايا والفئران، بما في ذلك الأورام التي كانت بطبيعتها أقل حساسية أو اكتسبت مقاومة. أبقت هذه التركيبات المسار مغلقًا لفترة أطول، وأطلقت المزيد من موت الخلايا، وغالباً ما أدت في الحيوانات إلى نتائج تعادل أو تفوق جرعات أعلى من إكزارافينيب وحده، دون سمّية إضافية واضحة. كما عززت العوامل التي تستهدف RAS مباشرة تأثير إكزارافينيب في نماذج كان فيها RAS سبباً واضحاً للمقاومة، مما يشير إلى تكتيك سريري واعد آخر.
ماذا يعني هذا للمرضى
بالنسبة للأشخاص المصابين بسرطان الرئة غير صغير الخلايا الحامل لطفرات BRAF من الفئة II أو III — أو لاندماجات BRAF المعقدة وتغايرات مشتركة في RAS — لا توجد حالياً علاجات موجَّهة معتمدة، وتبقى النتائج دون تلك الخاصة بالمرضى ذوي التغييرات الأكثر شيوعاً. تقدّم هذه الدراسة حجة علمية قوية بأن إكزارافينيب قد يساعد في سد هذه الفجوة عبر كبح إشارات RAF على نطاق واسع. كما تشرح كيف قد تتكيّف الأورام عبر التفاف ARAF‑KSR1 وتُظهر أن ضرب المسار على مستويات متعددة، وخصوصاً من خلال الجمع بين مُثبِّطات RAF وMEK أو إضافة مثبطات RAS، يمكن أن يوفر تحكماً أعمق وأكثر دواماً في الورم. معاً، ترسم هذه الرؤى طريقاً نحو تجارب سريرية تهدف إلى تقديم علاجات موجَّهة تركيبيّة مُفصَّلة لشريحة واسعة كانت مُهمَلة سابقاً من مرضى سرطان الرئة.
الاستشهاد: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
الكلمات المفتاحية: سرطان الرئة الطافِر BRAF, مُثبِّط بان‑RAF, إشارة MAPK, مقاومة للأدوية, توليفات العلاج الموجَّه