Clear Sky Science · ar
تغيّرات موروثة في تلامسات الكروماتين مرتبطة بالحساسية عبر الأجيال للاختلال الأيضي والبدانة الناجمين عن النظام الغذائي
عندما يلتقي نظام أجدادنا الغذائي بخصر العصر الحديث
لماذا يزداد وزن بعض الأشخاص ويطورون مشاكل في سكر الدم بسهولة أكثر من غيرهم، حتى عندما تبدو أنماط حياتهم صحية؟ تستكشف هذه الدراسة احتمالاً مقلقاً: أن التعرض لبعض المواد الكيميائية الصناعية أثناء الحمل يمكن أن «يهيّئ» أحفاداً بعدة أجيال للاستجابة بشكل سلبي للأنظمة الغذائية الغنية. باستخدام نماذج الفئران، يكشف الباحثون عن آلية يمكن أن تُنقل عبر الأجيال دون تغيير أحرف DNA، عبر إعادة تشكيل كيفية طيّ الجينوم داخل الخلايا.
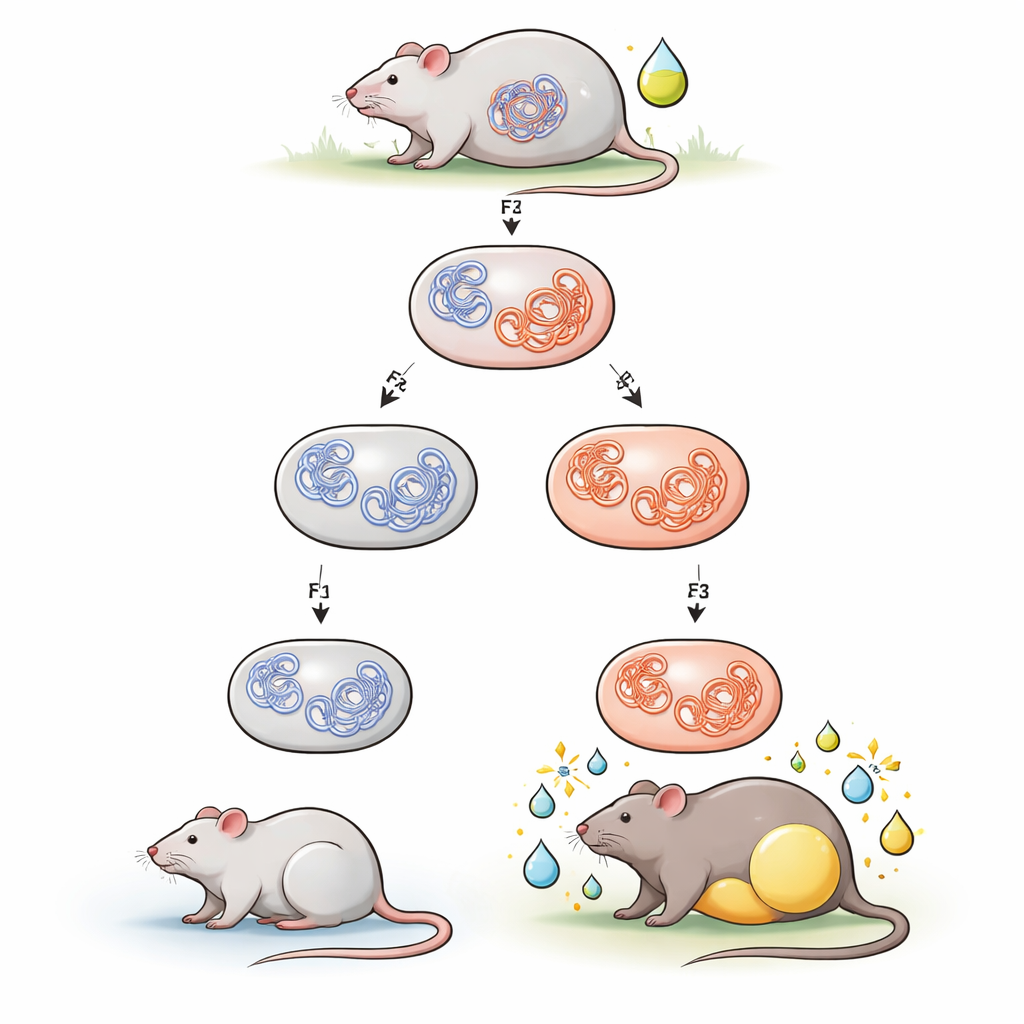
مادة كيميائية تترك ظلًا طويل الأمد
ركز الفريق على الترايبوتيلتين، مادة كانت شائعة سابقاً في مكافحات التلوث وقطاعات صناعية، ومعروفة كمسبب للسمنة لأنها تعزز تخزين الدهون. أعطي للأمهات الحوامل جرعات منخفضة من الترايبوتيلتين في ماء الشرب أثناء الحمل. تعرضت ذراريهن (الجيل الأول) للمادة داخل الرحم، وتعرضت الأحفاد (الجيل الثاني) عندما كانت الخلايا الجرثومية تتطور داخل تلك الذراري، في حين أن الأحفاد الثلاثة (الجيل الثالث) لم يتعرضوا مباشرة. عندما نُقلت فئران الأجيال الشابة من غذاء عادي إلى غذاء أعلى دهوناً، زاد ذوو الذكور من نسل الفئران التي تعرضت سابقاً للترايبوتيلتين في كتلة الجسم والدهون مقارنةً بالمجموعات الضابطة غير المعرضة. أما الإناث فلم تظهر تغيراً ملحوظاً. هذه الميلية المحددة للذكور نحو السمنة المحفزة بالغذاء تتوافق مع أعمال سابقة لنفس الفريق.
طيّ الجينوم كذاكرة خفية
لفهم كيف يمكن أن تُورث هذه الصفة دون طفرات في DNA، فحص الباحثون الخلايا الجرثومية البدائية من الأجنة في الأجيال الثلاثة الأولى. هذه خلايا غير ناضجة تتطور لاحقاً إلى الحيوانات المنوية والبويضات. باستخدام تقنية ترسم أي أجزاء من DNA تلامس بعضها في الفراغ ثلاثي الأبعاد، سعوا إلى العثور على تغيّرات دائمة في طيّ الكروموسومات. وجدوا أن نمط التلامسات كان مستقراً عموماً. ومع ذلك، في خلايا الجراثيم الذكرية، برزت منطقة صغيرة على الكروموسوم 19: ظهرت مجموعة من التلامسات الجديدة والمقوية واستمرت من الأجنة المتعرضة مباشرةً عبر جيلين لم يتعرضا. تحتوي هذه المنطقة على جين Ide، الذي يشفر إنزيم تحلل الأنسولين، وهو بروتين رئيسي يساعد عادة في إزالة الأنسولين من مجرى الدم.
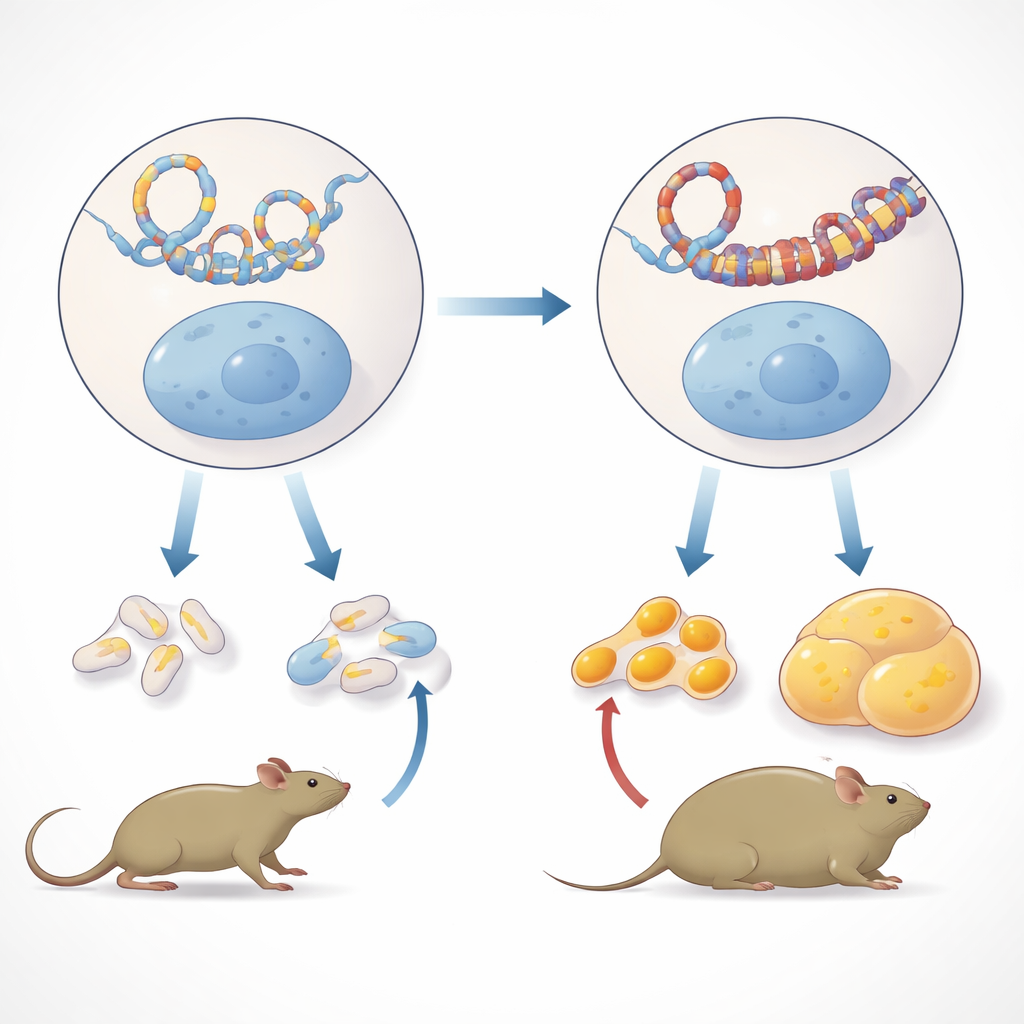
جين واحد في قلب التحول الأيضي
سأل الفريق بعد ذلك ما إذا كانت هذه التلامسات المعدلة في DNA لها تأثيرات في الأنسجة الجسدية العادية. في كبِد أحفاد الجيل الثالث البالغين من الفئران المتعرضة سابقاً، لاحظوا ارتباطاً أقوى لبروتين منظم للجينوم يُدعى CTCF عند عدة مواقع داخل منطقة Ide، مما يتوافق مع تكوُّن حلقة كروماتينية جديدة. في الوقت نفسه، انخفض نشاط Ide في كبِد الذكور، بينما أصبحت الجينات المجاورة Hhex وKif11 أكثر نشاطاً. لم يلاحظ هذا النمط في كبِد الإناث أو في أنسجة ذكور أخرى مثل العضلات أو مخازن الدهون أو الدماغ أو الطحال، مما يبرِز طبيعته المرتبطة بالنوع والنسيج. والأهم من ذلك، استبعد المؤلفون تفسيراً بسيطاً يقوم على تكرار هيكلي للجزء من الكروموسوم، موضحين أن عدد نسخ منطقة Ide لم يختلف بين السلالات المعرضة والضابطة.
من تراجع إزالة الأنسولين إلى السمنة
بما أن إنزيم تحلل الأنسولين يساعد في إزالة الأنسولين من الدورة الدموية، فالتراجع في نشاط Ide يجب أن يترك كمية أكبر من الأنسولين في الدم. وهذا ما رصده الباحثون بالضبط. حتى قبل تناول الغذاء الأعلى دهوناً، كان لدى الذكور من نسل الأمهات المعرضات للترايبوتيلتين مستويات أنسولين مرتفعة ودرجات أعلى على مؤشر قياسي لمقاومة الأنسولين، رغم أن سكر الصيام كان طبيعياً. بعد أسابيع على النظام الغذائي الأغنى، طوّروا كلّاً من ارتفاع سكر الدم والأنسولين، إلى جانب مخازن دهنية أكبر ومستويات مرتفعة من اللبتين، الهرمون المرتبط بكمية الدهون في الجسم. ارتفعت مستويات الببتيد-C، الذي يعكس كمية الأنسولين المنتجة، بشكل مشابه في الحيوانات المعرضة والضابطة. الفرق الحاسم كان نسبة الببتيد-C إلى الأنسولين، التي أشارت إلى تراجع في تفكك الأنسولين بدلاً من إفراز زائد — وهو ما يتوافق مع الانخفاض الملحوظ في Ide الكبدي.
ما الذي يعنيه هذا للوراثة والصحة
توضّح النتائج مجتمعة سلسلة من الأحداث: التعرض الأسري لمادة مسببة للسمنة يعيد بشكل طفيف تشكيل طيّ منطقة معينة من الجينوم في خلايا الجراثيم الذكرية؛ يُعاد إنشاء هذا البنية ثلاثية الأبعاد الجديدة في أباء الذكور اللاحقين في كبِدهم، ما يخفّض نشاط جين واحد ينظف الأنسولين؛ ونتيجة لذلك، تحمل هذه الحيوانات مستويات أنسولين مرتفعة مزمنة وتكون مهيّأة لاكتساب الدهون وتطوير اضطرابات سكر الدم عند تعرّضها لنظام غذائي عالي الدهون. للقراء غير المتخصصين، الرسالة الأساسية هي أن ما يعيشه الأجداد في بيئتهم يمكن أن يترك «ذاكرة» مادية في كيفية تغليف DNA، ليس بتغيير الشفرة الجينية بل بتغيير شكلها. هذه الذاكرة قد تؤثر بهدوء في كيفية استجابة الأجيال اللاحقة للأنظمة الغذائية الحديثة، مما يبرز أهمية الحد من التعرضات الضارة قبل أن تظهر مشاكل صحية.
الاستشهاد: Chang, R.C., Egusquiza, R.J., Amato, A.A. et al. Heritable changes in chromatin contacts associated with transgenerational susceptibility to diet-induced insulin dysregulation and obesity. Nat Commun 17, 2662 (2026). https://doi.org/10.1038/s41467-026-69214-5
الكلمات المفتاحية: علم الوراثة اللاجيني عبر الأجيال, مسببات السمنة, مقاومة الأنسولين, بنية الكروماتين, التعرض البيئي