Clear Sky Science · ar
هندسة إنزيم السيتوكروم P450 ليعمل كبيروكسجيناز لأكسدة انتقائية للستيرويدات
صنع أدوية من جزيئات صعبة الضبط
تُعد أدوية الستيرويد — من حبوب مضادة للالتهابات إلى علاج الهرمونات — من بين الأدوية الأكثر استخدامًا في العالم. ومع ذلك، فإن ضبط هذه الجزيئات بدقة، عن طريق إضافة ذرة أكسجين واحدة في الموضع الصحيح تمامًا، أمر شديد الصعوبة باستخدام الكيمياء التقليدية. تُظهر هذه الدراسة كيف أعاد العلماء تصميم إنزيم طبيعي ليتمكن من «تلميع» جزيئات الستيرويد بدقة باستخدام بيروكسيد الهيدروجين البسيط، مما قد يفتح طرقًا أكثر خضرة وأرخص لصنع أدوية هامة.
لماذا من الصعب تخصيص الستيرويدات
تتكون الستيرويدات من تراص مدمج لحلقات كربون، مع العديد من روابط الكربون-الهيدروجين المتشابهة تقريبًا. تكافح الطرق الكيميائية التقليدية لاستهداف رابطة واحدة فقط دون التأثير على الأخريات، وغالبًا ما تتطلب مواد فعّالة قاسية ودرجات حرارة مرتفعة وخطوات حماية متعددة تولّد نفايات. ومع ذلك، يمكن لتغييرات صغيرة — مثل إضافة مجموعة هيدروكسيل واحدة (–OH) في موقع محدد — أن تغير بشكل كبير سلوك الستيرويد في الجسم. تُعد إنزيمات عائلة السيتوكروم P450 متخصصة طبيعية في هذا النوع من تنشيط روابط C–H بدقة، لكن في شكلها الطبيعي عادةً ما تحتاج إلى جزيئات مساعدة مكلفة وآليات للتعامل مع الأكسجين، مما يقيّد استخدامها المباشر في التصنيع.
اكتشاف إنزيم واعد كنقطة انطلاق
باستخدام تنقيب الجينوم، حدّد الباحثون إنزيم P450 مستقل ذاتيًا يُسمى P450stri من بكتيريا تربة. على عكس إنزيم العمل الشائع P450BM3، الذي يفضل الأحماض الدهنية الصغيرة، يقبل P450stri طبيعيًا جزيئات ستيرويد ضخمة مثل التستوستيرون. تحت ظروفه الطبيعية، وبالاعتماد على العامل المساعد الخلوي NADH، يضيف P450stri مجموعات هيدروكسيل في ثلاث مواضع على التستوستيرون، مما ينتج خليطًا من المنتجات. جعلت هذه القدرة الفطرية على التعرف على الستيرويدات P450stri «هيكل انطلاق» جذابًا لهندسة محفز أكثر انتقائية وصديقًا للصناعة.
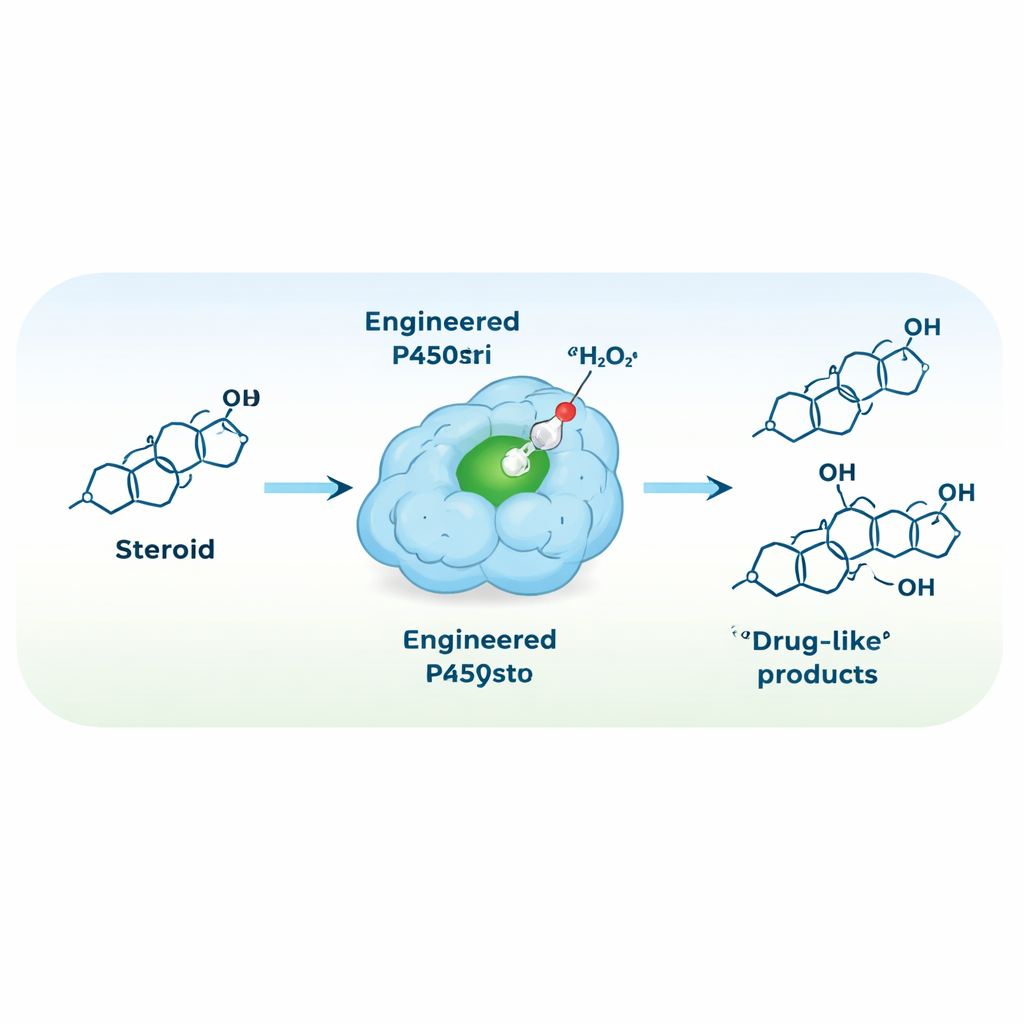
إعادة توصيل الإنزيم ليعمل على بيروكسيد الهيدروجين
لتبسيط إعداد التفاعل، سعى الفريق إلى تحويل P450stri إلى بيروكسجيناز — إنزيم يستخدم بيروكسيد الهيدروجين مباشرة كمؤكسد، مُلغيًا الحاجة إلى العوامل المساعدة والبروتينات المساعدة المكلفة. أدت طفرة استراتيجية واحدة، استبدال فينيل ألانين جامد فوق المركز الهيمي بألانين أصغر، إلى إنشاء نسخة تدعى M1. افتتحت هذه التغييرات مساحة حول مركز الحديد التفاعلي وجعلت الإنزيم، بشكل مفاجئ، أكثر تحملاً لمستويات مرتفعة من بيروكسيد الهيدروجين وأكثر انتقائية بكثير. في الوضع الجديد المدفوع بالبيروكسيد، حولت M1 التستوستيرون بشكل رئيسي إلى منتج واحد، مُهدرج في الموقع 15β، بانتقائية نحو 94% — ارتفاعًا من 35% في الإنزيم الأصلي.
نموذج «الزجاجة المستديرة» لتصميم إنزيم أذكى
لدفع الأداء إلى الأمام، قدّم المؤلفون مفهوم تصميم أسموه نموذج «الزجاجة المستديرة». يعاملون الموقع الفعال حيث تحدث الكيمياء كأساس مستدير والأنفاق الضيقة الموصلة كمُعنق وغطاء. يحدد القاعدة أي موقع على الستيرويد سيتعرض للتعديل، بينما يتحكم العنق في سهولة وصول الستيرويد وبيروكسيد الهيدروجين إلى المركز التفاعلي. مسترشدين بمحاكاة حاسوبية وبرامج رسم خرائط الأنفاق، عدّلوا منهجيًا مجموعة صغيرة من الأحماض الأمينية المبطنّة لهذه الأنفاق، مضبطين حجمها وخصائصها الكارهة للماء. أسفرت هذه الاستراتيجية ثنائية البُعد عن نسخة مميزة، M4، حافظت على انتقائية عالية لموضع 15β بينما زادت معدل التفاعل بشكل كبير وتحمّلت تراكيز بيروكسيد الهيدروجين حتى مئات الميلي مولار.
من منضدة المختبر إلى تحسينات ستيرويدية قابلة للتوسع
اختُبر الإنزيم المهندَس M4 بعد ذلك في تفاعلات على نطاق أكبر مع التستوستيرون وستيرويد ذي صلة يُستخدم في سياقات تعزيز الأداء. في خلطات مائية بسيطة عند درجة حرارة الغرفة، ومدفوعة فقط ببيروكسيد الهيدروجين، حوّلت M4 أكثر من 90% من المادة الأولية ووفّرت منتجات مهدرجة في الموقع 15β بعزلات بنسب غلة تقارب 75–80%. هذه الشروط أكثر اعتدالًا ونظافة من الطرق الكيميائية النموذجية. أخيرًا، أظهر الفريق أنه بنقل الطفرات الرئيسية إلى عدة إنزيمات P450 ذات صلة في نفس الفرع التطوري، استطاعوا تحويلها بشكل موثوق إلى بيروكسجينازات انتقائية وفعالة بالمثل، مما يبرز عمومية قواعد تصميمهم.
ماذا يعني هذا للأدوية المستقبلية
بالنسبة للقارئ غير المتخصص، الخلاصة أن الباحثين علّموا إنزيمًا طبيعيًا أن يتصرف كـ«مصنع صغير» شديد الدقة يعمل بالبيروكسيد لتعديل أدوية الستيرويد. من خلال الجمع بين نموذج مفهومي بسيط وطفرات مستهدفة، أنشأوا إنزيمًا قادرًا على إضافة مجموعة OH في الموضع المناسب تمامًا، تحت ظروف لطيفة وقابلة للتوسع، ثم نشروا هذه الاستراتيجية على بروتينات ذات صلة. قد يُبسِط هذا النهج إنتاج الستيرويدات الحالية، ويفتح طرقًا لمرشحين دوائيين جدد، ويعمل كخارطة طريق لهندسة إنزيمات أخرى تنشط روابط C–H العنيدة في جزيئات معقدة بشكلٍ نظيف.
الاستشهاد: Tang, T., Wang, R. & Chen, Y. Engineering a cytochrome P450 enzyme as a peroxygenase for selective hydroxylation of steroids. Nat Commun 17, 1996 (2026). https://doi.org/10.1038/s41467-026-69211-8
الكلمات المفتاحية: التحفيز الحيوي للستيرويدات, هندسة السيتوكروم P450, بيروكسجيناز, تحفيز بواسطة بيروكسيد الهيدروجين, هيدروكسيل انتقائي