Clear Sky Science · ar
الهندسة الأيضية لتوليف الدوكسوروبيسين عبر تحسين شركاء المختزل P450 والتحليل البنيوي لـ DoxA
لماذا تهم قصة أصل دواء السرطان
يُعدّ الدوكسوروبيسين أحد الأدوية الأساسية في العلاج الكيميائي الحديث، ويُستخدم لعلاج أنواع متعددة من السرطان من اللوكيميا إلى أورام الثدي. ومع ذلك، وعلى الرغم من عقود من الاستخدام، فإن طريقة تصنيع هذا الدواء تبدو ملتوية بشكل مفاجئ: عادةً ما تبني الصناعة الدواء من مركب ذي صلة بدلاً من السماح للميكروب المنتج الأصلي بإكمال المهمة. تكشف هذه الدراسة سبب معاناة البكتيريا المنتجة من إتمام الخطوات الكيميائية النهائية وتُظهر كيف أن إعادة هندسة آليتها الداخلية يمكن أن تزيد بشكل كبير من إنتاج الدوكسوروبيسين الكامل، مما يفتح الباب أمام إمدادات أكثر موثوقية وربما أقل تكلفة.
من بكتيريا التربة إلى دواء ينقذ الحياة
ينتمي الدوكسوروبيسين إلى مجموعة الأنثراسيكلينات، وهي عائلة من الجزيئات الطبيعية التي تُبنى بواسطة بكتيريا التربة من جنس Streptomyces. تشترك هذه المركبات في إطار كربوني مسطح وصلب ينزلق بين قواعد الـDNA، بالإضافة إلى وحدة سكرية تستقر في شقوق الـDNA. معاً، تعطل هذه المزايا آلية معالجة الـDNA في الخلية وتؤدي في نهاية المطاف إلى موت الخلية — وهي خاصية مفيدة ضد الخلايا السرطانية سريعة النمو. المنتج الكلاسيكي، Streptomyces peucetius، يصنع بطبيعته في الغالب دواءً سابقاً يُسمى داونوروبسين، وفقط كمية متواضعة من الدوكسوروبيسين الأكثر فعالية، الذي يختلف بوجود مجموعة أكسجين إضافية واحدة فقط. ذلك التغيير البنيوي الصغير يحسّن النشاط بشكل كبير لكنه يصعب على الميكروب تحقيقه بكفاءة.
إيجاد التوصيل الكهربائي الصحيح داخل الخلية
الإنزيم الحاسم الذي يقوم بالخطوات الثلاث الأخيرة من الأكسدة على هيكل الدواء يُدعى DoxA، وهو عضو في عائلة السيكروكروم P450. مثل مصنع كيميائي مصغر، يحتاج DoxA لتدفق ثابت من الإلكترونات لتنشيط الأكسجين وتركيب ذرات أكسجين جديدة على جزيء الدواء. داخل البكتيريا، تُزود تلك الإلكترونات عبر سلسلة من البروتينات المساعدة المعروفة بشركاء الاختزال (redox partners). يحتوي جينوم S. peucetius على عدة مرشحين، مما يجعل من غير الواضح أيهم يتزاوج فعلياً مع DoxA. بمقارنة نشاط الجينات والاستقلاب في سلالة طبيعية، وسلالة غنية بالداونوروبسين، وسلالة غنية بالدوكسوروبيسين، حدّد الباحثون فيردوكسين واحد (Fdx4) وفيردوكسين مختزل واحد (FdR3) كشركاء طبيعيين. إعادة تجميع هذا الثالوث في تفاعلات أنبوبية أكدت أن DoxA يعمل بأفضل صورة عند توصيلة بسلسلة نقل الإلكترون هذه على وجه التحديد، مثل مطابقة المحول الكهربائي المناسب لجهاز ما.
إزالة بطء الإنزيم الذاتي التسبب
حتى مع التوصيل الكهربائي الصحيح، يميل DoxA إلى التوقف عند الخطوة النهائية التي تحول الداونوروبسين إلى دوكسوروبيسين. أشارت أعمال سابقة إلى أن المنتج نفسه قد يعرقل الإنزيم. توجه الفريق إلى جين مجاور، dnrV، الذي كان دورُه غامضاً. أظهرت الاختبارات الكيميائية الحيوية أن بروتين DnrV يرتبط بقوة بمجموعة من جزيئات الأنثراسيكلين، بما في ذلك الدوكسوروبيسين، دون أن يُغيرها كيميائياً. إضافة DnrV إلى تفاعلات DoxA حسّن بشكل كبير تدفق التفاعلات، مما سمح بالتحويل الكامل للمقدمات إلى الدواء النهائي مع تجنب تفاعلات جانبية مدمرة. عملياً، يعمل DnrV كإسفنجة داخلية تمتص الدوكسوروبيسين المتشكل حديثاً، مانعاً إياه من انسداد الإنزيم أو إتلاف الـDNA داخل الخلية المنتجة.
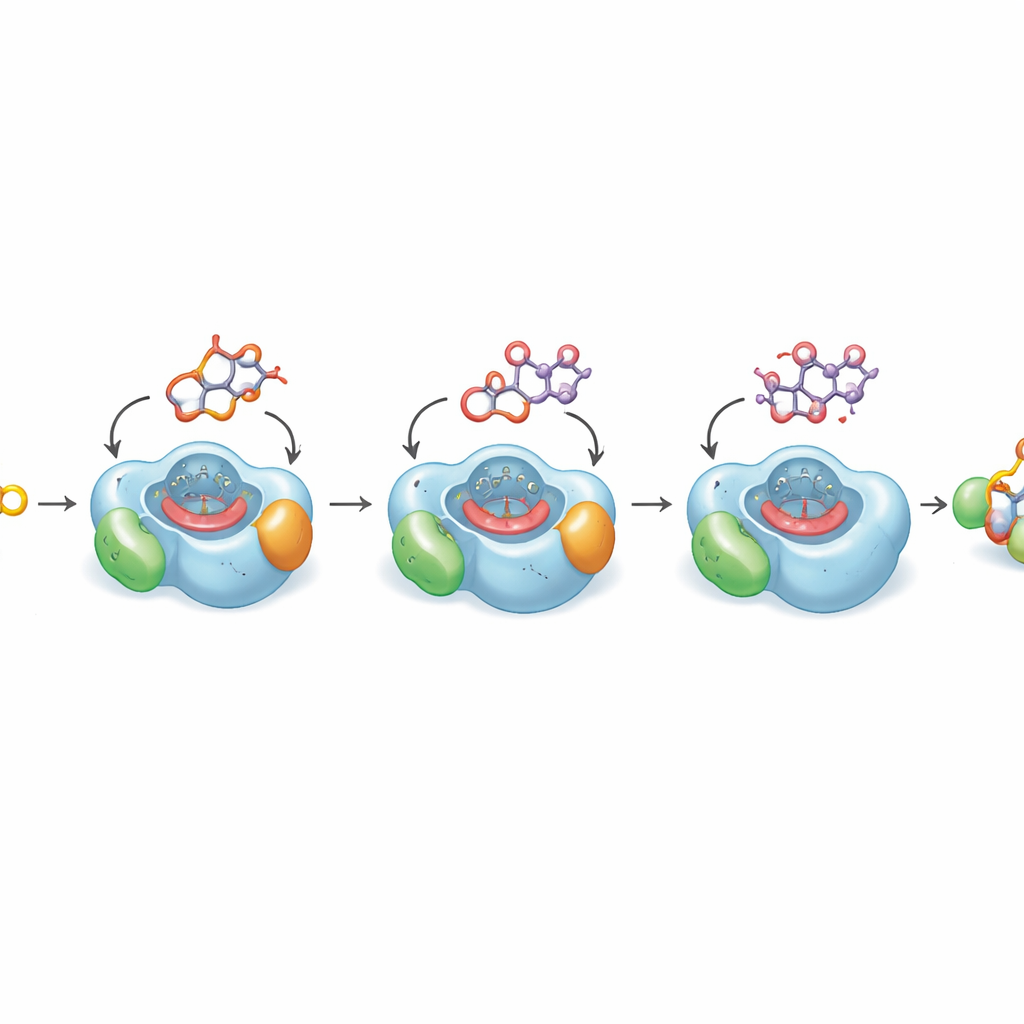
رؤية سبب بطء الخطوة الأخيرة
لفهم سبب بطء أكسدة الخطوة الأخيرة جوهرياً، حلّل المؤلفون بنيات بلورية عالية الدقة لـ DoxA مرتبطة بثلاثة وسطاء متتابعين. تكشف هذه البُنى كيف يستقر لب الدواء المسطح وسكره المرفق داخل جيب محكم فوق مجموعة الهيم في الإنزيم، وهي المركز المعدني التفاعلي الذي يؤدي الأكسدة. في الخطوات المبكرة، يكون ذرة الكربون التي يجب تعديلها قريبة من الهيم في وضع مثالي للتفاعل. لكن في الركيزة الأخيرة، الداونوروبسين، ينحني الجزء من الجزيء الذي يحتاج إلى هيدروكسلة مبتعداً عن الهيم إلى جيب زيتي صغير، وهي ترتيب تُظهر حسابات كمومية أنه مفضل طاقياً. تؤكد المحاكاة الحاسوبية على مدى ميكروثانية أن الجزيء نادراً ما يتخذ الوضع المنتج لتلك الإدخال الأكسجيني الأخير. يفسّر هذا الانحياز البنيوي سبب عدم كفاءة التحويل إلى دوكسوروبيسين بطبيعته.
بناء سلالة أفضل لصنع الدوكسوروبيسين
مسلحين بهذه الرؤى، أعاد الباحثون تصميم البكتيريا بعقلانية بدلاً من الاعتماد على الطفرات العشوائية. أدخلوا جين إصلاح الحمض النووي لتثبيت الإنتاج، ثم ركّبوا نسخاً إضافية من doxA، وشركاء الاختزال الأمثلين fdx4 وfdr3، والبروتين الرابط المفيد dnrV تحت محركات مُختارة بعناية لموازنة مستوياتها. ضبطوا أيضاً ظروف الزراعة واستخدموا راتنجات خاصة لامتصاص الوسطاء السامة واللصقة. في فلاسكات المختبر ومفاعل حيوي سعة 20 لتراً، أنتجت أفضل سلالة مهندسة 336 ملليغراماً من الدوكسوروبيسين لكل لتر من الوسط بمعدل 81:19 للدوكسوروبيسين مقابل الداونوروبسين — زيادة تقارب 180% عن السلالة الأصلية ومزيج منتج أنقى بكثير.
ما يعنيه هذا لإمداد أدوية السرطان المستقبلية
بفكّ كل من نظام الدعم الإلكتروني وبنية ثلاثية الأبعاد لإنزيم رئيسي، يشرح هذا العمل سبب أداء الميكروب الطبي الحيوي بشكل دون المستوى في صنع أكثر الأنثراسيكلينات قيمة لدينا. مطابقة DoxA مع شركاء الاختزال الطبيعيين، وإضافة بروتين مساعد لالتقاط الدواء، وإعادة توازن تعبير الجينات حوّل منتجاً متردداً إلى منتج قوي. ومع أن مزيداً من ضبط الإنزيم قد يسرّع الخطوة الكيميائية النهائية أكثر، فإن الدراسة تقرّب بالفعل تصنيع الدوكسوروبيسين بالكامل بيولوجياً من الواقع الصناعي. بالنسبة للمرضى وأنظمة الرعاية الصحية، قد تترجم مثل هذه التقدّمات إلى وصول أكثر أماناً وقابلة للتوسع وموفراً للتكلفة لدواء علاج كيميائي أساسي.
الاستشهاد: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
الكلمات المفتاحية: إنتاج الدوكسوروبيسين, توليف الأنثراسيكلين, هندسة الإنزيمات, تصنيع الأدوية الميكروبي, سيكروكروم P450