Clear Sky Science · ar
تنشيط كيناز بروتين شاذ يحفز إفراز الجلوكوز المعوي في داء السكري
تحويل الأمعاء إلى صمام للسكر
يعيش الأشخاص المصابون بالسكري مع فائض من السكر في الدم. تجرى عمليات جراحية لسد الشهية مثل تحويل المسار المعدي (جراحة المجازة المعدية) غالباً ما تعيد مستويات السكر في الدم إلى وضعها الطبيعي بسرعة مدهشة، حتى قبل فقدان الكثير من الوزن، لكن آلية حدوث ذلك كانت لغزاً. تكشف هذه الدراسة عن "صمام سكر" قائم على الأمعاء—آلية تمكّن الأمعاء من سحب السكر من الدم وطرد جزء منه إلى التجويف المعوي—مما يشير إلى هدف دوائي جديد قد يحاكي فوائد الجراحة دون الحاجة إلى عملية.
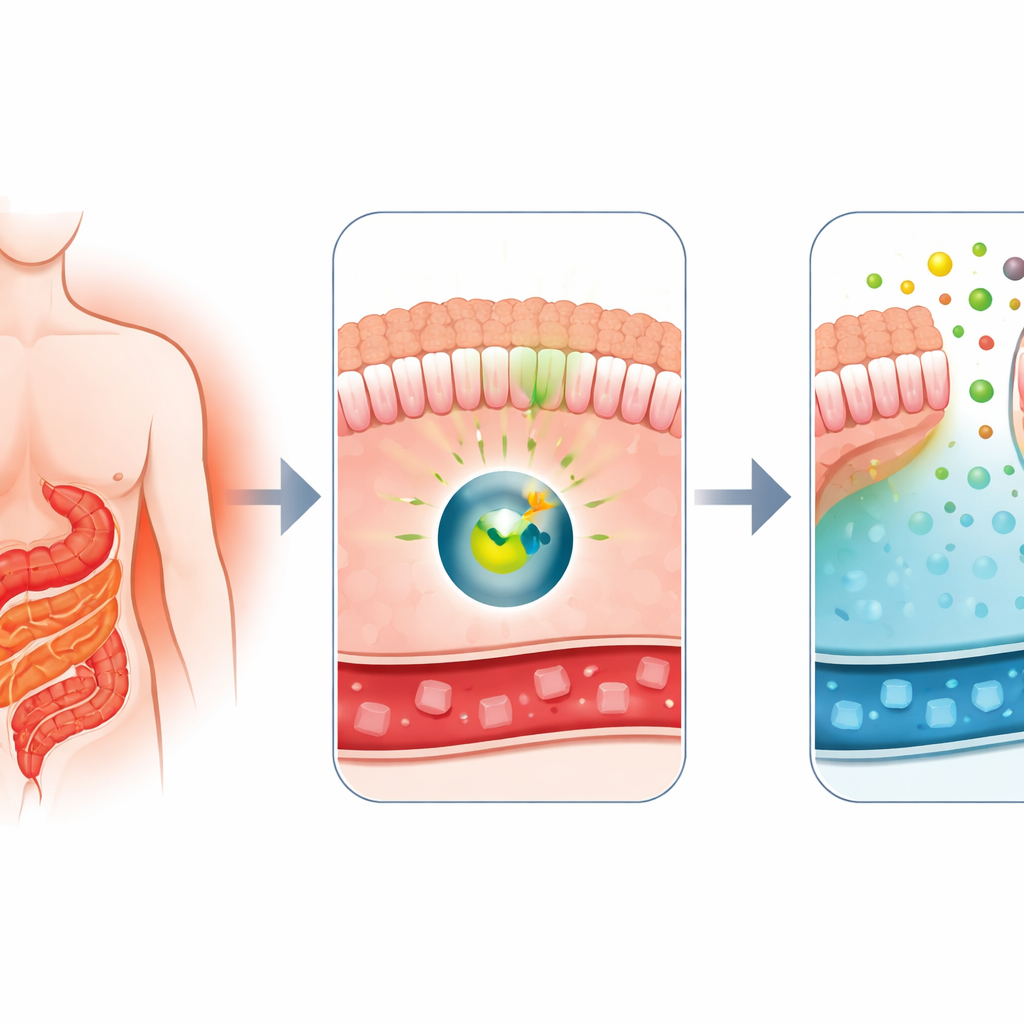
لماذا تغير الجراحة مستويات السكر بسرعة كبيرة
عرف الأطباء منذ زمن طويل أن تحويل المسار Roux-en-Y، وهو عملية شائعة لفقدان الوزن، يعد أيضاً من أقوى العلاجات لداء السكري من النوع 2. فور الجراحة، يتحسن سكر المرضى في الدم غالباً بشكل كبير، حتى قبل أن يفقدوا وزناً كبيراً. أظهر عمل سابق من هذه المجموعة أن أجزاء من الأمعاء الدقيقة تبدأ بعد التحويل بأن تتصرف كإسفنجة، تمتص الجلوكوز من مجرى الدم وتطلق بعضه إلى الفراغ الداخلي للأمعاء. بدا هذا السلوك الغريب، المسمى إفراز الجلوكوز المعوي، معتمداً على بروتين ناقل يُدعى GLUT1. والسؤال الكبير كان: ما هو المفتاح الجزيئي الذي يأمر الأمعاء بالتحول إلى هذا الوضع المخلّص للسكر؟
استخدام بيانات ضخمة للعثور على المفتاح الجزيئي
للبحث عن ذلك المفتاح، استخدم الباحثون نظام اكتشاف أدوية حسابي واسع النطاق مبني على Connectivity Map، قاعدة بيانات توضح كيف تغيّر آلاف المواد الكيميائية نشاط الجينات في الخلايا. قارَنوا أنماط التعبير الجيني من خمس حالات كانت فيها ظاهرة إفراز الجلوكوز المعوي مرتفعة—بما في ذلك نسيج من فئران خضعت للتحويل وخلايا عوملت بإشارة نمو معوية—مع الأنماط الناتجة عن أدوية معروفة. برزت فئة واحدة من المركبات بشكل ثابت: مُفعِّلات كيناز البروتين C (PKC)، وهي عائلة من الإنزيمات التي تنقل الإشارات داخل الخلايا. وعند التعمق أكثر، ركز الفريق على الفئة "الشاذة" من إنزيمات PKC، لا سيما الإنزيم المسمى PKCζ، التي كانت نشاطاته في خلايا الأمعاء الأكثر تطابقاً مع حالة الإفراز الشبيهة بالتحويل.
مضخة السكر في خلايا الأمعاء أثناء العمل
بالغوص إلى مستوى الخلية الواحدة باستخدام تسلسل RNA الخلوي أحادي الخلية، وجد المؤلفون أن جراحة التحويل تعزز كل من PKCζ وGLUT1 في خلايا امتصاص المغذيات المحددة المبطة للجزء البعيد من الأمعاء الدقيقة. في مزروعات خلوية ونماذج أمعاء بشرية عضوية، أدى زيادة PKCζ اصطناعياً أو المعالجة ببروستراتين—مركب نباتي يفعّل بأمان هذه الكينازات الشاذة—إلى دفع GLUT1 نحو سطح الخلايا. هناك عمل GLUT1 كمضخة ثنائية الاتجاه: سحبت المزيد من الجلوكوز من الجانب المواجه للدم في الخلايا وسمحت لجزء من الفائض بأن يخرج إلى مساحة الأمعاء. من المهم أن هذه إعادة توجيه السكر لم تُسرّع بشكل ملحوظ أيض السكر داخل الخلايا (التحلل السكري)، ما يشير إلى أن التأثير الرئيسي كان التخلص من الجلوكوز بدلاً من إنتاج طاقة إضافية.
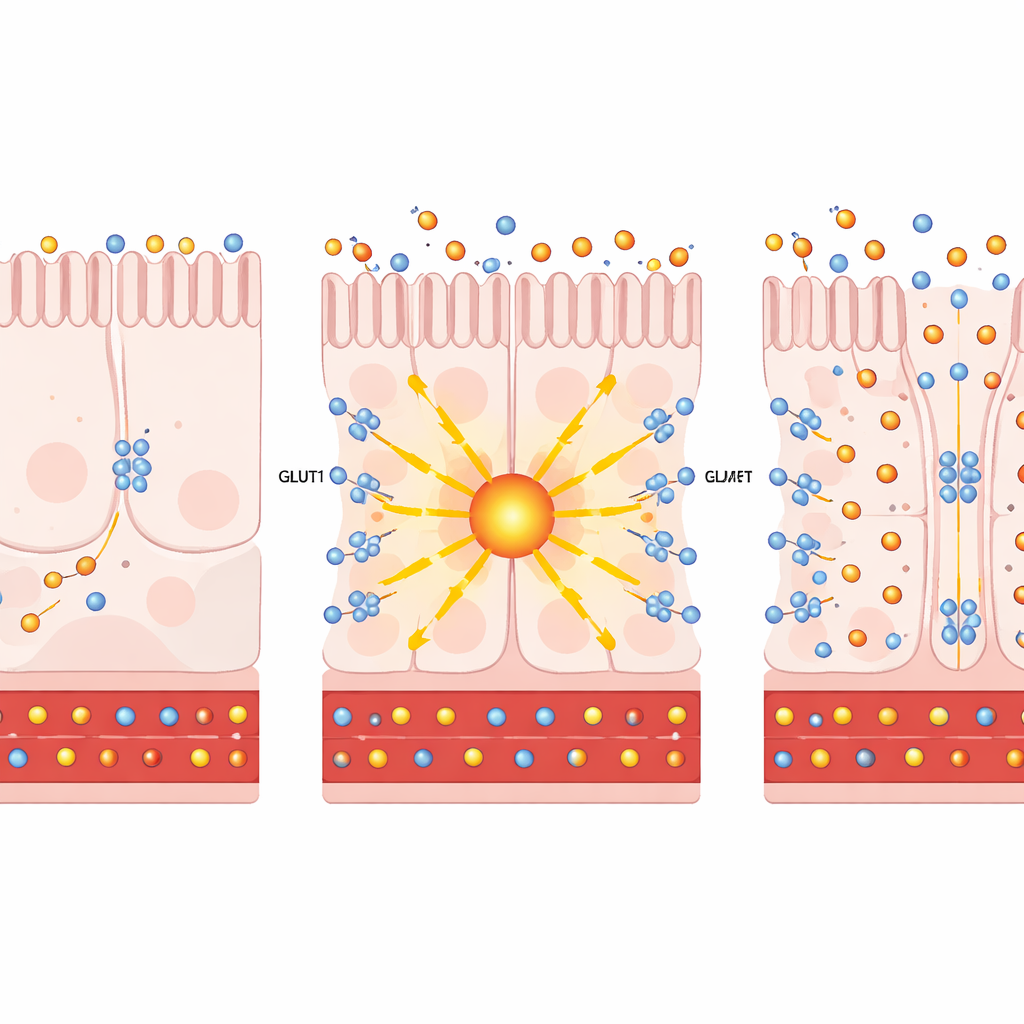
من الخلايا إلى الفئران: محاكاة الجراحة دون مشرط
اختبر الفريق بعد ذلك ما إذا كان تفعيل هذا المسار في الحيوانات الحية يمكن أن يحسّن السكري. في فئران سمينة مقاومة للإنسولين، أدى توصيل PKCζ إضافي موجه خصيصاً إلى الأمعاء إلى تباطؤ زيادة الوزن، وخفض سكر الصيام، وتحسن في تحمّل الجلوكوز. أظهرت متتبّعات سكر مشع امتصاصاً أكثر للجلوكوز من قبل الأمعاء البعيدة وطردها إلى تجويف الأمعاء. وظهرت صورة مشابهة في نماذج فئران مرضية عولجت ببروستراتين: فقدوا وزناً أقل، وتعاملوا مع أحمال السكر بشكل أفضل، وحوّلوا المزيد من الجلوكوز إلى القناة المعوية، وكل ذلك من دون تغيّر في مستويات الإنسولين أو تناول الطعام أو سلامة الحاجز المعوي. في شرائح النسيج، ظهر GLUT1 على جانبي الخلايا المواجه للدم والمواجه للأمعاء، موضوعة بشكل مثالي لسحب السكر من الدوران ودفعه إلى الأمعاء.
ماذا قد يعني هذا لرعاية السكري المستقبلية
للغير متخصص، الرسالة الأساسية هي أن الأمعاء يمكن تحويلها إلى منفذ مسيطر عليه لفرط سكر الدم. من خلال تنشيط إنزيم محدد داخل خلايا الأمعاء—كيناز البروتين الشاذ—استطاع الباحثون دفع الخلايا إلى تحريك المزيد من ناقلات GLUT1 إلى سطحها والتصرف كتصريف قابل للعكس، يسحب السكر من الدم ويعيد جزءاً منه إلى الأمعاء. في الفئران، حسّن هذا التصريف المعوي للسكر مستويات السكر في الدم وحدّ من زيادة الوزن دون تحفيز مفرط للإنسولين أو تغيير الشهية أو إتلاف الأمعاء. ورغم أن البروستراتين والمركبات المماثلة لم تُعتمد بعد كأدوية للسكري، فإن هذا العمل يشير إلى مسار aPKC–GLUT1 كهدف واعد لأدوية مستقبلية قد تعيد جزءاً من الفوائد الأيضية لجراحة المجازة المعدية من دون الحاجة لعملية جراحية.
الاستشهاد: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
الكلمات المفتاحية: إفراز الجلوكوز المعوي, داء السكري من النوع 2, ناقلة GLUT1, كيناز البروتين الشاذ, بروستراتين