Clear Sky Science · ar
المحدد الجزيئي لاعتماد تعطّل قناة Nav1.7 البشرية على الجهد الكهربائي يكشفه مثبط انتقائي لـ Nav1.7 قائم على الفعالية
خفض شدة إشارات الألم
لماذا يشعر بعض الأشخاص بألم مبرح نتيجة لمسة خفيفة بينما بالكاد يشعر آخرون بالألم؟ جزء كبير من الإجابة يكمن في بوابات بروتينية دقيقة داخل خلايانا العصبية تتحكم في الإشارات الكهربائية. تكشف هذه الدراسة كيف تجعل خصوصية بنيوية طفيفة في إحدى هذه البوابات، المسماة Nav1.7، هذه البوابة مهمة بشكل خاص في إثارة الألم — وكيف يمكن لمركب طبيعي، يُفاريغرافانول D، أن يغلقها انتقائياً. تشير النتائج إلى استراتيجية جديدة لتصميم مسكنات ألم تُهدئ الأعصاب المفرطة النشاط دون إبطاء القلب أو تعطيل الدماغ. 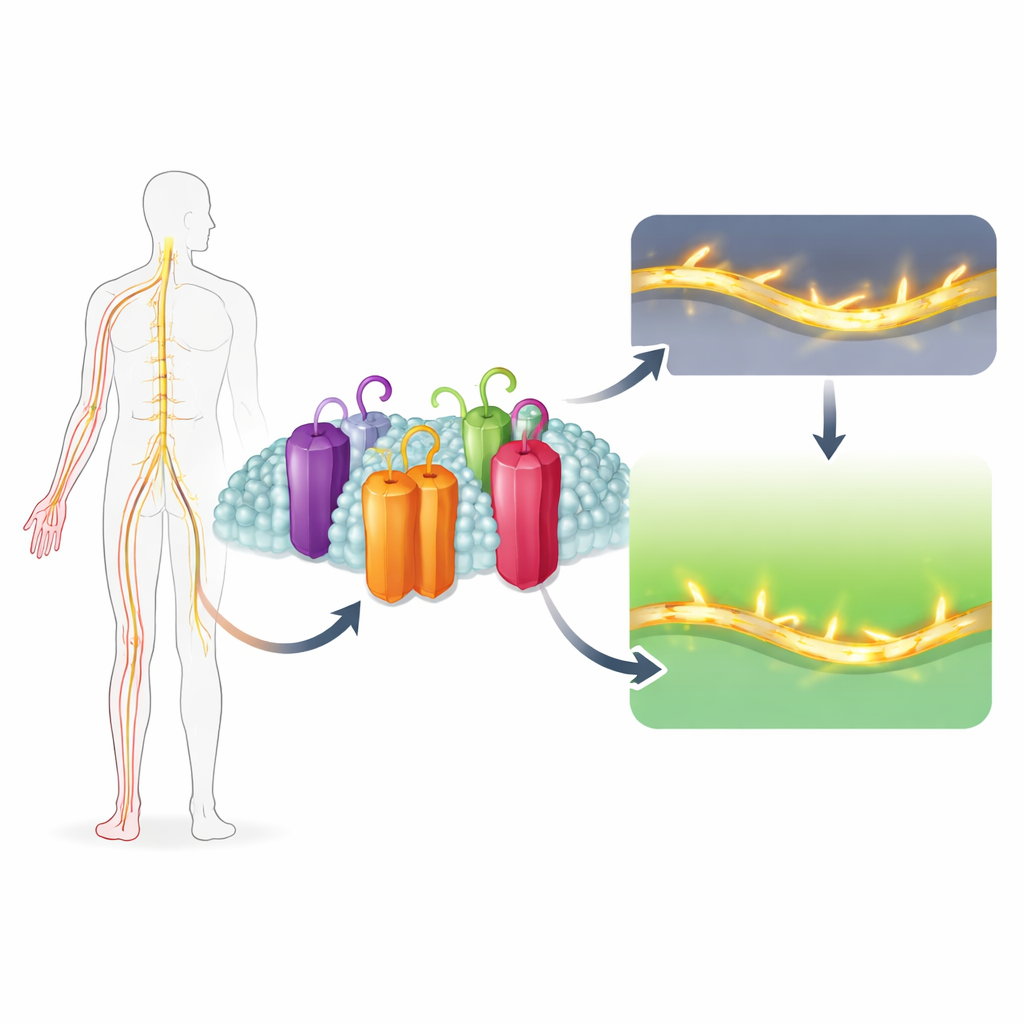
حارس خاص للألم
تطلق أعصابنا نبضات كهربائية بفضل قنوات الصوديوم، وهي مسام مجهرية تفتح لفترة قصيرة للسماح لأيونات الصوديوم الموجبة بالشحنة بالاندفاع إلى داخل الخلية. هناك تسع نسخ رئيسية من هذه القنوات في البشر، كل منها مخصّص لأنسجة مختلفة مثل الدماغ والعضلات والقلب أو أعصاب استقبال الألم. Nav1.7 هي النسخة المتمركزة في ألياف الألم المحيطية. تميزها قدرتها على الانفتاح والإغلاق عند جهود أقل مقارنة بقريباتها، ما يجعلها تستجيب حتى لأدنى تغيرات الجهد. هذا يجعل Nav1.7 مضخماً قوياً للإشارات الضعيفة المسببة للألم. تظهر الدراسات الوراثية أن فرط نشاط Nav1.7 يسبب متلازمات ألم موروثة شديدة، في حين أن غياب وظيفة Nav1.7 بالكامل يجعل الأشخاص غير قادرين على الشعور بالألم مطلقاً.
اكتشاف حاجز انتقائي للألم
لطالما طمح مطورو الأدوية لاستهداف Nav1.7 لعلاج الألم المزمن، لكنها تشبه عن كثب قنوات صوديوم أخرى حيوية لنبضات القلب ووظائف الدماغ. ترتبط معظم الأدوية التجريبية بعدة أنواع من القنوات، مسببة آثاراً جانبية أو تفشل في التجارب السريرية. فحص الباحثون أكثر من 1500 مركب طبيعي باستخدام اختبار خلوي يكتشف تغيّرات في جهد الغشاء. حددوا عائلة من الجزيئات من نبات Uvaria grandiflora، مع التركيز على مركب واحد يدعى يُفاريغرافانول D (UGD). قلّل UGD من تيارات الصوديوم في عدة أنواع من القنوات، لكنه كاد أن يطفئ Nav1.7 تماماً بينما حجب نصف التيار تقريباً في قنوات صوديوم أخرى حتى عند جرعات عالية. هذا يعني أن انتقائيته لا تنبني على ارتباط أوثق فحسب، بل على تأثير أقوى بكثير بعد الارتباط.
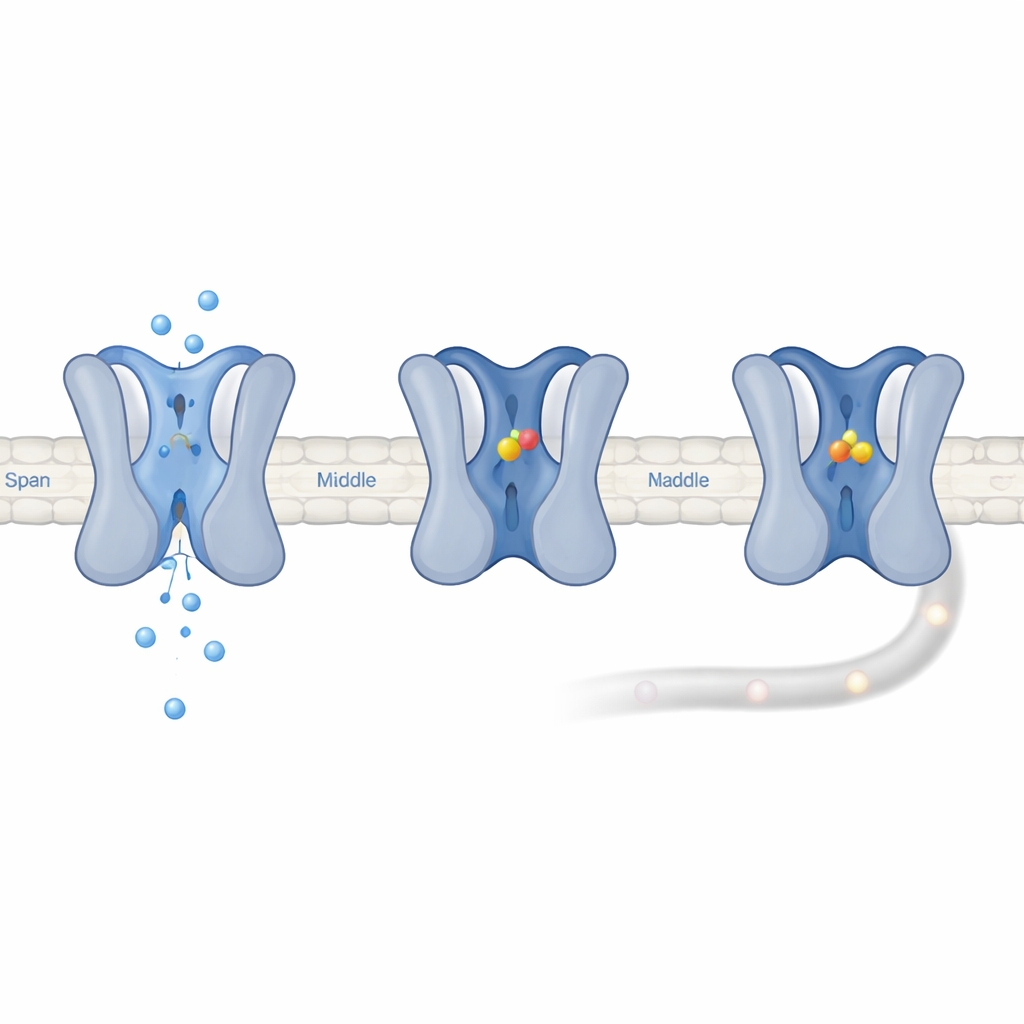
تغير على مستوى ذرة واحدة يجعل Nav1.7 فريداً
لفهم سبب فعالية UGD على Nav1.7، بنى الفريق قنوات تهجينية (chimeric) تبدّل قطعاً بين Nav1.7 وقناة دماغية قريبة، Nav1.2. حدّدت هذه المقاربات منطقة صغيرة قرب فم المسام الخارجي، بين مقطعين هيكليين يسمى S5 وS6 في المجال الثالث، باعتبارها المحدد الرئيسي لقوة الحجب الكامل لUGD. كشف مقارنة تسلسلات الأحماض الأمينية أن Nav1.7 تحمل وحدها ثريونين في الموضع 1398، بينما تحمل كل قنوات الصوديوم البشرية الأخرى ميثيونين أكبر حجماً هناك. عندما استبدل الباحثون ثريونين Nav1.7 بميثيونين، لم يعد UGD قادراً على إغلاق القناة تماماً؛ واستبدال الميثيونين بثريونين في Nav1.2 جعل تلك القناة تتصرف مثل Nav1.7. هذا الاستبدال الفردي حوّل أيضاً الجهد الذي تفتح وتتعطل عنده القنوات: جعل الثريونين القناة تفتح وتتعطل عند جهود أكثر سلبية وبسرعة أكبر، وهي خصائص تُفضّل وجود Nav1.7 في حالة غير راحة حتى بالقرب من جهد الراحة الطبيعي للخلايا العصبية الحسية للألم.
إقفال القناة في وضع راحة-منخفض
أظهرت التسجيلات الكهربائية أن UGD لا يلتصق بـ Nav1.7 حين تكون مغلقة أو مفتوحة لفترة وجيزة. بل يفضّل القنوات التي دخلت حالة "التعطّل البطيء" طويلة الأمد، حيث يكون المسام مغلقاً ويستغرق مئات الملّي ثانية أو أكثر للتعافى. حين وُجد UGD، استغرق خروج القنوات من هذه الحالة نحو عشرة أضعاف المدة عادة، مما يعني أن UGD يثبّت هذه الحالة. اقترحت المحاكاة الحاسوبية أن UGD يستوطن في جيب يتكوّن حيث يلتقي حلقة من المجال الثالث مع لولب في المجال الرابع، ويكوّن اتصالات رئيسية مع خمسة أحماض أمينية. أضعف تبديل أي من هذه البقايا تأثير UGD، مما يؤكد أهمية هذا الجيب. وبما أن بنية Nav1.7 الغنية بالثريونين تدفعها للانتقال إلى حالات معطلة عند جهود أقل، فعدد أكبر من قنواتها يكون في الحالة التي يفضّل UGD الارتباط بها، ما يفسر سبب كبت Nav1.7 وظيفياً أكثر بكثير من قريباتها رغم تشابه قوة الارتباط.
من مسام الأيونات إلى تخفيف الألم
في النهاية، ما يهم هو كيفية تأثير هذه الأحداث الجزيئية على الخلايا الحقيقية. في خلايا حسية للألم من عقدة الجذر الظهرية لدى الجرذان، قلّل UGD كثيراً عدد جهد الفعل — النبضات السريعة للجهد التي تحمل معلومات الألم — وفي النهاية أوقفها تماماً عند تراكيز ميكرومولارية منخفضة وما دون ميكرومولار. في المقابل، كانت خلايا شبيهة بالقلب بشرية مشتقة من الخلايا الجذعية، والتي تستخدم بشكل أساسي قناة صوديوم مختلفة (Nav1.5) وتستريح عند جهد أقل قليلاً، أقل حساسية بحوالي 60 مرة. هذا يوحي بأن حاجزاً "انتقائياً بالفعالية" مثل UGD يمكنه أن يخمد مسارات الألم أكثر بكثير من الأنسجة القلبية أو المنبهة الأخرى ببساطة بسبب عدد المرات التي تقضيها Nav1.7 في حالتها المعطلة والمفضّلة دواءً.
ماذا يعني هذا لعلاجات الألم المستقبلية
تكشف الدراسة أن تفصيلاً بنيوياً صغيراً — ثريونين واحد — يكمن وراء سلوك Nav1.7 المميز عند جهود منخفضة وقدرته على توليد "تيارات العتبة"، الإشارات الصغيرة التي تحدد ما إذا كانت خلية الألم ستطلق نبضة أم لا. من خلال الارتباط وتثبيت الشكل المعطّل لهذه القناة، يستغل UGD تلك النزعة المدمجة ويكبت Nav1.7 بقوة أكبر من قنوات الصوديوم الأخرى. للغير مختص، الخلاصة هي أن الباحثين حددوا نقطة ضعف دقيقة في بوابة الألم بالجسم وأظهروا طريقة للضغط عليها دون تعطيل قنوات القلب أو الدماغ بشكل كبير. تفتح هذه الرؤية طريقاً لتصميم مسكنات ألم جديدة تُهدئ الأعصاب المفرطة النشاط عبر استهداف سلوك الجهد وحالة القناة، بدلاً من ملاحقة الارتباط الأوثق فقط إلى Nav1.7.
الاستشهاد: Zhao, F., Xi, C., Li, J. et al. Molecular determinant of low-voltage dependence of human Nav1.7 inactivation revealed by efficacy-based Nav1.7 selective inhibitor. Nat Commun 17, 2559 (2026). https://doi.org/10.1038/s41467-026-69184-8
الكلمات المفتاحية: قناة الصوديوم Nav1.7, الألم المزمن, يُفاريغرافانول D, التثبيط المعتمد على الحالة, قنوات الصوديوم البوابية بالجهد