Clear Sky Science · ar
آلية ضخ Na+ المدفوعة بالأكسدة والاختزال في ناقل NADH-quinone في Vibrio cholerae تعتمد على تغيّرات تبادُلية في التشكّل
كيف أصبح مصنع طاقة الكوليرا هدفًا دوائيًا
البكتيريا المسببة للكوليرا، Vibrio cholerae، تبقى على قيد الحياة وتتكاثر بتشغيل محطة طاقة جزيئية صغيرة في غشاء خليةها. تكشف هذه الدراسة، بتفصيل غير مسبوق، كيف يتغير شكل أحد محركاتها الرئيسية — إنزيم يُدعى Na⁺-NQR — أثناء عمله لضخ أيونات الصوديوم خارج الخلية. فهم هذه الآلية الجزيئية لا يكتفي بإرضاء الفضول الأساسي حول كيفية تحويل الحياة للطعام إلى طاقة قابلة للاستخدام، بل يشير أيضًا إلى طرق جديدة لتصميم مضادات حيوية تُعطّل البكتيريا الضارة دون التأثير على خلايا الإنسان.
محرك يعمل بالصوديوم في البكتيريا
تعتمد العديد من البكتيريا البحرية والممرِضة على Na⁺-NQR كخطوة أولى في سلسلة التنفس، وهي سلسلة التفاعلات التي تستخرج الطاقة من المغذيات. يقع Na⁺-NQR في الغشاء الداخلي ويأخذ الإلكترونات من جزيء وقود يُدعى NADH، مارًا بها عبر سلسلة من الجزيئات المساعدة المُلوّنة (المعروفة بالمُقارنات أو cofactors) إلى الكوينون، وهو جزيء صغير آخر مُضمّن في الغشاء. مع تدفّق الإلكترونات، يستخدم الإنزيم تلك الطاقة لدفع أيونات الصوديوم (Na⁺) من داخل الخلية إلى الخارج، مكوّنًا تدرّجًا للصوديوم. هذا التدرّج يشبه بطارية مشحونة: يُشغّل محرّك السوط الجرثومي للسباحة، ويساعد في إنتاج ATP (عملة طاقة الخلية)، ويدعم امتصاص المغذيات وطرد الأدوية. وبما أن Na⁺-NQR يوجد فقط في البكتيريا ويختلف اختلافًا كبيرًا عن الإنزيم ذي الصلة في ميتوكوندريا الإنسان، فهو هدف جذّاب لمضادات حيوية ذات انتقائية عالية.
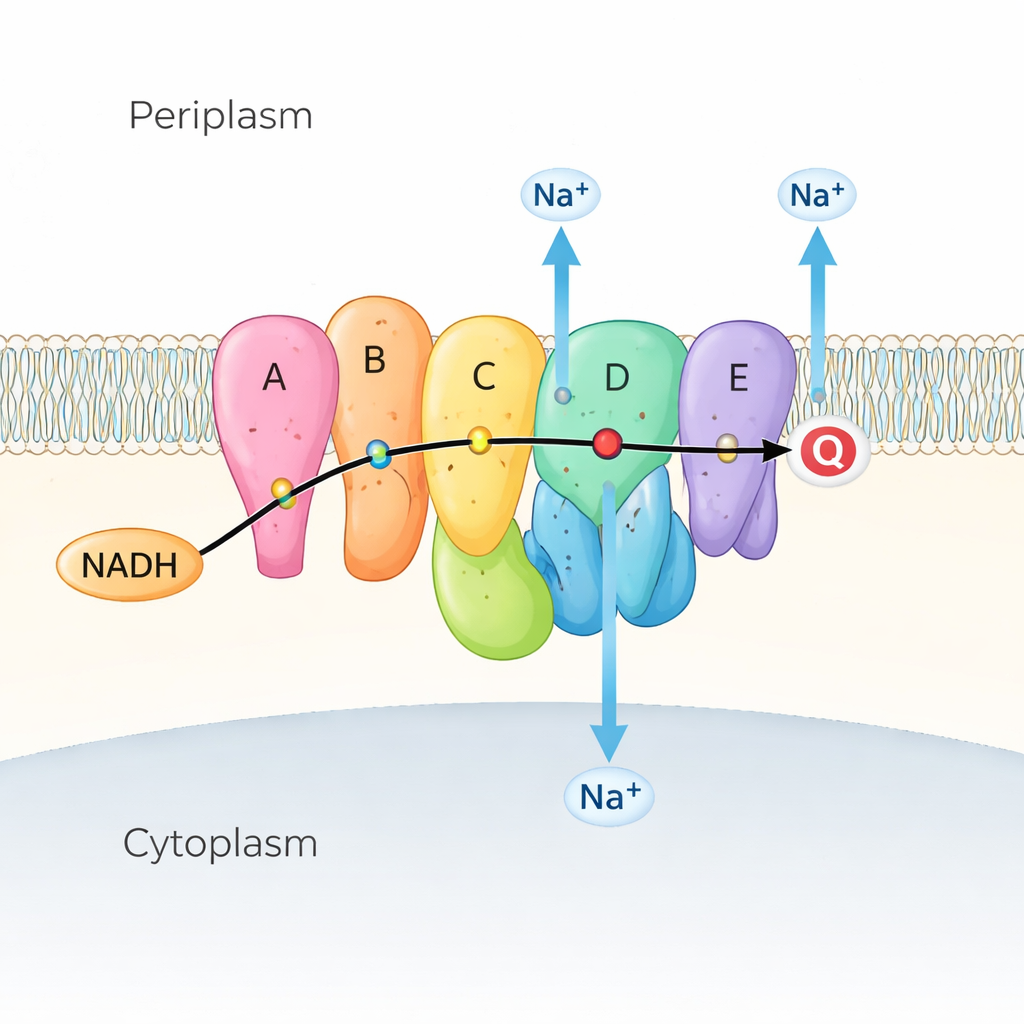
رصد حركة الآلة
أظهرت لقطات بالأشعة السينية والميكروسكوب الإلكتروني بالتجميد السابقة مواقعٍ فرعية ووحدات Na⁺-NQR ومقارناته، لكنها كشفت أيضًا لغزًا: بعض القفزات الإلكترونية الحرجة كانت بعيدة جدًا عن بعضها بحيث لا يمكن للإلكترونات أن تنتقل بكفاءة ما لم يتحوّل شكل البروتين. عالج المؤلفون هذا بالتقاط Na⁺-NQR في حالات مختلفة بدرجات طفيفة. استخدموا طفرات تزيل مقارنات محددة، وأدوية توقف التفاعل في مراحل معينة، ومحاليل بوجود أو بدون صوديوم. باستخدام cryo-EM عالي الدقة وتحليل صور متقدّم، تمكنوا من فصل وإعادة بناء حالات تكوّن متعددة لنفس الإنزيم، محولين اللقطات الثابتة فعليًا إلى فيلم لدورته العاملة.
ذراع مرنة ومشبك ناقل متحرك
أحد الاكتشافات الرئيسية يتعلق بوحدة سيتوبلازمية مرنة، NqrF، التي تحمل مقارنين ناقلين للإلكترون. حدّدت المجموعة ثلاث مواضع لمجالها الشبيه بالفيريدوكسين — المُلقب بحالات «أعلى»، «وسط»، و«أسفل». في الحالة النادرة لكنها الحرجة «الأسفل»، يتأرجح هذا المجال الصغير إلى جيب تشكّله وحدتان غشائيتان، NqrD وNqrE، مقربًا مجموعة الحديد–كبريت الخاصة به بما يكفي لتمرير إلكترون إلى الأمام. في الوقت نفسه، تتصرف وحدة محيطية (خارجية) تسمى NqrC كمشبك قابل للتحريك. في إحدى البنى («المستقرة») تتأوّضع بجانب وحدة غشائية أخرى، NqrB، موضوعةً لتمرير الإلكترونات نحو المستقبل النهائي الكوينون. في بنية ثانية («المنقولة») تتحرّك NqrC نحو NqrD/E، مقربةً مُقارن الفلافين الخاص بها ليستقبل إلكترونًا من مركز الحديد–كبريت الخاص بهما. تُظهر هذه الحركات أن NqrF وNqrC يتصرفان كقوافل ديناميكية، تجسران فجوات كبيرة في سلسلة المقارنات.
كيف تضخ تغيّرات الشكل الصوديوم
يكمن جوهر مضخة الصوديوم في الوحدتين المزدوجتين NqrD وNqrE، اللتين تشكّلان حزمة مركزية من الحلزونات العابرة للغشاء. باستخدام كل من البُنى والمحاكاة الديناميكية الجزيئية على المستوى الذري، يُظهر المؤلفون أنه عندما يُختزَل (يكتسب إلكترونًا) مركز الحديد–كبريت في NqrD/E، فإنه يخلق موقعًا مشحونًا سالبًا يجذب أيون Na⁺ وبعض جزيئات الماء من الجانب السيتوبلازمي، مكوّنًا جيب ارتباط عابر. تتصرّف الأحماض الأمينية المحبة للدهون أعلاه وأسفله كبوابات داخلية وخارجية، متحكمةً في وصول الأيون. عندما تتحول NqrD/E من شكل «مفتوح للداخل» إلى «مفتوح للخارج»، يتحرّك Na⁺ نحو الجانب البروتوبلازمي ويُطلق في النهاية مع إعادة أكسدة مركز الحديد–كبريت. تُظهر المحاكاة بقاء Na⁺ مرويًا جزئيًا بالماء ولكن دون وجود ممر مائي ممتد، مما يشير إلى أن الإنزيم محكم الإغلاق ضد تسريبات البروتون غير المرغوب فيها.
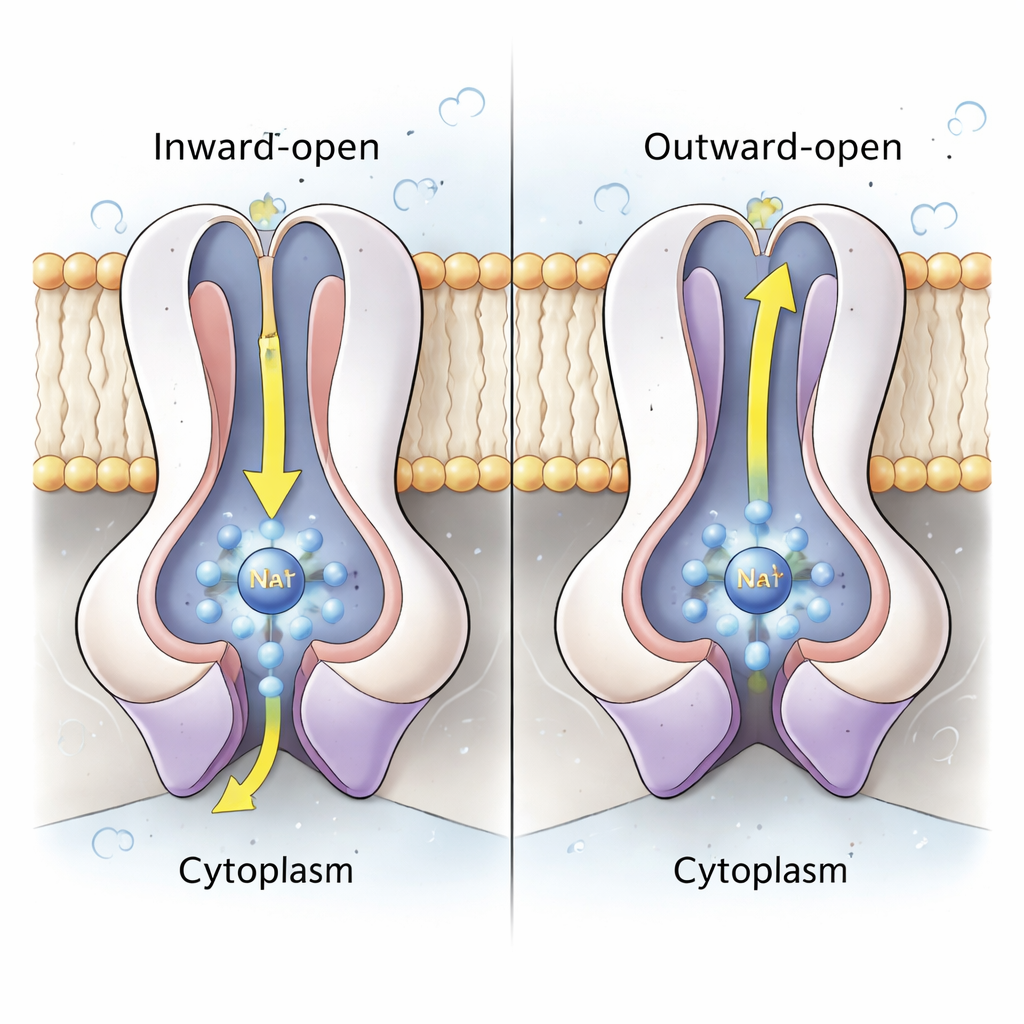
دورة منسقة تقفل الاتّجاه
من خلال دمج كل حالاتهم البُنائية والمحاكاة، يقترح الباحثون دورة من ست خطوات. يرتبط NADH أولًا ويتبرع بالإلكترونات إلى NqrF، الذي يمرر بعد ذلك إلكترونًا إلى NqrD/E، مما يحفّز امتصاص Na⁺ من السيتوبلازم وتحميل الجيب المركزي. يؤدي تبدّل البنية الناتج لـ NqrD/E إلى الشكل المفتوح للخارج إلى طرد Na⁺ إلى الفضاء الخارج البلازمي ويشجّع NqrC على التحرك إلى الموضع المناسب لاستقبال الإلكترون. تنقل الخطوات اللاحقة الإلكترونات إلى الفلافين والريبوفلافين ومن ثم إلى الكوينون، الذي يجب أن يستقبل إلكترونين ليصبح كوينولًا. والأهم من ذلك، أن تغيّرات الشكل نفسها التي تحرّك Na⁺ تُرخّي وتُصلب بالتناوب NqrF وNqrC، ما يجعل تدفّق الإلكترونات إلى الأمام مرجحًا فقط عندما يتم ضخ Na⁺ للخارج ويثبّط الانزلاق العكسي. تساعد هذه المطابقة الإنزيم على ضخ Na⁺ عكس تدرّج موجود، محافظةً على «بطارية» البكتيريا مشحونة.
لماذا يهم هذا للطب وعلم الأحياء
بالنسبة للقارئ غير المتخصّص، توضح هذه الأعمال كيف تبني الحياة آلات متقنة التنسيق من البروتينات، حيث تحفّز تغيّرات صغيرة في الشحنة حركات كبيرة ومفيدة. لأبحاث الأمراض المعدية، توضح النتائج أن انتقال Na⁺ في Na⁺-NQR يحدث بشكل رئيسي عبر لبّ NqrD/E، وليس عبر الوحدة NqrB التي كانت مشتبَهًا بها سابقًا. تُصقل هذه الرؤية مواقع ارتباط الأدوية المستقبلية لتعطيل المحرك الذي يزوّد Vibrio cholerae ومسارات ممرِضة أخرى بالطاقة، مع تجنّب الإنزيمات البشرية. على نطاق أوسع، توفّر الدراسة مخططًا بنيويًا لكيفية توصيل تفاعلات الأكسدة والاختزال لضخ الأيونات — مبدأ تصميم تعيد الطبيعة استخدامه في أشكال عديدة من الآلات الحيوية للطاقة.
الاستشهاد: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
الكلمات المفتاحية: مضخة الصوديوم, تنفس بكتيري, Na+-NQR, تجميد إلكتروني - الميكروسكوب (cryo-EM), أهداف مضادات حيوية