Clear Sky Science · ar
نظام اصطناعي للتحكم بالموت الخلوي الالتهابي استجابةً للـ RNA قائم على نيوكلياز–بروتياز CRISPR من النوع III-E
تحويل انفجارات الخلايا القاتلة إلى أدوات موجهة
في بعض الأحيان تدافع أجسامنا عن نفسها بجعل الخلايا المصابة أو التالفة تنفجر في شكل مدمر من الانتحار الخلوي المصحوب بالالتهاب. هذا الانفجار لا يزيل الخلايا الخطيرة فحسب، بل يستدعي أيضاً الجهاز المناعي. تقدم الدراسة الجديدة دائرة جينية اصطناعية تُدعى DAMAGE، قادرة على قراءة رسائل الـ RNA داخل الخلية وتقرير ما إذا كانت تلك الخلية يجب تدميرها. من خلال ربط نظام دفاع ميكروبي بآلية موت الخلايا البشرية، يُظهر الباحثون طريقة لمحو الخلايا المصابة بالفيروسات أو الخبيثة أو المتقدمة في العمر بشكل انتقائي مع الحفاظ على الخلايا السليمة المجاورة. 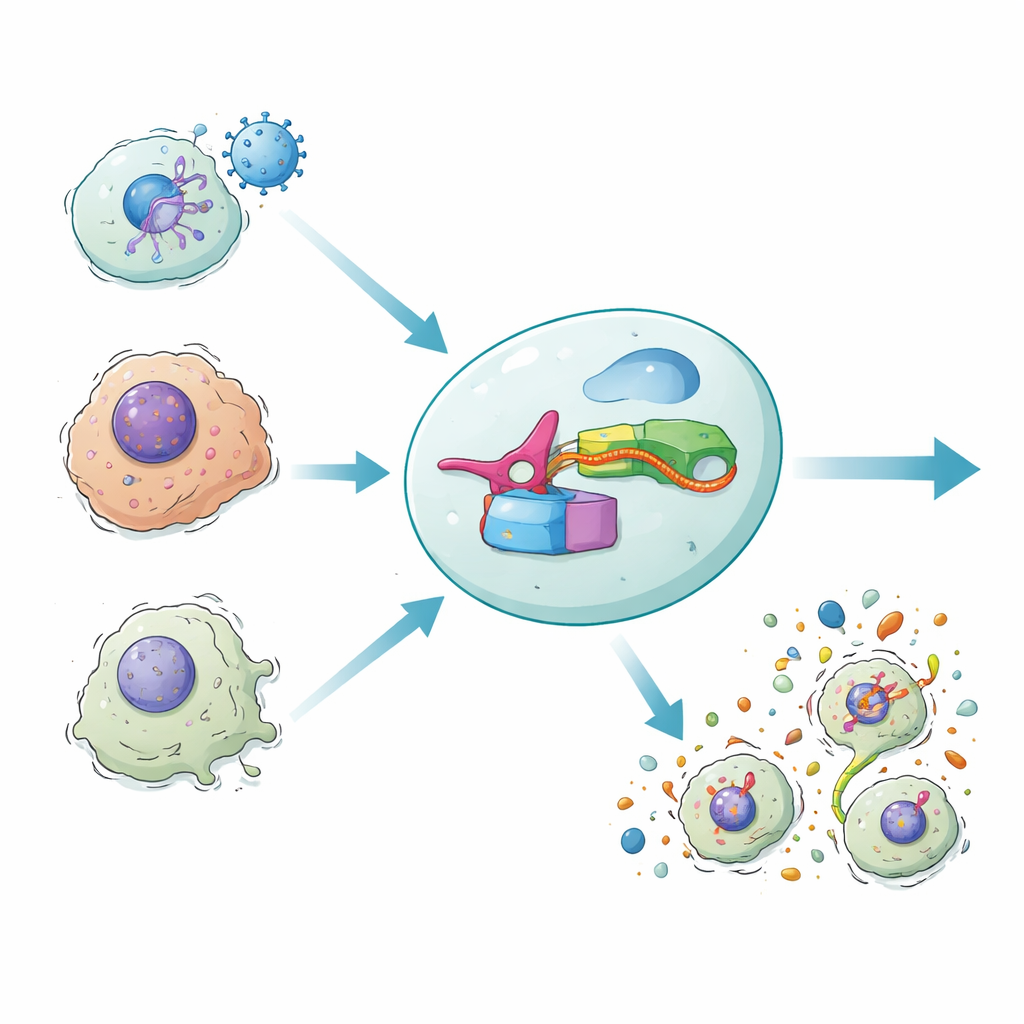
كيف تفجّر الخلايا نفسها طبيعياً
في الموت الخلوي الالتهابي، توجد عائلة من البروتينات تُدعى الغازدرمين داخل الخلايا كقنابل محشوة. لكل غازدرمين نصف أمامي «قاتل» يستطيع ثقب أغشية الخلايا، ونصف خلفي «غطاء أمان» يقيّد هذا القاتل. عندما تكتشف حساسات المناعة وجود خطر، تقصّ إنزيمات الغازدرمين إلى نصفين، مطلقة النصف الأمامي لتجميع مسام في الغشاء الخارجي. تنتفخ الخلية، تنفجر، وتطرح إشارات إنذار تجذب خلايا الجهاز المناعي. هذه الاستجابة القوية تساعد في مكافحة العدوى والأورام، لكن شبكات التحكم الطبيعية معقدة وصعبة إعادة توصيلها للعلاج.
استعارة دفاعات بكتيرية لقراءة الـ RNA
طوّرت البكتيريا وحدات دفاعية مدمجة معروفة اليوم من خلال تكنولوجيا CRISPR. أحد هذه الأنظمة، النوع III-E، يستخدم بروتيناً يُدعى Cas7‑11 يمكنه الالتصاق بتسلسلات RNA محددة بمساعدة دليل RNA قصير. عندما يجد Cas7‑11 RNA مطابقاً، يُفعّل إنزيم مرافقاً، Csx29، الذي يقطع بروتيناً شريكاً، Csx30. أدرك المؤلفون أن Csx30 يمكن أن يعمل «مفصلاً» قابل التخصيص بين أي جزأين بروتينين. دمجوا هذا المفصل بين نصفي القتل وغطاء الأمان في الغازدرمين البشري، فأنشأوا منفذين اصطناعيين ينفصلون فقط عندما يكتشف المستشعر الشبيه بـ CRISPR الـ RNA المستهدف داخل الخلية.
مفتاح موت قابل للبرمجة للخلايا المريضة
يتكوّن هذا التصميم المسمى DAMAGE (اختصاراً لـ Death Manipulation Gene) من خمسة مكونات: مستشعر Cas7‑11، قاطع Csx29، اندماج غازدرمين–Csx30، دليل RNA، والـ RNA المستهدف داخل الخلية. عندما يظهر الرسالة الـ RNA الصحيحة، يرتبط Cas7‑11 بها، يفعل Csx29، ويقّطع Csx29 مفصل Csx30 في البروتين الاندماجي. يتحرّر النصف القاتل من الغازدرمين، يحفر مساماً في الغشاء، وتموت الخلية في انفجار التهابي. ببساطة تغيير دليل RNA أعاد توجيه DAMAGE إلى أهداف خلوية مختلفة. أظهروا أنه يمكنه التعرف على RNA من فيروس الجهاز التنفسي المخلوي، وفيروس الورم الحليمي البشري عالي المخاطر في خلايا سرطان عنق الرحم، وعدداً من طفرات KRAS المسببة للسرطان التي تختلف عن RNA الطبيعي بحرف واحد فقط. في كل حالة، أُزيلت الخلايا الحاملة للـ RNA المشبوه بشكل انتقائي، بينما بقيت الخلايا الشاهدة المجاورة سليمة. 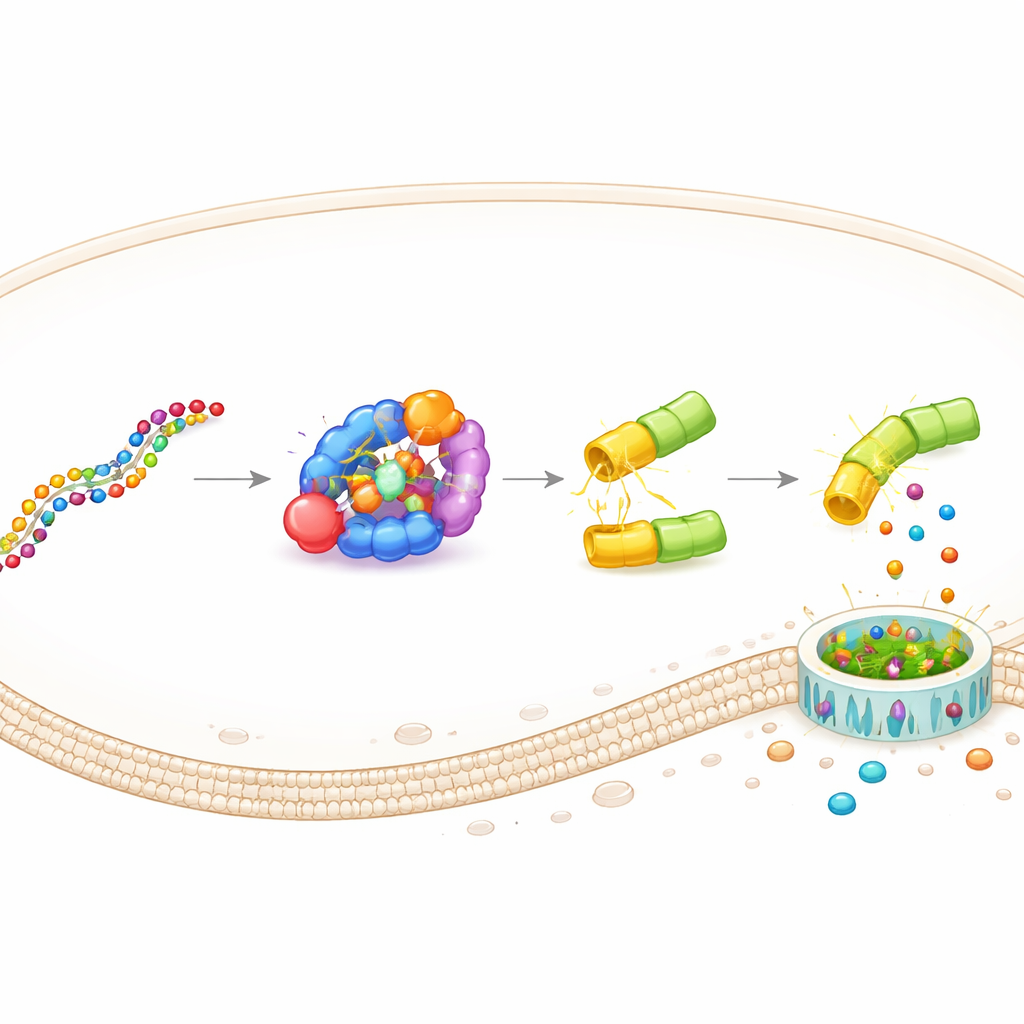
التركيز على الخلايا المسنة
سأل الباحثون أيضاً إن كان DAMAGE يستطيع مطاردة الخلايا الشيخوخية—الخلايا المسنة أو المضغوطة التي تتوقف عن الانقسام لكنها تتراكم في الأنسجة وتساهم في الضعف والمرض المزمن. عادةً ما تزيد هذه الخلايا من إنتاج بروتينين حارسيين، p16 وp21. من خلال برمجة أدلة تستهدف الـ RNA لكل من p16 وp21، أعدّ الفريق نسخة اسمها DAMAGE‑Aging. قتلت هذه الدائرة الخلايا ذات مستويات عالية من هذه الرسائل بينما بيّنت حماية للخلايا التي أُزيل فيها p16 جينياً، مؤكدة أن النظام يقرأ وفرة الـ RNA في الزمن الحقيقي بدلاً من تغييرات ثابتة في الـ DNA. علاجات دوائية رفعت مستويات p16 أو p21 جعلت الخلايا أكثر عرضة لهذا الانتحار المستهدف.
تغليف النظام للعلاجات المستقبلية
للاقتراب من التطبيق العملي، كبّش المؤلفون أجزاء الـ DNA المتعددة لـ DAMAGE في تركيب مبسّط، DAMAGE‑Plus، وأظهروا أنه لا يزال يعمل بشكل موثوق. ثم نسخوا هذا التركيب إلى mRNA اصطناعي، وحزموه في جسيمات دهنية نانوية مشابهة لتلك المستخدمة في لقاحات كوفيد‑19، ووصلوه إلى خلايا في مزرعة خلوية. نجح إصدار الـ mRNA في تجميع الدائرة وإطلاق موت التهابي مستهدف في الخلايا الحاملة للـ RNA الفيروسي أو المرتبط بالسرطان. على الرغم من أن النظام ككل لا يزال ضخم الحجم ولم يُختبر إلا في خطوط خلوية، فإن هذه النتائج توحي بأن القتل الخلوي المبرمج الموجَّه بالـ RNA قد يُنشر يوماً ما عبر تركيبات mRNA قابلة للحقن.
طريقة جديدة لقراءة الرسائل الخلوية والتفاعل معها
بعبارات بسيطة، يُعد DAMAGE حارساً جزيئياً يتحقق من «معرّف» الـ RNA الداخلي لكل خلية ويُخرج فقط تلك التي تبدو خطرة—مصابة بفيروس، حاملة لطفرات، أو مسنة—عن طريق دفعها إلى شكل انفجاري من الانتحار الخلوي. تُظهر الدراسة أنه يمكن ربط مجسات RNA البكتيرية بآليات موت الخلايا البشرية بدقة عالية، حتى لتمييز اختلافات بحرف واحد في الرسائل الوراثية. وبينما ما زال ثمة عمل هندسي كبير مطلوب قبل أن يُستخدم مثل هذا النظام بأمان في الحيوانات أو البشر، يلخّص البحث استراتيجية قوية جديدة: قراءة ضوضاء الـ RNA الحية داخل الخلايا وترجمتها مباشرة إلى قرارات حياة أو موت.
الاستشهاد: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
الكلمات المفتاحية: الانفجار الخلالي الالتهابي (بايروسيتوز), CRISPR, علاج موجه بواسطة RNA, مناعة السرطان, شيخوخة الخلايا