Clear Sky Science · ar
تجمعات ذات دقة ذرية لبروتينات غير منظمة بطبيعتها باستخدام AlphaFold
لماذا تهم البروتينات المتغيرة الشكل
تمتلئ خلايانا ببروتينات لا تستقر أبدًا في شكل واحد جامد. تتصرف هذه البروتينات "غير المنظمة بطبيعتها" أكثر مثل المعكرونة المترهلة منها كآلات مطوية بعناية، ومع ذلك فهي مركزية في عمليات تتراوح من إشارات الخلايا إلى الأمراض العصبية التنكسية. وبما أنها تتحرك وتتغير باستمرار، فإن التقاط كامل مدى أشكالها بتفاصيل ذرية أمر صعب للغاية وعادةً ما يتطلب سنوات من التجارب وحسابات مكثفة. يعرض هذا المقال طريقة جديدة لاستغلال الذكاء الاصطناعي والفيزياء معًا لرسم خريطة هذه الجزيئات القلقة بكفاءة أكبر بكثير.
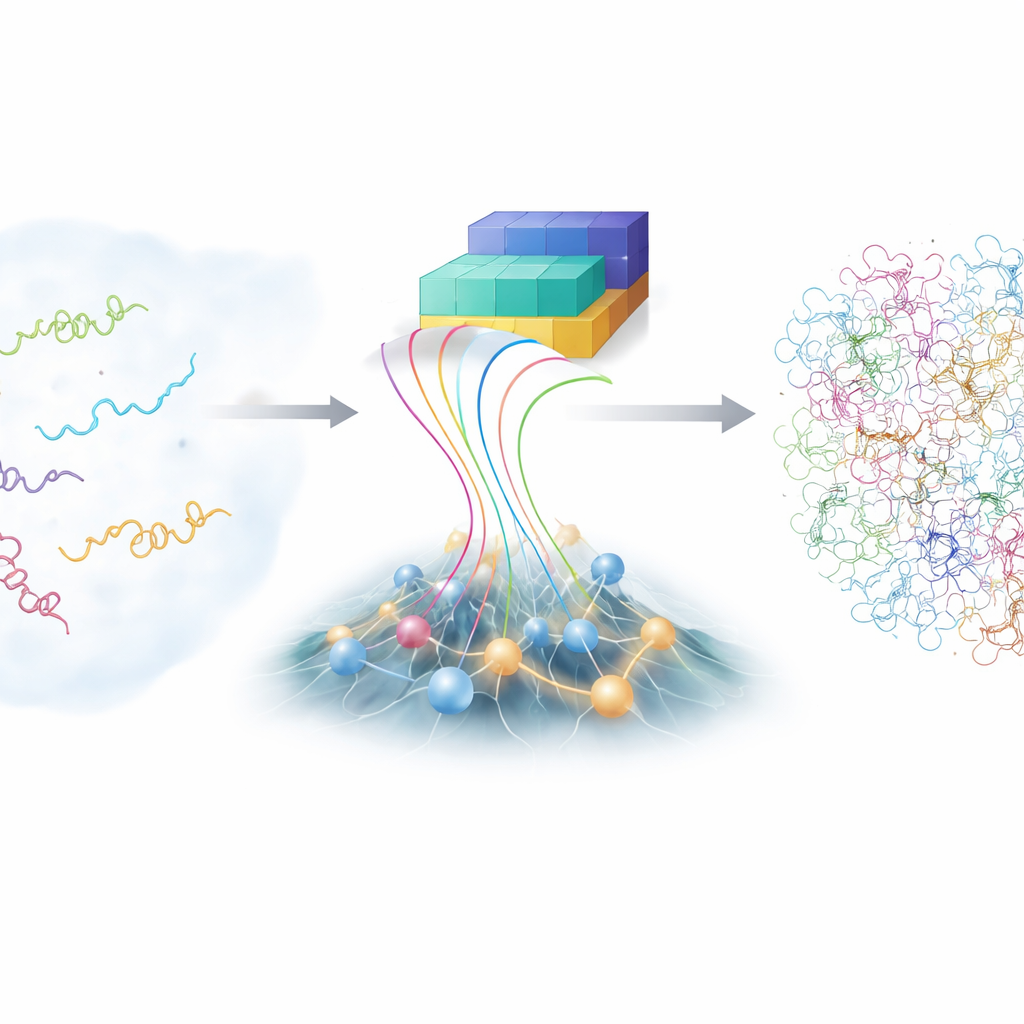
تحدي الجزيئات القلقة
على عكس نماذج البروتين في الكتب المدرسية التي تظهر بنية واحدة مرتبة، تتجول البروتينات غير المنظمة بطبيعتها عبر مشهد شاسع من الأشكال الممكنة. تساعدها هذه المرونة على التعرف على شركاء متعدّدين، لكنها تجعل دراستها صعبة للغاية. تقنيات المختبر التقليدية، مثل الرنين المغناطيسي النووي المتقدم ونشر الأشعة السينية، يمكنها أن تقدم معلومات متوسطة عبر العديد من الأشكال لكنها لا تكشف كل هيئة على حدة. يمكن لمحاكاة الحاسوب بتفصيل ذري كامل، من حيث المبدأ، تتبع كل ذرة بينما يلتف البروتين غير المنظم، ومع ذلك فهي مكلفة للغاية وتعتمد على نماذج فيزيائية مضبوطة بدقة. ونتيجة لذلك، لدى المجتمع العلمي مجموعة محدودة فقط من تجمعات البروتينات غير المنظمة الدقيقة والمفصلة للتعلم منها.
دمج التخمينات الذكية مع قواعد فيزيائية
في السنوات الأخيرة، أذهل عائلة أدوات التعلم العميق AlphaFold علم الأحياء بتوقع هياكل البروتينات من سلاسل الأحماض الأمينية. بالنسبة للبروتينات غير المنظمة، ومع ذلك، فإن قوة AlphaFold الاعتيادية—التنبؤ بأفضل شكل واحد—أقل فائدة، لأن هذه البروتينات لا تمتلك شكلًا واحدًا فقط. ما توفره AlphaFold مع ذلك هو معلومات غنية حول مدى احتمال اقتراب أو ابتعاد أجزاء مختلفة من السلسلة عن بعضها البعض. بنى المؤلفون إطارًا جديدًا يُدعى bAIes يعامل هذه المعلومات المستمدة من الذكاء الاصطناعي كدليل طري ويخلطها مع نموذج فيزيائي سريع يبدأ عمدًا من منظور "اللولب العشوائي"، حيث تستكشف السلسلة جميع الثنيّات والالتواءات الممكنة دون تفضيل بنية معينة.
من التشابكات العشوائية إلى التجمعات الواقعية
أولًا، بنى الباحثون نموذجًا فيزيائيًا فعالًا يعيد إنتاج كيفية تصرف سلسلة بروتينية غير منظمة بالكامل، بناءً على إحصاءات مستخرجة من آلاف الهياكل البروتينية المعروفة. هذا النموذج يعمل كـ"مُرجِع"—التوقع الأساسي لكيفية تحرك البروتين غير المنظم إذا لم نعلم شيئًا آخر. بعد ذلك، يقرأ bAIes توقعات AlphaFold حول أزواج البقايا التي تميل إلى الاقتراب. بدلًا من إجبار البروتين على نمط واحد، يحوّل تلك التلميحات إلى قيود مسافة لطيفة ذات عدم يقين مدمج، مما يسمح للسلسلة بالامتثال لاقتراحات الذكاء الاصطناعي فقط عندما تتسق مع الصورة الفيزيائية الأوسع.
الاختبار مقابل التجارب الحقيقية
لمعرفة ما إذا كانت هذه النهج تعمل، طبّق الفريق bAIes على مجموعة مكوّنة من 21 بروتينًا تتراوح من سلاسل شبه عشوائية تمامًا إلى أنظمة أكثر تعقيدًا ذات حلقات مؤقتة ومجالات متعددة. لكل منها، قارنوا التجمعات المولّدة بالحاسوب مع مجموعة واسعة من القياسات التجريبية التي تستقصي تفاصيل محلية وكذلك الحجم والشكل الكلي. بالنسبة للبروتينات المرنة جدًا مثل الببتيد المرتبط بمرض ألزهايمر Aβ40، كان نموذج اللولب العشوائي البسيط قد اقترب بالفعل من الواقع، وحافظ bAIes على هذا التوافق الجيد. بالنسبة للبروتينات نصف المهيكلة، حسن bAIes المطابقة مع التجارب من خلال التقاطه الصحيح لمواقع ظهور واختفاء القطع الحلزونية القصيرة والبقع المدمجة. والأهم من ذلك، بقيت الطريقة متينة حتى عندما كان AlphaFold واثقًا بشكل مبالغ فيه وتنبأ خطأً بطيّات مستقرة حيث تُظهر تجارب المحلول عدم التنظيم، لأن bAIes يسمح صراحةً بوجود أخطاء في مدخلات الذكاء الاصطناعي.
التفوّق أو المضاهاة مع الطرق القائمة
بعد ذلك واجه المؤلفون bAIes بمحاكاة ذرية كاملة الثقيلة التي تُشغل على حواسيب متخصصة فائقة، ونماذج خشنّة متقدمة تبسط البروتينات إلى خرزات، ومولِّدات تعلم عميق جديدة مدرّبة على بيانات المحاكاة. عبر اختبارات متعددة، طابق bAIes باستمرار أو تفوّق على هذه الطرق في استنساخ البيانات التجريبية، مع كونه أقل تكلفة حسابيًا بكثير من المحاكاة الشاملة. كما عمل أيضًا إلى ما بعد بروتينات IDP البسيطة، متعاملًا مع بروتينات ذات عدة مجالات صلبة مرتبطة بواصلات مرنة واستعاده أشكالها العامة في المحلول. عندما قام الباحثون بمزيد من الضبط الدقيق لتجمعات bAIes باستخدام بيانات تجريبية، تحسّن التوافق أكثر، مما يدل على أن الطريقة يمكن أن تكون نقطة انطلاق قوية للنمذجة التكاملية.
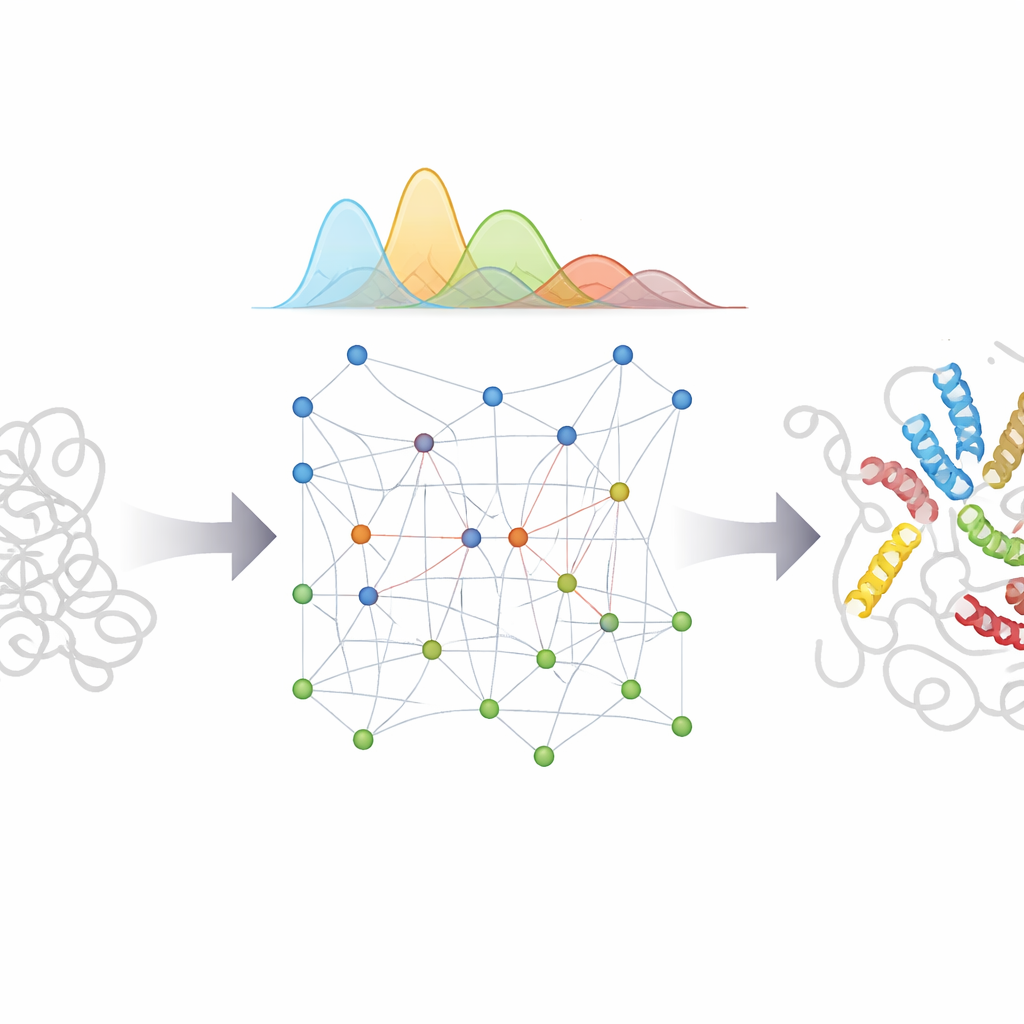
ما يعنيه هذا لأجل علم الأحياء والطب
بدمج قوة AlphaFold في تمييز الأنماط مع نموذج فيزيائي مصمم بعناية ومعالجة بايزية لعدم اليقين، يقدم bAIes مسارًا عمليًا نحو "أفلام" مفصّلة للبروتينات غير المنظمة بدلًا من لقطات ثابتة واحدة. يمكن أن تساعد هذه التجمعات ذات التفاصيل الذرية العلماء على فهم كيف تتعرف المناطق المرنة على شركاءها، وكيف تبدأ أخطاء الطي والتجميع في أمراض مثل باركنسون وألزهايمر، وكيف قد ترتبط جزيئات صغيرة بأهداف متقلبة ومراوغة. وبما أن الطريقة فعّالة ومضمّنة في برمجيات مفتوحة المصدر، فيمكن اعتمادها على نطاق واسع لتوليد تجمعات واقعية للعديد من البروتينات غير المنظمة، موجهةً التجارب وداعمةً أنظمة ذكاء اصطناعي مستقبلية تهدف إلى التنبؤ ليس بشكل واحد فحسب، بل بكامل نطاق الأشكال التي يمكن لجزيئات الحياة الأكثر مرونة أن تتبنّاها.
الاستشهاد: Schnapka, V., Morozova, T.I., Sen, S. et al. Atomic resolution ensembles of intrinsically disordered proteins with Alphafold. Nat Commun 17, 2399 (2026). https://doi.org/10.1038/s41467-026-69172-y
الكلمات المفتاحية: البروتينات غير المنظمة بطبيعتها, AlphaFold, النمذجة البايزية, تجمعات البروتين, علم الأحياء البنيوي