Clear Sky Science · ar
تأثير قوى المذيب والتماثل المكسور على تجمّع البروتينات المصمَّمة عند واجهة سائلة-صلبة
لماذا يهمّ هذا العالم الصغير على سطحٍ ما
من خلايا الطاقة الشمسية إلى أجهزة الاستشعار الطبية، ستعتمد العديد من التقنيات المستقبلية على بناء هياكل دقيقة حيث تلتقي الجزيئات البيولوجية بالمواد الصلبة. تدرس هذه الدراسة كيف تصطف "قضبان" بروتينية مصمَّمة خصيصًا على أسطح معدنية في ماء مالح. الدرس المفاجئ هو أن الماء الموجود مباشرةً عند السطح، واللا تماثلات الطفيفة في البلورة تحته، يمكن أن تغيّر تمامًا كيفية ترتيب هذه البروتينات—أحيانًا تنتج أنماطًا لا تتوقعها النظريات الكلاسيكية.
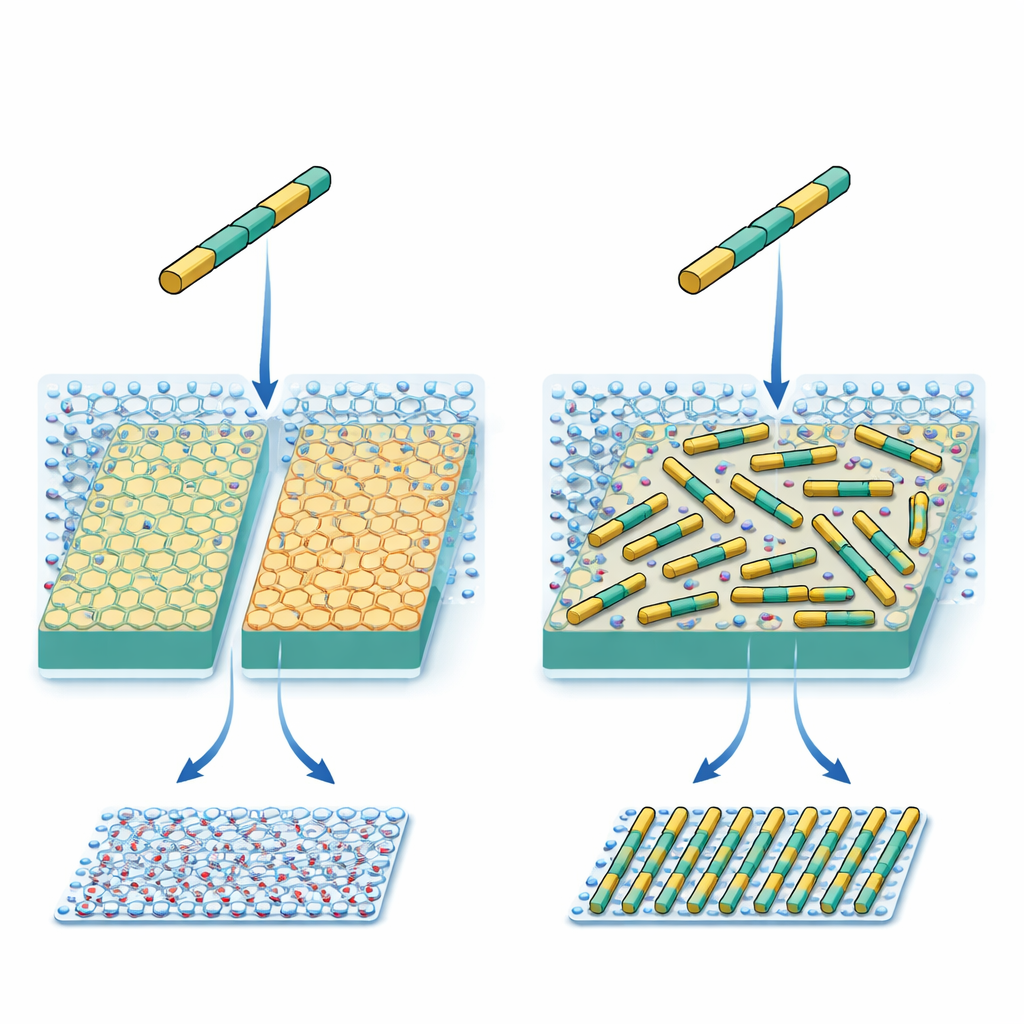
تصميم البروتينات لتتلاءم مع البلورة
عمل الباحثون مع بروتين صناعي على شكل قضيب قصير وقاسٍ. جرى تصميم كيمياء سطحه وتباعد مجموعاته المشحونة بعناية لتتوافق مع نمط أيونات البوتاسيوم على معدن شائع يُدعى الميكا. من الناحية المبدئية، كان من المتوقع أن يفضّل كل قضيب بروتيني ثلاثة اتجاهات مكافئة على سطح البلورة، مثل الاصطفاف على امتداد ثلاث أشعة لعجلة. أظهرت أعمال سابقة أن البروتينات، رغم هذا التصميم الدقيق، شكلت أنماطًا متعددة غير متوقعة بدلًا من النمط الواحد الذي صممه المهندسون. هذه التناقضات دلّت على أن هناك قوة مهمة مفقودة من قواعد التصميم الحالية.
سطحان شبه متطابقان، نتيجتان مختلفتان جدًا
لتتبع ما يجري، استخدم الفريق مجهر القوة الذرية عالي السرعة، الذي يمكنه مراقبة حركات وقِيام قضبان البروتين الفردية على السطح في الزمن الحقيقي. قاموا بمقارنة شكلين متقاربين من الميكا. كلاهما يعرِض شبكة بوتاسيوم مماثلة على السطح، لكن هياكلهما الذرية الداخلية تختلف قليلًا، وهو ما يغيّر بدوره كيفية تنظيم الماء في طبقات فوق السطح. عند مستويات ملح متواضعة، شكّلت القضبان سجادة كثيفة لكنها فوضوية محليًا على كلا السطحين، مع رقع صغيرة من الاصطفاف فقط. عندما زاد تركيز الملح إلى حدٍ عالٍ جدًا، انقسم السلوك: على نوع ميكا واحد بقيت القضبان غير مرتبة عبر الثلاثة اتجاهات، بينما على النوع الآخر تكونت تلقائيًا صفوف طويلة، متوازية، ومتباعدة بشكل منتظم عبر السطح كله.
طبقات الماء والتماثل المكسور
ساعدت نماذج الحاسوب للمعادن والماء المحيط على تفسير هذا الانقسام في السلوك. على شكل الميكا الأكثر تماثلًا، تحافظ الطبقة الأولى والثانية من جزيئات الماء على نمط سداسي منتظم. على الشكل الأقل تماثلًا، تكسر ذرات داخلية ومجموعات مدفونة داخل البلورة ذلك التماثل الثلاثي، وينتقل هذا النمط المكسور إلى طبقات الماء القريبة، فتتطوّر بها مناطق تشبه الشرائط. البروتينات لا تلامس البلورة الجرداء وحدها؛ بل تتفاعل أيضًا مع هذا الماء المنظم. نتيجةً لذلك، يصبح أحد اتجاهات القضبان مرغوبًا بعض الشيء أكثر من الاتجاهين الآخرين، رغم أن توافق البروتين مع البلورة المصمم كان يوحي بأن الثلاثة يجب أن تكون متساوية.
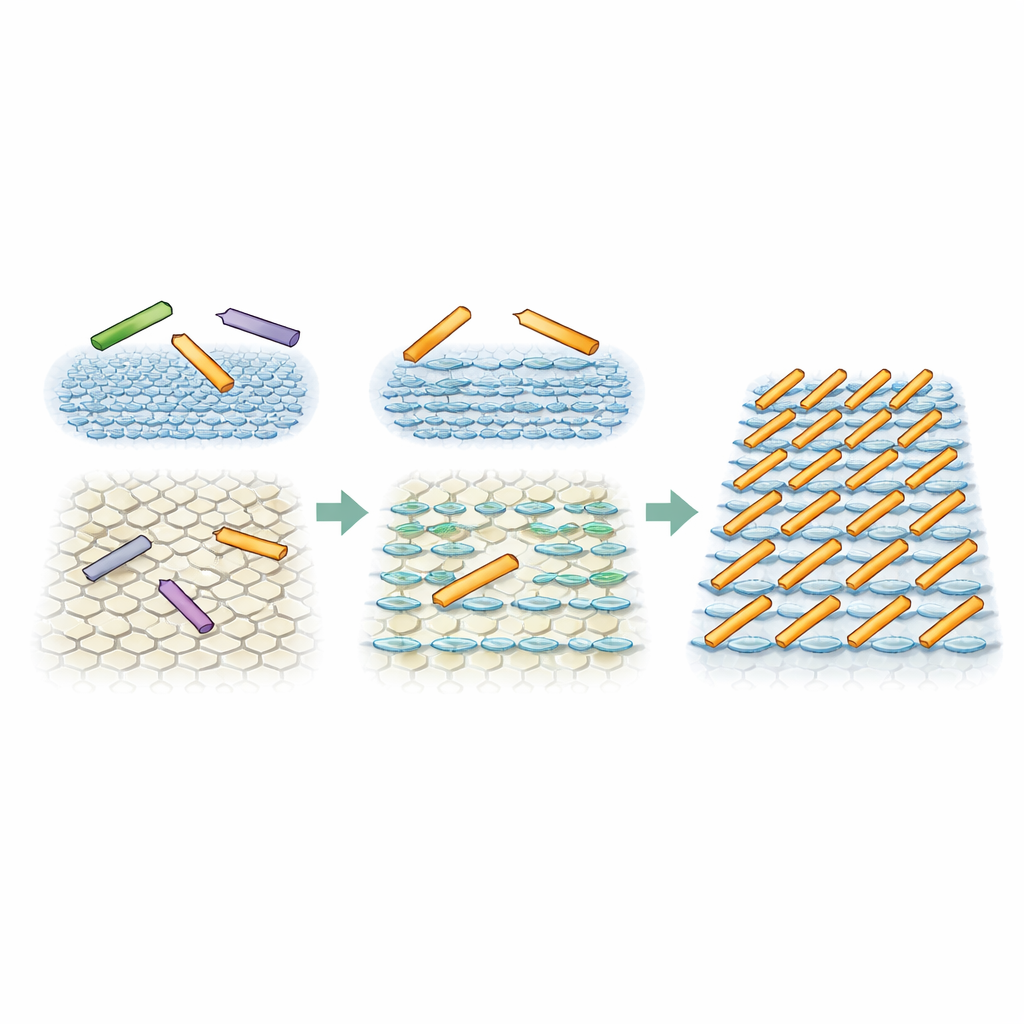
المحاكاة تكشف طورًا غير متوقع
لاختبار ما إذا كان التحيز الاتجاهي الطفيف من البيئة السطحية يمكن أن يفسر بالفعل الأنماط المرصودة، أجرى الباحثون محاكاة مونت كارلو لمستطيلات صلبة بسيطة تمثّل القضبان البروتينية. في مجموعة من المحاكاة، كانت الثلاثة اتجاهات متساوية الاحتمال، مقلدةً السطح المتماثل تمامًا. في تلك الحالة، بقيت القضبان في حالة كثيفة لكن مع فوضى، مع اصطفافات مؤقتة أو محدودة فقط، تمامًا كما شوهد على أحد أنواع الميكا. في مجموعة ثانية، جعلوا أحد الاتجاهات أكثر تفضيلًا بشكل طفيف—بنحو الضعف مقارنة بالاتجاهين الآخرين—كمحاكاة لتأثير طبقات الماء المخططة. في ظل هذه الظروف، وعندما كان بإمكان القضبان التحرك بما يكفي، تطورت المنظومة طبيعيًا إلى حالة بها صفوف متوازية ومتباعدة بانتظام. هذا ما يُسمّى طورًا سمكتياً، والنظرية السائدة تقول إنه لا ينبغي أن يظهر للأعمدة غير المتداخلة في بعدين، ومع ذلك جعل الدفع الاتجاهي الصغير من الواجهة هذا الطور مستقرًا.
إعادة التفكير في تصميم المواد المُستلهمة من الأحياء
باختصار، تُظهر هذه الدراسة أن كيمياء السطح المصممة بدقة مع البروتين ليست كافية للتنبؤ بكيفية ترتيب البروتينات المصممة على المواد الحقيقية. الماء الموجود بين البروتين والصلب، وطريقة كسر البلورة للتناظر بشكل دقيق، يمكن أن يوجها التجميع إلى أنماط لا تتوقعها نماذج الكتب الدراسية. من خلال الجمع بين المجهر عالي السرعة، والتعلّم الآلي لقياس الدرجة التنظيمية، والمحاكاة المبنية على الفيزياء، تحدد الدراسة طريقة لإدراج هذه التأثيرات الخفية للمذيب والتماثل في أدوات تصميم البروتين المستقبلية. للمهتمين بتصميم مواد هجينة بيولوجية-غير عضوية موثوقة، الرسالة واضحة: يجب أن تصمّموا ليس فقط للبروتين والسطح، بل أيضًا لطبقة الماء المنظمة التي تربط بينهما.
الاستشهاد: Yadav Schmid, S., Helfrecht, B., Stegmann, A. et al. Impact of solvent forces and broken symmetry on the assembly of designed proteins at a liquid-solid interface. Nat Commun 17, 2446 (2026). https://doi.org/10.1038/s41467-026-69170-0
الكلمات المفتاحية: التجمّع الذاتي للبروتين, واجهات سائلة-صلبة, بنية الماء البينية, ترتيب سمكتي, مواد مُستلهمة من الأحياء