Clear Sky Science · ar
آلية محول متعدد القيم تقود إدخال الأنزيمات المحلِّلة للبروتين إلى النواة
كيف تحافظ الخلايا على نظافة غرف التحكم لديها
داخل كل خلية تعمل النواة كمركز قيادة، محمَّلة بالحمض النووي والبروتينات التي تتحكم في تشغيل أو إطفاء الجينات. للحفاظ على فعالية هذا المركز، تعتمد الخلايا على "الممزقات" الجزيئية القوية المسماة بالمحللات البروتينية (بروتيازومات) التي تفكك البروتينات البالية أو المشوشة. تكشف هذه الورقة الطريقة التي تدير بها الخلايا مهمة سحب هذه المحللات الضخمة عبر البوابات الضيقة إلى داخل النواة في الوقت الملائم.
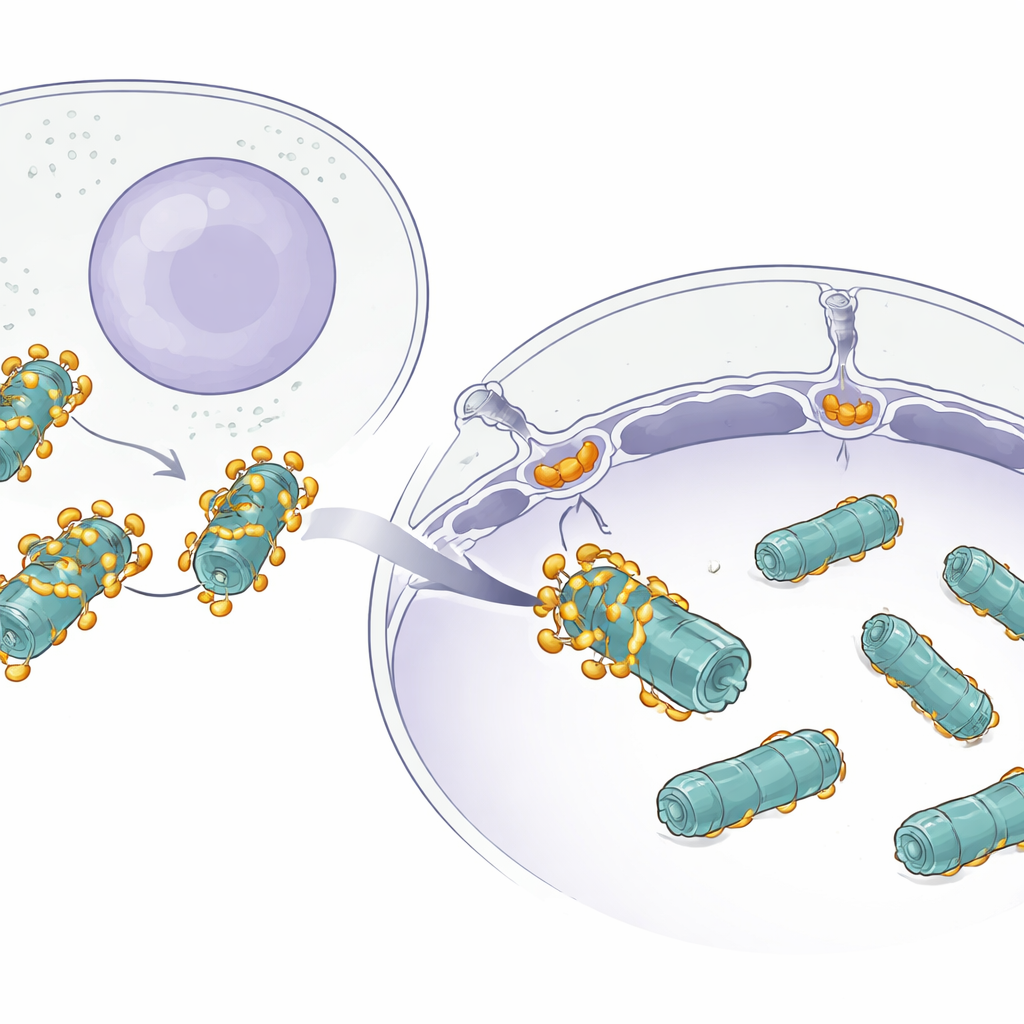
التحدي المتمثل في تحريك آلات كبيرة
العديد من البروتينات تنتقل بهدوء بين جسم الخلية والنواة عبر مداخل عملاقة في الغلاف النووي تُعرف بمسام النواة. يمكن للبروتينات الصغيرة المرور بسهولة، لكن الآلات الكبيرة مثل البروتيازوم مختلفة: إنها مجمعات ضخمة على شكل برميل مبنية من عدة أجزاء. بينما كان معروفًا أن الحمولات الصغيرة تستخدم بروتينات مساعدة تسمى الإمبورتينات لدخول النواة، ظلّ الأمر غير واضح كيف يمر شيء كبير بحجم البروتيازوم بكفاءة دون أن يعلق أو يضيع.
مساعد متحوّل الشكل يظهر بالوضوح
ركز الفريق على بروتين صغير ومرن يدعى AKIRIN2، والذي أظهرت أعمال سابقة أنه ضروري تمامًا لدخول البروتيازومات إلى النواة. الخلايا التي تنقسم بدون AKIRIN2 لا تستطيع إدخال البروتيازومات إلى النواة وتموت بسرعة لأن البروتينات النووية التالفة تتراكم. باستخدام مزيج من الأساليب ـ بما في ذلك مسح طفراتي واسع غيّر تقريبًا كل حمض أميني في AKIRIN2، والمجهر الإلكتروني بالتبريد عالي الدقة لرؤية المجمع ثلاثي الأبعاد، والاختبارات الكيميائية الحيوية الدقيقة ـ خرّج الباحثون الأجزاء المهمة في AKIRIN2 ووظائفها. اكتشفوا مقطعًا شبيهًا بـ"الجناح" ومنطقة لولبية تتيح لـAKIRIN2 تشكيل ثنائيات (أزواج)، وكلاهما يلعب دورًا رئيسيًا في إمساك البروتيازومات وشركائها.
بناء مقبض نقل متعدد الأيادي
كشفت الصور التركيبية أن نسخًا متعددة من AKIRIN2 تتجمع على جانب واحد من البروتيازوم كما لو كانت أيادي متعددة تمسك نفس الجسم. كل زوج من AKIRIN2 يرتبط بنقاط محددة على السطح الخارجي للبروتيازوم بينما يتفاعل أيضًا مع إمبورتينات مختلفة. أحد الإمبورتينات، IPO9، يمسك بـAKIRIN2 بطريقة غير عادية، يلتف حوله ويتغير شكله أثناء تجميع المركب. إمبورتينات أخرى، تعمل أيضًا كأزواج، تتعرف على إشارات دخول نووية قصيرة يحملها AKIRIN2. وبما أن عدة جزيئات AKIRIN2 تجلس على نفس البروتيازوم، فإنها تعرض معًا العديد من هذه الإشارات دفعة واحدة. هذا "المقبض" متعدد القيم يسمح لجموع الإمبورتينات بالالتصاق في آن واحد، مانحًا البروتيازوم الضخم قوة سحب كافية للتحرك عبر المسام النووية.
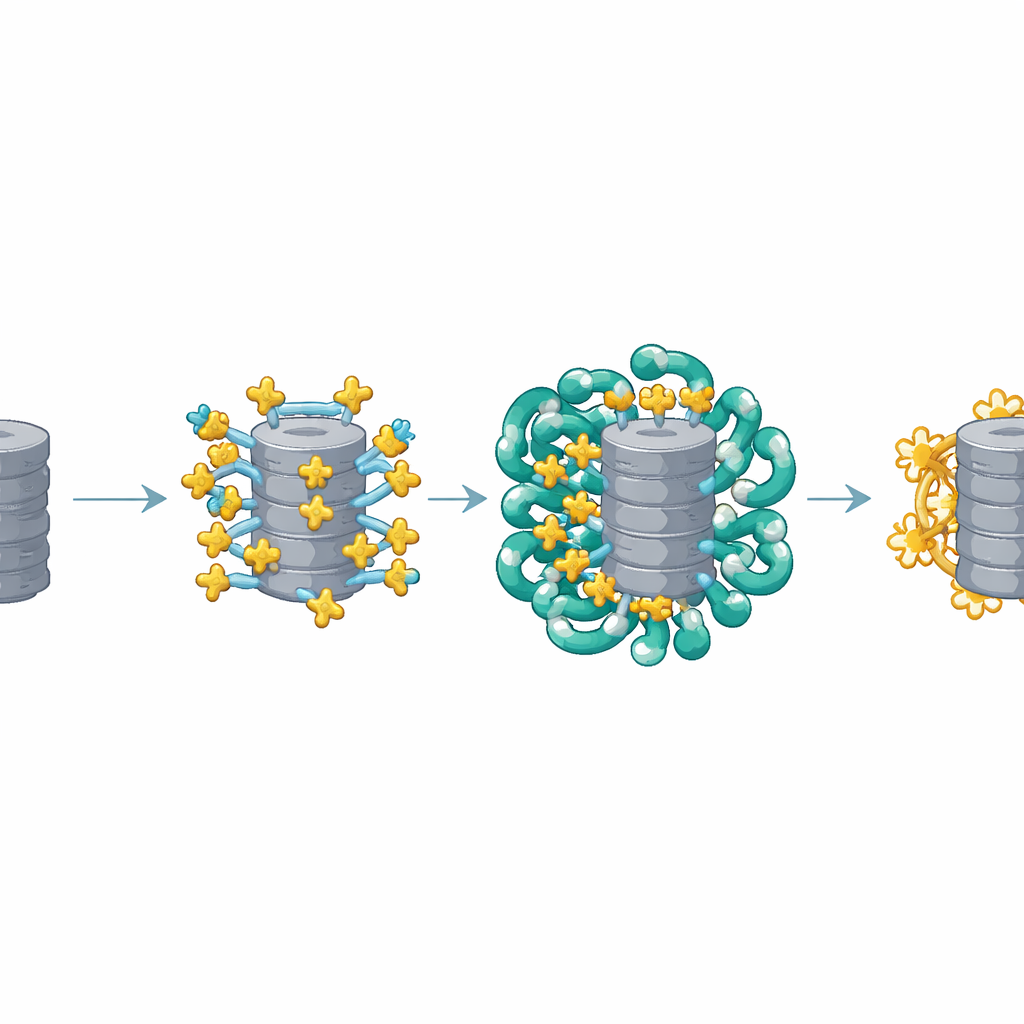
دورة تجميع وإطلاق ذكية
أظهرت تجارب إعادة التركيب في نظام مبسط داخل أنبوب اختبار أن البروتيازومات لا تدخل النوى بكفاءة إلا عند حضور كل من AKIRIN2 والإمبورتينات معًا. كلما زاد مقدار AKIRIN2، كانت عملية الإدخال أقوى وأسرع. بعد دخولها إلى النواة، يجب إزالة آلية النقل حتى تتمكن البروتيازومات من العمل. تستخدم الخلية هنا إطلاقًا ذا خطوتين. بروتين صغير مفتاحي يسمى Ran في صورته المرتبطة بـGTP يزيح معظم الإمبورتينات عن حمولتها. يظل AKIRIN2 وبعض IPO9 متمسكين بعناد أكبر، لكن للنواة حل احتياطي: تقوم البروتيازومات النووية مباشرةً بابتلاع AKIRIN2 نفسه، دون الوسم المعتاد باليوبيكويتين. تُظهر القياسات عبر دورة الخلية أن مستوى AKIRIN2 يبلغ ذروته أثناء انقسام الخلية عندما تتشكل نوى جديدة، ثم ينخفض في بداية الطور G1، ما يتوافق مع هذا التنظيف الموجَّه.
لماذا يهم هذا الأمر بخلاف بروتين واحد
مجتمعة، تُظهر هذه النتائج أن AKIRIN2 يعمل كهيكل مرن يجمع الكثير من الإمبورتينات على بروتيازوم واحد، محولًا مشكلة نقل صعبة إلى جهد جماعي منسق. من خلال تجميع إشارات الدخول النووية على محول بدلاً من البروتيازوم نفسه، يمكن للخلايا التحكم في توقيت وقوة دخول الآلات الكبيرة إلى النواة دون إعادة تصميم هذه الآلات. يبدو أن استراتيجيات مماثلة قائمة لمجاميع بروتينية كبيرة أخرى، وحتى الفيروسات تستغل حيلًا ذات صلة لغزو النواة. فهم هذا المنطق العام للنقل يعمّق صورتنا عن كيفية حفاظ الخلايا على توازن البروتين في أكثر مقصوراتها حساسية، وقد يشير في نهاية المطاف إلى طرق جديدة للتدخل عندما يختل تَحلِّي البروتين أو وظيفة النواة.
الاستشهاد: Brunner, H.L., Kalis, R.W., Grundmann, L. et al. A multivalent adaptor mechanism drives the nuclear import of proteasomes. Nat Commun 17, 2359 (2026). https://doi.org/10.1038/s41467-026-69162-0
الكلمات المفتاحية: النقل النووي, المحللات البروتينية (بروتيازوم), AKIRIN2, إمبورتين, تحلل البروتين