Clear Sky Science · ar
ألكينيلة وألكاينيلة انتقائية في المراحل المتأخرة عند N‑Me للأدوية والأمينات الثالثة غير المنشطة باستخدام التحفيز الضوئي-أكسدي
لماذا لا تزال إعادة تصميم الأدوية القديمة مهمة
تنجح العديد من الأدوية الحالية في علاج الأمراض، لكنها تترك مجالاً لتحسين السلامة، والآثار الجانبية، أو دقة استهدافها داخل الجسم. يزداد اهتمام الكيميائيين بإجراء «تعديلات طفيفة» على الأدوية الموجودة في المراحل المتأخرة من التطوير بدلاً من اختراع جزيئات جديدة من الصفر. تُظهر هذه الدراسة كيف يمكن لأشعة الضوء المرئي أن تُستخدم لإضافة أجزاء جديدة إلى نوع شائع من لبنات تركيب الأدوية، مولّدة مرشحين محسّنين مضادين للاكتئاب وشارِعةَ مسارٍ أسرع لتطوير علاجات مُنقّحة.
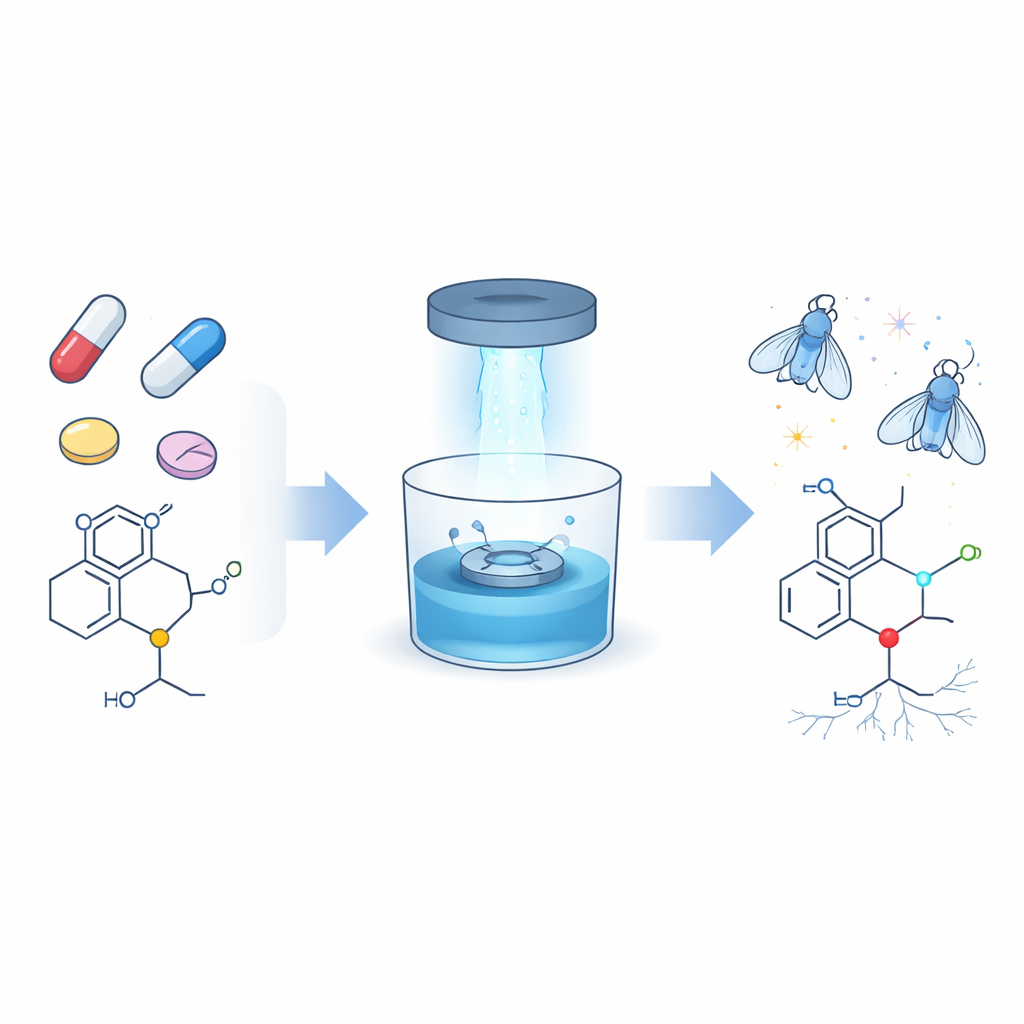
ترقية ميزة شائعة في كثير من الأدوية
جزء مفاجئ وكبير من الأدوية الحديثة—أكثر من اثنين من كل خمسة—يحتوي على شظايا غنية بالنيتروجين تُسمى الأمينات، ومعظمها من النمط الفرعي المعروف بالأمينات الثالثة. توجد هذه المجموعات في المضادات الحيوية، أدوية السرطان، أدوية الحساسية، المسكنات، ومضادات الاكتئاب. حتى الآن، واجه الكيميائيون صعوبة في تعديل جزء صغير واحد من هذه المجموعات بشكل انتقائي، وهو وحدة N‑methyl، عندما تكون محاطة بعدة روابط كربون–هيدروجين متشابهة تقريبًا. سعى المؤلفون إلى تطوير طريقة لطيفة وموثوقة لربط «مقابض» جديدة—تحديداً روابط كربون–كربون المزدوجة (ألكينات) والثلاثية (ألكاينات)—بتلك الموضعية N‑methyl دون الإخلال بباقي جزيء الدواء.
استخدام الضوء لإعادة توصيل رابطة واحدة في كل مرة
استعان الفريق بالتحفيز الضوئي-الأكسدي، وهي تقنية تستخدم الضوء المرئي ومحفزاً حساساً للضوء لتحريك إلكترونات مفردة وإثارة تفاعلات تحت شروط لطيفة. في نظامهم، يُثير الضوء الأزرق محفزاً عضوياً، فيؤدي ذلك مؤقتاً إلى سحب إلكترون من الأمين الثالثي. تخلق هذه الخطوة جذراً قصير العمر عند موضع N‑methyl يمكنه الارتباط بجزيئات شريكة مُختارة بعناية تحمل مجموعات فينيلية أو ألكاينية. من خلال ضبط شروط التفاعل—اختيار المذيب والقاعدة والإضافات—حقق الباحثون عوائد عالية وتحكماً ممتازاً، بحيث تستقر المجموعة الجديدة على موضع N‑methyl حصرياً تقريباً، حتى عندما تتواجد مواقع شبيهة متعددة. أظهروا ذلك على مجموعة واسعة من الأمينات البسيطة ثم على أدوية حقيقية، بما في ذلك مضادات الهيستامين، أدوية القلب، مضادات العدوى، والعديد من مضادات الاكتئاب.
من تعديل كيميائي إلى فعالية مضادة للاكتئاب أفضل
لاختبار ما إذا كانت هذه التعديلات البنيوية قد تؤثر طبياً، ركز المؤلفون على الإيميبرامين، مضاد اكتئاب ثلاثي الحلقات مستخدم منذ زمن طويل. صمموا ونمذجوا أكثر من عشرين متغيراً للإيميبرامين حيث حمل الامتداد الفينيل أو الألكاين حلقات عطرية يمكن أن تتناسب بشكل مريح داخل جيب هيدروفوبي من ناقل السيروتونين البشري، وهو بروتين يتحكم في مستويات المرسل المرتبط بالمزاج، السيروتونين. أشارت حسابات الاقتران الحاسوبي إلى أن العديد من هذه الجزيئات المعدلة ينبغي أن ترتبط بمثل أو أفضل من الدواء الأصلي. ثم تم تركيب أكثر المرشحين واعدة باستخدام الطريقة المدفوعة بالضوء واختبارها في أنظمة حية: نموذج ذبابة الفاكهة للاكتئاب المعتمد على العزلة الاجتماعية، ولأفضل مركبين في خلايا عصبية فأرية تنقل السيروتونين بنشاط.
كيف كشفت الذباب والخلايا عن أدوية أقوى
في ذباب الفاكهة الذكور المعزول، يظهر السلوك الشبيه بالاكتئاب على شكل عدوانية مرتفعة. يخفّض إطعام الإيميبرامين هذه العدوانية، ما يعكس تأثيره كمضاد للاكتئاب لدى البشر. بشكل لافت، قلّلت عدة مشتقات إيميبرامين الناتجة عن الطريقة الجديدة العدوانية بنفس القدر، وعملت أربعة مرشحين حتى أفضل من الإيميبرامين نفسه. في خلايا قرن آمون الفأرية المزروعة، حجب مركبان رائدان إعادة امتصاص السيروتونين أقوى من الإيميبرامين، كما تم تأكيد ذلك بقياسات كيميائية مباشرة للسيروتونين وبصبغة فلورية تضيء عند دخولها الخلايا. تشير هذه الاختبارات إلى أن تغييرات طفيفة في المرحلة المتأخرة عند موضع N‑methyl يمكن أن تعزز فعلياً قوة مضادات الاكتئاب بدلاً من أن تكون مجرد إعادة تشكيل على الورق.
لماذا يكون التفاعل انتقائياً جداً
كان سؤال علمي رئيسي هو لماذا يعديل التفاعل مجموعة N‑methyl بنقاوة عندما تبدو مواضع قريبة أخرى قابلة للتفاعل بالمثل. من خلال تجارب تحكم، وقياسات دوران الإلكترون، وحسابات حاسوبية مفصلة، أظهر المؤلفون أن نقطة القرار الحاسمة ليست عند تكوين الجذر الأولي، بل عند إضافة هذا الجذر إلى الشريك الفينيل أو الألكاين. المسار الذي يؤدي من جذر N‑methyl إلى المنتج النهائي هو أكثر سهولة من الناحية الطاقية وأسرع بكثير من المسارات المتنافسة، ما يوجه التفاعل عملياً نحو نتيجة واحدة. تساعد هذه البصيرة في تفسير الانتقائية العالية ويمكن أن تُرشد استراتيجيات مماثلة على جزيئات معقدة أخرى.
ماذا يعني هذا العمل للأدوية المستقبلية
بشكل عام، تقدم الدراسة طريقة عملية لتحديث الأدوية القائمة التي تحتوي على أمينات ثالثية بشكل جراحي، مضيفة مقابض كيميائية مدمجة يمكن أن تضبط كيفية تفاعلها مع الأهداف البيولوجية أو ربطها بمكونات أخرى. من خلال إظهار أن مثل هذه التعديلات في المراحل المتأخرة يمكن أن تحول مضاد اكتئاب معروف إلى متغيرات أكثر فعالية في نماذج حيوانية وخلوية بسيطة، يشير العمل إلى مزيج قوي من الكيمياء التركيبية الحديثة، والحوسبة، والبيولوجيا. ومع تطبيق هذا النهج على أدوية أخرى، قد يسرع صقل المرشحين الدوائيين ويساعد في تحديث العلاجات القديمة بأداء وسلامة محسّنين.
الاستشهاد: Paul, S., Mahato, S., Mahapatra, S.K. et al. Late-stage N-Me selective alkenylation and alkynylation of drugs and unactivated tertiary amines using photoredox catalysis. Nat Commun 17, 2695 (2026). https://doi.org/10.1038/s41467-026-69131-7
الكلمات المفتاحية: التحفيز الضوئي-أكسدي, التعديل في المراحل المتأخرة, الأمينات الثالثة, تصميم أدوية مضادة للاكتئاب, ناقِل السيروتونين