Clear Sky Science · ar
فوسفاألومينين(3) قابل للعزل قادر على تفعيل الجزيئات الصغيرة عبر أوضاع تفاعل فريدة
كسر الروابط القوية بأداة كيميائية جديدة
يسعى الكيميائيون دائماً لإيجاد طرق لإقناع الجزيئات العنيدة بالتفاعل. العديد من المواد الشائعة، من غاز الهيدروجين إلى ثاني أكسيد الكربون، ثابتة بشدة، مما يصعّب تحويلها إلى منتجات مفيدة. تُبلغ هذه الورقة عن جزيء مصمّم حديثاً مبني من الألومنيوم والفوسفور يمكنه الإمساك بهذه الشركاء المترددة وفتح روابطها. فهم والتحكّم في هذا النوع من تفعيل الروابط قد يساعد مستقبلاً على تحويل غازات النفايات إلى مواد أولية، أو يوفّر طرقاً ألطف وتوفيرية للمعادن لصنع المواد الكيميائية الدقيقة والمواد.
رابطة مصمّمة بين الألومنيوم والفوسفور
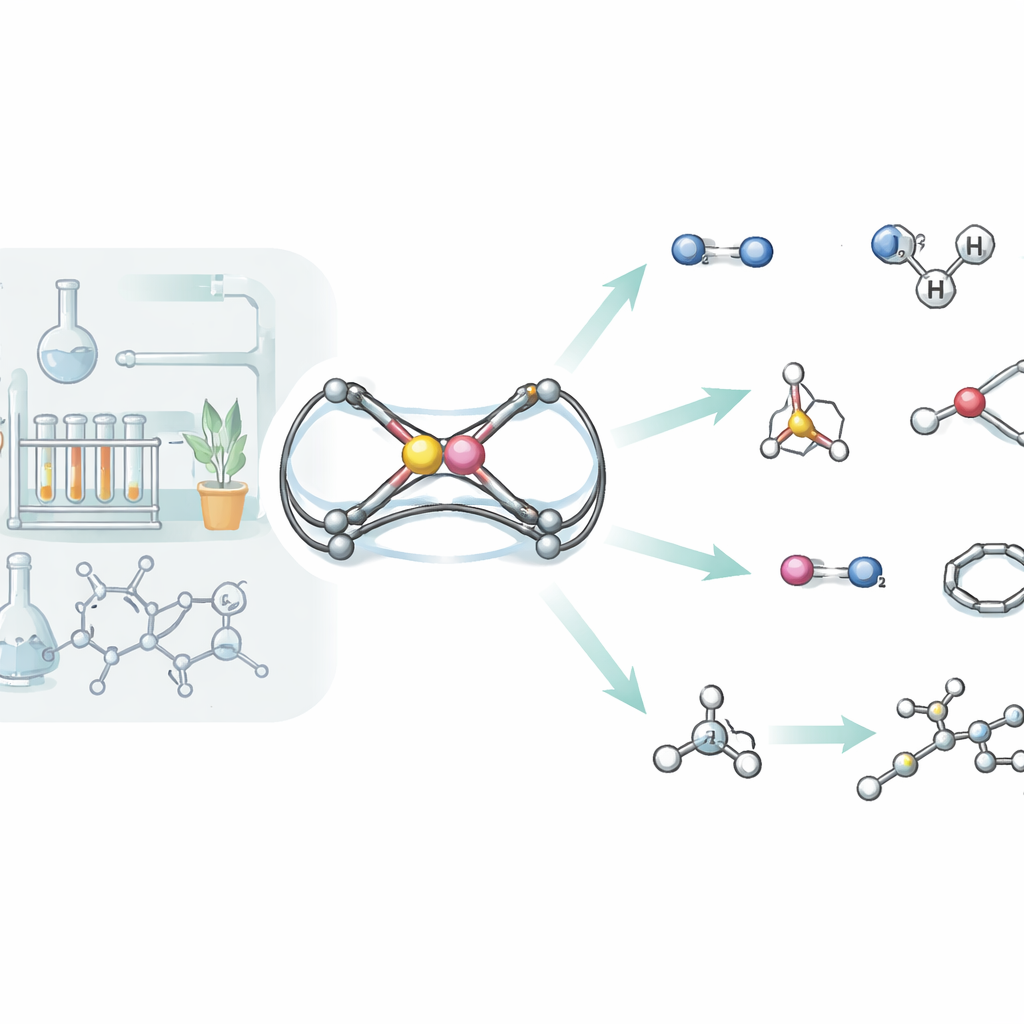
في صميم الدراسة توجد نوعية نادرة من الترابط بين عنصرين من مجموعات رئيسية: الألومنيوم والفوسفور. صنع الباحثون جزيئاً أطلقوا عليه اسم «3» في الورقة، حيث يتقاسم هذان الذرتان رابطة مزدوجة ضيقة. للحفاظ على هذا الثنائي التفاعلي من التفكك، غلّفوه بإطار عضوي ضخم يحميه من التفاعلات العرضية. ومن خلال مسارين تخليقيين مختلفين، حصلوا على هذا المعقّد بشكل قابل للعزل ونمّوا بلورات مفردة مناسبة لانحراف الأشعة السينية، مؤكّدين أن الفوسفور مرتبط بالألومنيوم برابطة قصيرة شبيهة بالرابطة المزدوجة بينما كل ذرة مدعومة بأربطة محيطة تحتوي نيتروجيناً. أظهرت الحسابات أن الإلكترونات موزعة بشكل غير متساوٍ بين الألومنيوم والفوسفور، مما يجعل الرابطة مستقطبة ومستعدة لهجوم جزيئات أخرى.
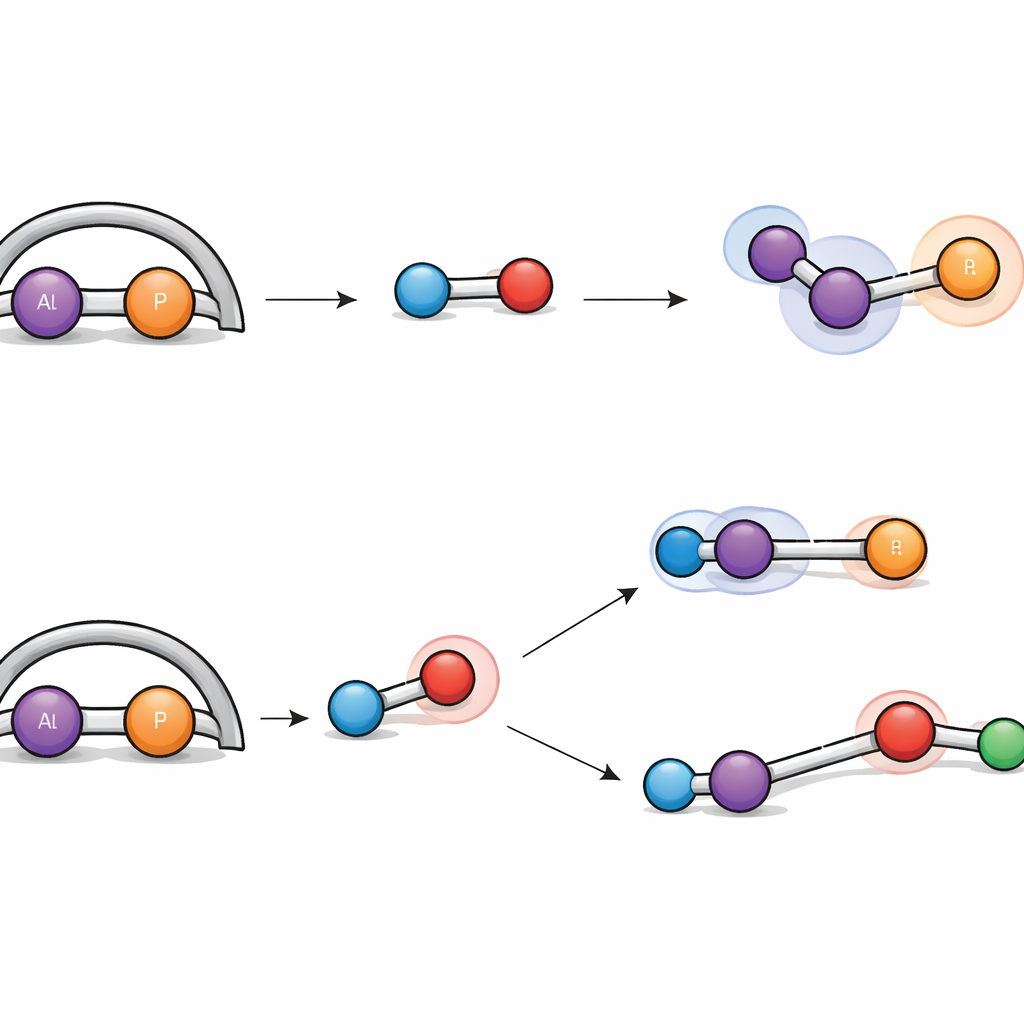
كيف يتعامل الجزيء الجديد مع غاز الهيدروجين
يُعرف عن غاز الهيدروجين أنه صعب الإنقسام دون استخدام معادن ثمينة، ومع ذلك يتمكن وحدة الألومنيوم–الفوسفور الجديدة من فعل ذلك. عند تعريض المعقّد للهيدروجين تحت ظروف لطيفة، يتفاعل بطريقتين متميزتين. في أحد المسارات، تُضاف رابطة H–H ببساطة عبر رابطة الألومنيوم–الفوسفور المزدوجة، فتتحول إلى رابطتين مفردتين وتلتصق ذرة هيدروجين بكل ذرة. في الأخرى، يُفصَل جزيء الهيدروجين بشكل تعاوني بواسطة الألومنيوم وذرة نيتروجين مجاورة، سلوك يذكّر بما يُسمى «أزواج لويس المحبطة» التي تفعل الهيدروجين دون محفزات معدنية تقليدية. تتبعت المحاكيات الحاسوبية التفصيلية كلا المسارين، مبينة أن حواجز الطاقة متقاربة، ما يفسّر تكوّن الناتجين جنباً إلى جنب.
تفكيك مجموعة من الجزيئات الصغيرة
الهيدروجين هو البداية فقط. اختبر الفريق بشكل منهجي كيف يتفاعل هيكل الألومنيوم–الفوسفور مع مجموعة واسعة من الجزيئات الصغيرة، بما في ذلك الفوسفور الأبيض، أيزوكيندا، ثاني أكسيد الكربون، أكسيد النيتروز، أزيد ثلاثي ميثيل السيليل، ثنائيات السيلينيوم، السيليانات، الأمينات، الستيرين، والألكاينات البسيطة. في العديد من هذه التفاعلات، تُكسر رابطة Al=P الأصلية تماماً، لتنتهي الذرتان في هياكل أقفاصية أو حلقية أكبر تدمج أجزاءً من الجزيء الداخل. على سبيل المثال، يُفكّك الفوسفور الأبيض (P4) ويعاد بناؤه إلى قفص ألومنيوم–فوسفور، بينما يدخل ثاني أكسيد الكربون مرتين لتكوين حلقة سداسية تربط الألومنيوم والفوسفور معاً عبر جسرين جديدين كربون–أكسجين. مع السيليانات والأمينات، يتصرف الجزيء بدلاً من ذلك بشكل أقرب إلى رابطة مزدوجة كلاسيكية: تُضاف وحدة Si–H أو N–H بطريقة منظمة عبر Al=P، مما يظهر مرة أخرى الطابع «π» لهذه الوصلة غير المألوفة.
لماذا يهم الإطار المحيط
واحدة من الدروس الرئيسة في العمل هي أن الإطار الضخم والغني بالنيتروجين حول وحدة Al=P ليس مجرد سقالة؛ بل يوجّه كيف وأين تحدث التفاعلات. بمقارنة نتائجهم مع أنظمة ألومنيوم–فوسفور أقدم وأقصر عمراً، يعرِض المؤلفون أن تغييرات طفيفة في اللِّيغانات الداعمة تقلب التوازن بين مسارات مختلفة، مثل الإضافة البسيطة عبر الرابطة المزدوجة مقابل التمزق الأكثر تعقيداً للروابط وتشكّل الحلقات. كشفت التحليلات المتقدمة لتوزيع الإلكترونات استقطاباً قوياً لرابطة Al=P وأبرزت كيف يمكن لذرات النيتروجين المجاورة أن تتعاون مع الألومنيوم، خاصة في تفعيل الهيدروجين. كما يدفع الحجم الفراغي—الازدحام الفيزيائي لمجموعات كبيرة—الجزيئات الداخلة نحو موقع تفاعلي معين أو آخر.
ماذا يعني هذا للكيمياء المستقبلية
قد تبدو سلسلة المواد المتخصصة في هذه الدراسة بعيدة عن غير المتخصص، لكن الرسالة الأساسية واضحة: من خلال ضبط الروابط والشكل حول عناصر المجموعة الرئيسية بعناية، يمكن للكيميائيين بناء أدوات رشيقة تضاهي أو تكمل المحفزات المعدنية التقليدية. هذا المعقّد القابل للعزل من الألومنيوم–الفوسفور لا ينجو فقط في زجاجة بل يتعامل أيضاً مع مجموعة واسعة من الجزيئات الصغيرة الصعبة تحت ظروف لطيفة، مفصلاً الهيدروجين، معيداً ترتيب الفوسفور الأبيض، وملتقطاً ثاني أكسيد الكربون. تُظهر الدراسة أن تغييرات طفيفة في «مقبض» الجزيء يمكن أن تعيد توجيه تفاعليته بشكل عميق، مما يقدّم مخططاً لتصميم محفزات مستقبلية تساعد في تحويل الجزيئات البسيطة والثابتة إلى منتجات أكثر قيمة بدقة وكفاءة.
الاستشهاد: Cha, Y., Yang, Z., Zhuang, X. et al. An isolable phosphaalumene(3) capable of small molecule activation via unique modes of reactivity. Nat Commun 17, 2390 (2026). https://doi.org/10.1038/s41467-026-69118-4
الكلمات المفتاحية: تفعيل الجزيئات الصغيرة, كيمياء المجموعة الرئيسية, رابطة مزدوجة الألومنيوم والفوسفور, زوج لويس المحبط, آليات تفعيل الروابط