Clear Sky Science · ar
آلية تثبيط سينثازات بيتا−1,3-غلوكان الفطرية بواسطة أدوية مضادة للفطريات من نوع التريتيربوينويد
لماذا يهم وقف العدوى الفطرية
تتسبب العدوى الفطرية بهدوء في مقتل أكثر من مليون شخص سنوياً وتهدد المحاصيل والنظم البيئية في جميع أنحاء العالم. الأطباء يعتمدون حالياً على مجموعة محدودة من الأدوية المضادة للفطريات، وبعض الفطريات الخطرة تتطور لتتفادى هذه الأدوية. يكشف هذا البحث، بتفاصيل جزيئية، كيف تتشبث فئة جديدة من الأدوية المضادة للفطريات بمحرّك أساسي تحتاجه الفطريات لبناء جدارها الخلوي الواقي وتُعطّله. فهم هذه العملية يوفر خارطة طريق لتصميم علاجات أفضل قادرة على التفوق على الفطريات المقاومة.
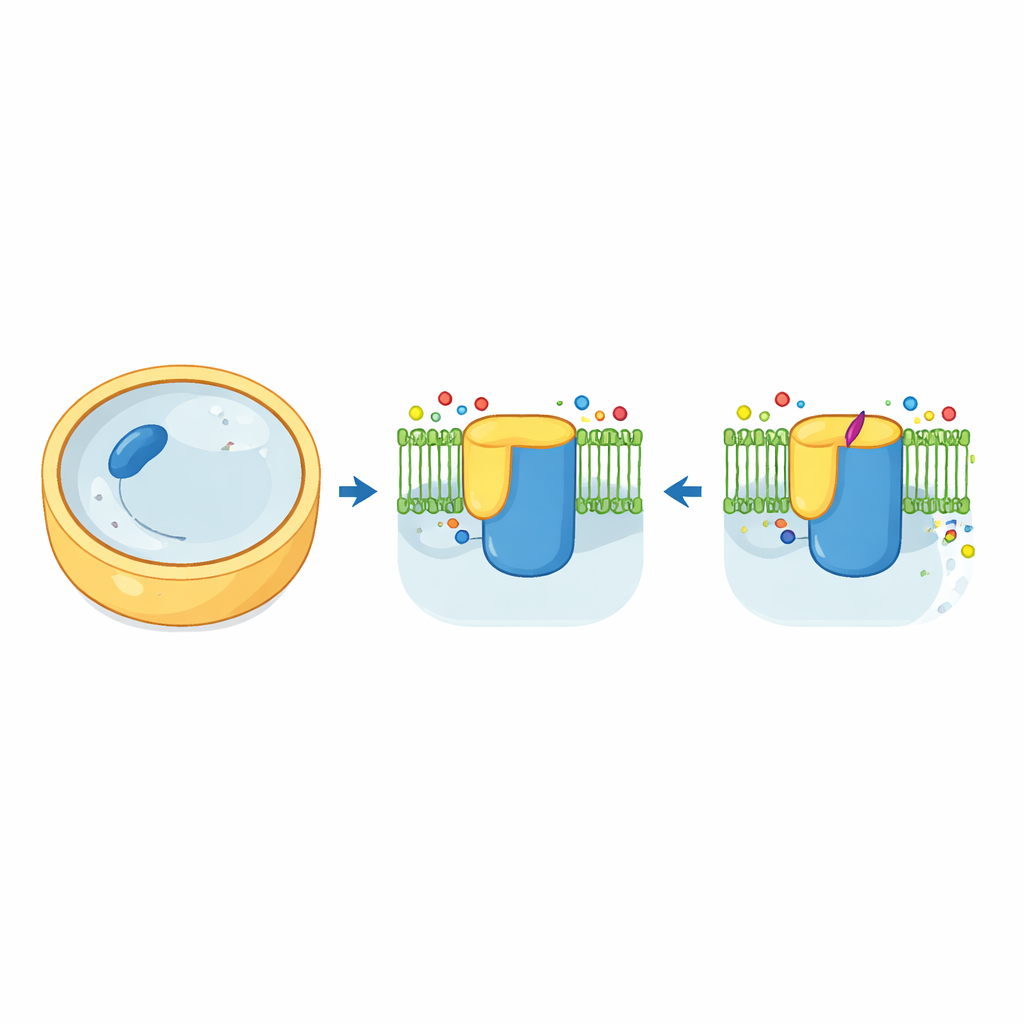
صانع الطوب في جدار الخلية الفطري
تُغلف الخلايا الفطرية بجدار صلب مكوَّن إلى حد كبير من بوليمر سكري يُدعى بيتا-1,3-غلوكان. يعمل الإنزيم الذي يصنع ويصدر هذا البوليمر، المعروف باسم بيتا-1,3-غلوكان سينثاز، كصانع طوب وحزام ناقل في آن واحد. في خميرة الخَبز، تُبنى هذه الآلة من نسختين متشابهتين جداً، Fks1 وFks2، كل واحدة مدموِجة في غشاء الخلية وتتحكم فيهما بروتين مساعد صغير يُسمى Rho1. باستخدام المجهر الإلكتروني بالتبريد، التقط المؤلفون صوراً ثلاثية الأبعاد عالية الدقة لكل من Fks1 وFks2 في حالتهما الطبيعية. تكشف البنى عن "منصة عمل" كبيرة في السيتوسول متصلة بغابة من الحلزونات العابرة للغشاء، مع تجويف مركزي من المحتمل أن يعمل كالنفق الذي يخرج عبره سلسلة الغلوكان النامية من الخلية.
كيف يمسك دواء طبيعي بالإنزيم
تنحدر الأدوية التريتيربوينويدية ذات الأهمية السريرية، بما في ذلك الدواء الفموي إيبريكسا فانغرب، من مركب طبيعي يدعى إنفيوما فنغين. حتى الآن، لم يكن معروفاً بالضبط أين ترتبط هذه الأدوية على سينثاز الغلوكان. حلّل الباحثون بنى كل من Fks1 وFks2 مرتبطة بالإنفيومافنغين. بشكل مفاجئ، لا يترسخ الدواء في الموقع الفعال حيث تُربط وحدات السكر. بدلاً من ذلك، يستقر على الجزء الخارجي لحلزون غشائي واحد يسمى TM5، جالساً داخل الغشاء على بعد نحو ثلاثة نانومترات من المركز التحفيزي وبالقرب من القناة المحتملة لخروج الغلوكان. تحضن أمينواسيدات رئيسية في هذه المنطقة قلب الدواء الكاره للماء وتتصل بذيله الحمضي، بينما يلامس ملحقه السكري البروتين بالكاد — ما يفسر لماذا تمكن الكيميائيون من تعديل هذا الجزء دون فقدان الفعالية.
أدوية تُجمد آلة متحركة
للوهلة الأولى، يبدو شكل الإنزيم إجمالاً مع الإنفيومافنغين وبدونه شبه دون تغيير. يكمن الفرق الحاسم في كيفية تنظيم الليبيدات المحيطة ومدى مرونة بعض الحلزونات. عند ارتباط الدواء، يدور جانب عطري قريب ليُقفل الإنفيومافنغين في موضعه ومع بقايا أخرى يثبت ليبيداً منظماً بجانب الدواء. تصبح ليبيدات إضافية شبيهة بالستيرول مصفوفة بدقة حول مجموعة من الحلزونات الأفقية التي تساعد في تحديد مسار تصدير الغلوكان. تعمل هذه الليبيدات كوتد ودعامات، مقفلة الحلزونات ومدخل القناة في ترتيب "أساسي" محدد. تُظهر الاختبارات الجينية أن تغيير العديد من نقاط التماس للدواء أو لهذه الستيرولات يضعف ارتباط الدواء أو يدمر وظيفة الإنزيم، وتطابق الطفرات في هذه المواقع طفرات المقاومة المعروفة في مسببات الأمراض البشرية والنباتية.
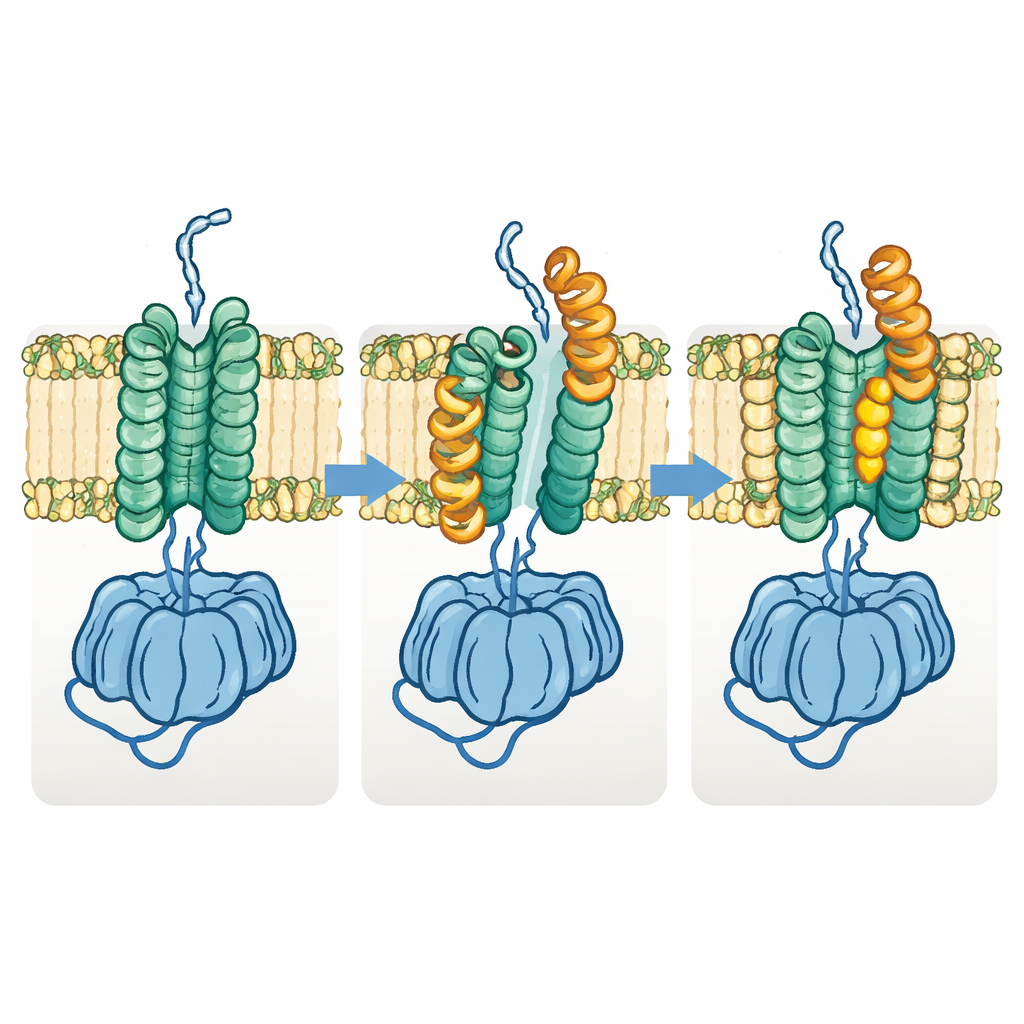
تحوّل شكلي ضروري لنقل البوليمر
اكتشف الفريق أيضاً شكلًا "مفتوحًا" مميّزًا لـFks1. في هذه الحالة، تتحرك نصف منطقة الغشاء جانبياً وتتأرجح الحلزونات الأفقية الرئيسية إلى الخارج، فتفتح المساحة بين حزمتَي الغشاء وتوسّع النفق الظاهر للغلوكان. يُشير مقارنة العديد من البنى إلى أن الإنزيم يدور بين الحالتين الأساسيتين خلال عمله الطبيعي: الحالة الأساسية تُهيئ وتُباشر تكوين البوليمر، بينما تسمح الحالة المفتوحة للسلسلة النامية بالتحرك جانبياً عبر الغشاء نحو الخارج. عندما صمّم المؤلفون روابط ديسلفيدية تقفل الإنزيم بشكل دائم في أي من الحالتين، فقدت النسختان الغالبية العظمى من نشاطهما، داعمةً فكرة أن هذا التحول الشكلي ضروري للوظيفة.
ما يعنيه هذا لأدوية مضادة للفطريات في المستقبل
بإظهار أن الإنفيومافنغين والأدوية ذات الصلة لا تعمل عن طريق حجب الجيب التحفيزي بل عن طريق إعادة تشكيل بيئة الغشاء المحلية وتجْميد سينثاز الغلوكان في حالته الأساسية، يكشف هذا البحث عن وضع غير تقليدي لآلية عمل الدواء. كما يُظهر أن Fks1 وFks2 يتشاركان بنُهج وباستجابات دوائية متطابقة تقريباً، مما يوضح لماذا يجب أخذ كلاهما بعين الاعتبار عند مواجهة المقاومة. وعلى نطاق أوسع، يبرز العمل كيف يمكن للجزيئات الصغيرة أن تتحكم في بروتينات غشائية "غير قابلة للدواء" عن طريق الارتباط بأسطح ضحلة وتجند الليبيدات، مقدماً مخططاً مفهوماً لتصميم جيل جديد من مضادات الفطريات التي تظل فعالة حتى مع تطور الفطريات.
الاستشهاد: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
الكلمات المفتاحية: الأدوية المضادة للفطريات, جدار الخلية الفطري, سينثاز الغلوكان, مقاومة الدواء, المجهر الإلكتروني بالتبريد