Clear Sky Science · ar
هياكل التبريد الإلكتروني لبكتيريوفاج T4 لوسائط وسط تركيب البوابة والرقبة تكشف آلية احتفاظ بالجينوم الفيروسي
كيف يحتفظ الفيروس بحمضه النووي تحت الضغط
بكتيريوفاج T4 هو فيروس يصيب بكتيريا الإشريكية القولونية ويضغط حمضه النووي بشدة داخل الرأس لدرجة أن الضغط الداخلي قد يكون أعلى بخمس إلى سبع مرات من داخل زجاجة шампан. ومع ذلك، لا يتسرب الحمض النووي بينما يكمل الفيروس بناء بقية جسده. تكشف هذه الدراسة، بتفصيل جزيئي، كيف يحل T4 هذه المشكلة باستخدام بوابتين صغيرتين تعملان كغرفة ضغط لمادته الوراثية.
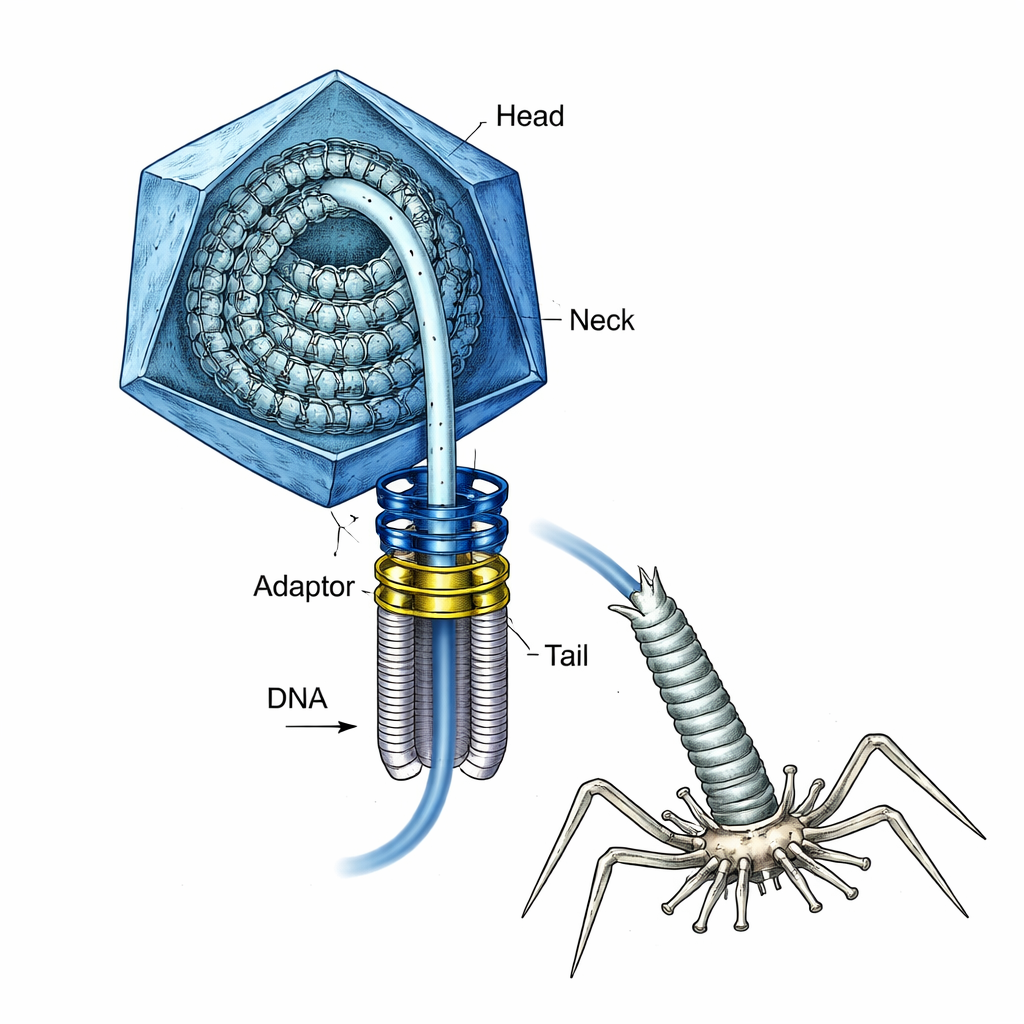
الفيروس الذي بداخله نابض مشدود
لطالما كان T4 أداة أساسية في علم الأحياء الجزيئي، كما أنه نموذج لبناء لقاحات وأدوات توصيل جيني مستقبلية. أثناء التجميع، يبني الفيروس أولاً غلافًا بروتينيًا فارغًا أو رأسًا، وبوابة حلقية خاصة عند زاوية واحدة. ثم يعمل محرك جزيئي قوي على سحب الحمض النووي إلى الداخل عبر هذه البوابة حتى يمتلئ الرأس. عند تلك النقطة، يجب أن ينفصل المحرك، وأن تُربط الرقبة والذيل، ولاحقًا يجب حقن الحمض النووي في بكتيريا—كل ذلك دون السماح بتفريغ الحمض النووي المضغوط مسبقًا. لم تكن الآلية التي يحتفظ بها الفيروس بهذا الحمض النووي شديد الضغوط خلال تلك الانتقالات مفهومة جيدًا.
إعادة بناء الرقبة في المختبر
أعاد الباحثون تكوين قطع أساسية من T4 في بكتيريا وخلطوها بطرق محكومة لمراقبة كيف يتجمع العنق—الموصل بين الرأس والذيل. تم إنتاج بروتينين فيروسيين يسمى كل منهما gp13 وgp14 بشكل منفصل. وحدهما كانا يعومان كوحدات مفردة، لكن معًا انطبقا إلى حلقات مكدسة تشكل قناة مركزية لمرور الحمض النووي. ولدهشة العلماء، كان بروتين ثالث يظهر باستمرار في هذه التحضيرات: Hfq، بروتين بكتيري معروف عادةً بمساعدته في التحكم بالرنا والنشاط الجيني في الإشريكية القولونية. وأكدت قياسات الطيف الكتلي أن Hfq يرتبط تحديدًا بـ gp14، مما يوحي بأن الفيروس يستعير هذا البروتين المضيف كجزء من رقبته.
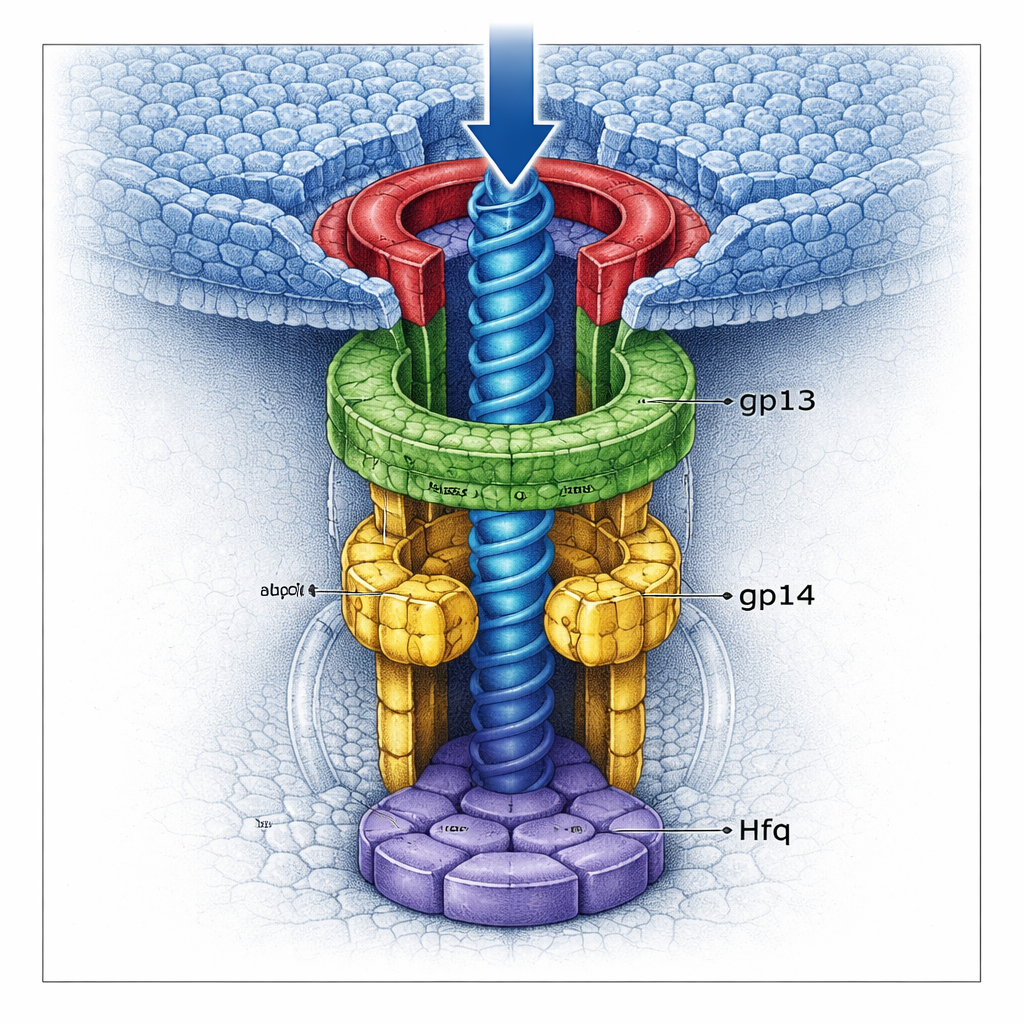
بوابتان تقفلان الجينوم
باستخدام مجهر إلكتروني بالتبريد عالي الدقة، صور الفريق عدة نسخ من معقد الرقبة بتفاصيل شبه ذرية. وجدوا أن gp13 يشكل حلقة عريضة تتكيف مع البوابة، بينما يجلس gp14 تحتها كسداسي، مكوّنًا قناة أضيق. والأهم أن كل وحدة من وحدات gp14 تسهم بحلقة طويلة تتأرجح نحو منتصف النفق. معًا تشكل ست من هذه «حلقات الإيقاف» بوابة محكمة يمكنها الإمساك بالمقطع الأخير من الحمض النووي عندما يحاول الخروج من الرأس. تحت gp14، يتجمع بروتين Hfq المُستعار إلى سداسي خاص به، يسد قاع القناة كباب ثانٍ. عندما يكون Hfq حاضرًا، يكون تركيب gp13–gp14 أكثر اكتمالًا وصلابة، وتُضيّق البوابات المجمعة القناة أكثر، مما يجعل تسرب الحمض النووي أقل احتمالًا بكثير.
التوقيت، مقاومة الأخطاء، ومساعد مستعار
تظهر الدراسة أيضًا أن هذا النظام أكثر من مجرد سدادة ثابتة؛ إنه تسلسل من التغيّرات المترابطة في الشكل. بمجرد أن يمتلئ الرأس، يدفع الضغط الداخلي البوابة نحو تباين تكويني يكشف مواقع ارتباط لـ gp13. ثم ترسو رقبة مُجمعة مسبقًا من gp13–gp14–Hfq على البوابة. ينثني gp13، يتأرجح إلى الأعلى، ويقفل على كل من البوابة والغطاء الخارجي، ناسجًا الرقبة بقوة في الرأس. خلال هذه المرحلة، تحافظ حلقات إيقاف gp14 وسدادة Hfq على الحمض النووي في مكانه. يلعب Hfq دورًا ثانيًا كعامل مراقبة جودة: عبر احتلاله الأسطح الرئيسية على gp14، يمنع gp14 من الارتباط بالبوابة في الموضع الخطأ، والذي قد يؤدي إلى تجميع خاطئ للرقبة. لا يحدث إزاحة Hfq وفتح الطريق لإطلاق الحمض النووي المسيطر إلا عندما يصل الذيل المُبني مسبقًا وتكوّن بروتين طرف الذيل gp15 رابطة أقوى مع gp14، طاردًا Hfq.
لماذا يهم هذا الأمر أبعد من فيروس واحد
بعبارات بسيطة، يستخدم T4 قفلًا ذا بابين لإبقاء نابض حمض نووي قوي مضغوطًا بينما يكمل بناء بقية الفيروس. الباب الأول مبني من بروتين الرقبة الخاص به gp14، والباب الثاني مستعار من بروتين المضيف Hfq، الذي يستخدمه الفيروس مؤقتًا ثم يتخلى عنه. تضمن هذه البوابة المزدوجة أن لا يفقد تقريبًا أي حمض نووي وأن يكون الفيروس النهائي مُعدًا للعدوى. وبما أن العديد من الفيروسات الكبيرة تضغط جينوماتها تحت ضغوط متطابقة وتشارك بنية ذات صلة، تشير هذه النتائج إلى أن أنظمة بوّابات مماثلة، وحتى الاستيلاء المؤقت على بروتينات العائل، قد تكون منتشرة على نطاق واسع. قد يوجّه فهم هذه الآليات تصميم ناقلات فيروسية أكثر أمانًا للطب ويشير إلى طرق جديدة لعرقلة الفيروسات الضارة عبر استهداف «أقفال» جينوماتها.
الاستشهاد: Han, L., Mao, Q., Zhu, J. et al. Cryo-EM structures of bacteriophage T4 portal-neck assembly intermediates reveal a viral genome retention mechanism. Nat Commun 17, 1964 (2026). https://doi.org/10.1038/s41467-026-69107-7
الكلمات المفتاحية: بكتيريوفاج T4, تجميع فيروسي, مجهر إلكتروني بالتبريد, تغليف الجينوم, تفاعل العائل–الفيروس