Clear Sky Science · ar
استراتيجية تركيبية توافقيّة لتطوير عوامل توصيل بروتينات تعديل الجينوم تستهدف شبكية الفأر
أمل جديد لعلاج العمى الوراثي
تبدأ العديد من أشكال العمى الوراثي بخلل في جين واحد داخل الخلايا الحسّاسة للضوء في الجزء الخلفي من العين. يمكن لأدوات تعديل الجينات الحديثة مثل CRISPR، من حيث المبدأ، تصحيح هذه الأخطاء، لكن إيصال آليات التعديل بأمان إلى الخلايا المستهدفة كان عقبة كبيرة. تصف هذه الدراسة طريقة جديدة لنقل محرّرات الجينات القوية مباشرة إلى شبكية الفأر باستخدام جسيمات شبيهة بالدهون مصممة خصيصًا، مما يفتح إمكانية علاجات لمرة واحدة تستعيد البصر لدى الأشخاص المصابين بأمراض وراثية في العين.
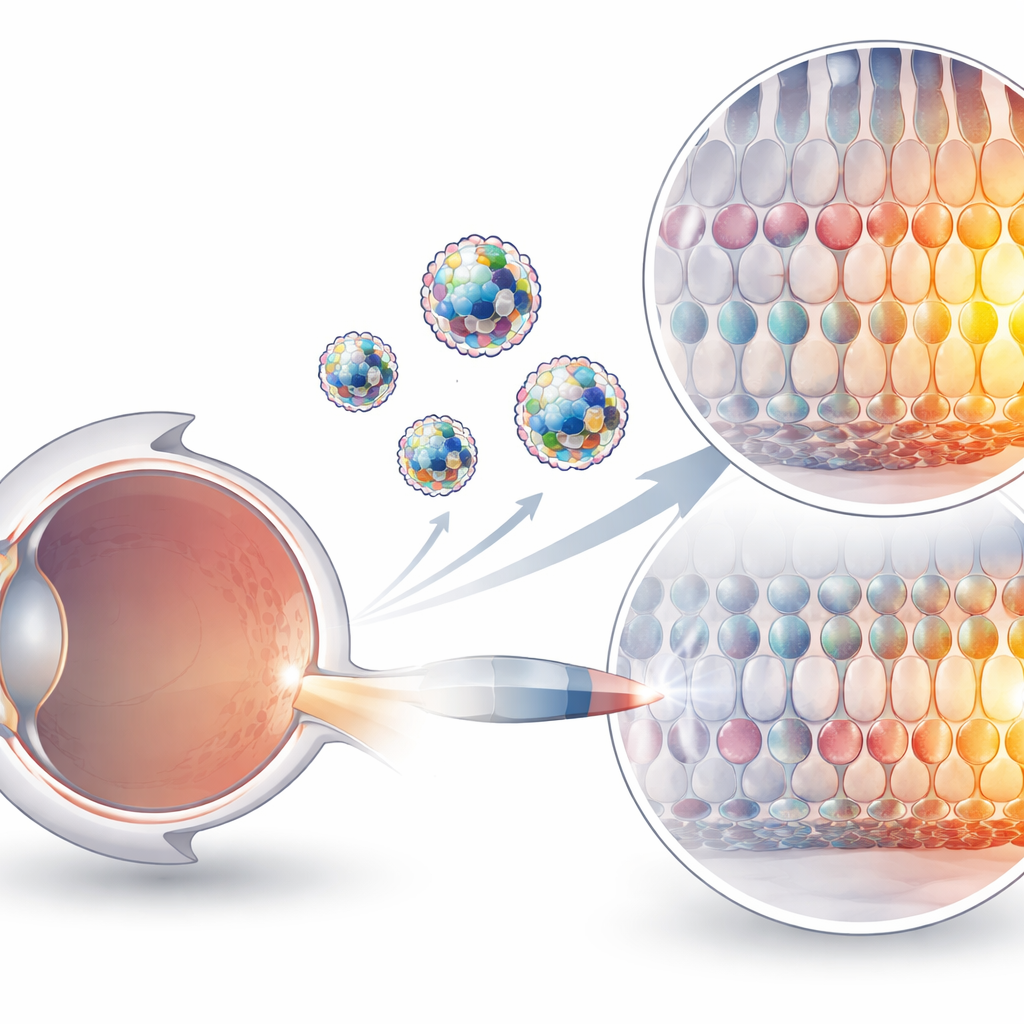
لماذا من الصعب توصيل محرّرات الجينات
يمكن الآن لأدوات معتمدة على CRISPR تغيير حروف مفردة في الـDNA دون قطع كلا الشريطين، وهو تقدم يجعلها جذابة لعلاج اضطرابات وراثية. لكن هذه الأدوات عبارة عن آلات بروتينية–RNA ضخمة، مشحونة كهربائيًا وهشة في الجسم. تعتمد طرق التوصيل الحالية إلى حد كبير على فيروسات معدّلة أو على جسيمات تنقل المخططات الوراثية للمحرّر بدلاً من نقل المحرّر نفسه. قد تثير الفيروسات تفاعلات مناعية ولها حدود صارمة للحجم، بينما يعمل توصيل الحمض النووي المرسال جيدًا في الكبد لكنه يظل غير فعال في أنسجة أخرى كثيرة، بما في ذلك العين. الحقن المباشر للمركبات البروتينية–RNA الجاهزة يعد فكرة أنظف وأكثر أمانًا، لكن هذه المركبات افتقرت إلى ناقل مناسب يساعدها على عبور أغشية الخلايا والوصول إلى أهدافها.
ناقلة مستوحاة من صبغة
لجأ الباحثون إلى نقطة انطلاق غير متوقعة: صبغة Coomassie Brilliant Blue، وهي صبغة زرقاء داكنة تُستخدم كثيرًا في مختبرات الأحياء وموافَق عليها بالفعل لبعض عمليات العين. ترتبط هذه الصبغة بقوة بالعديد من البروتينات المختلفة. قام الفريق بربط رؤوس Coomassie كيميائيًا بـ"ذيول" شبيهة بالدهون لابتكار عائلة من الجزيئات الجديدة تسمى ليبيدويدات. في الماء، تميل هذه الليبيدويدات إلى التجمع في جسيمات، حيث تُدفن الأجزاء الزيتية في الداخل وتبقى مجموعات Coomassie مكشوفة من الخارج بحيث يمكنها الالتصاق بالبروتينات. من خلال تغيير طول وتفرع وشحنة الذيول، بنى العلماء عشرات المركبات المرشحة المصممة لربط بروتينات تحرير الجينات من جهة والتفاعل مع أغشية الخلايا من الجهة الأخرى.
اختبار توصيل البروتين إلى خلايا العين
لمعرفة أي التصاميم تعمل بالفعل، استخدم الفريق أولاً بروتين اختبار بسيط يدعى Cre recombinase الذي يبدّل مفتاحًا جينيًا من الفلورة الخضراء إلى الحمراء أو العكس في خلايا وفئران مهندَسة وراثيًا. حملت عدة ليبيدويدات Coomassie بروتين Cre بكفاءة إلى خلايا مزروعة، محولة نسبًا كبيرة من الخلايا من الأخضر إلى الأحمر. عند حقنها تحت شبكية فئران تقريرية، أطلقت مركبات مختارة تغييرات لونية بارزة في كل من الطبقة الصبغية الداعمة للرؤية والـphotoreceptors الحساسة للضوء، مما يدل على أن البروتينات وصلت إلى الخلايا التي تتأثر في كثير من أمراض العمى الوراثي. كشفت هذه التجارب المبكرة أيضًا أن تغييرات طفيفة في بنية الليبيدويد قد تغيّر أنواع الخلايا المستهدفة، مما يوحي بأنه يمكن ضبط الإصدارات المستقبلية لتستهدف طبقات شبكية معينة.
تعزيز التحرير الجيني وإنقاذ الرؤية
بعد ذلك، حمل الفريق نظامه بمحرّر أساس أدينين، وهو نسخة محسّنة من CRISPR قادرة على تصحيح الطفرة المفردة المسببة لفقدان البصر في فئران rd12، نموذج لعمى طفولي شديد. وحدها، كانت مركبات البروتين–RNA للمحرّر تخترق الخلايا بشكل ضعيف. حسّن أحد الليبيدويدات، المسمى CBB11، عملية التوصيل لكنه كان يميل إلى التماسخ في المحلول. لاستقراره، دمج الباحثون CBB11 داخل ليبوزومات صغيرة ومحددة جيدًا—كرات مجوفة مصنوعة من عدة أنواع من الدهون، تشمل مكونات مستخدمة سريريًا في لقاحات mRNA. في هذه التركيبات، أمسك CBB11 على سطح الليبوزوم بجزء البروتين للمحرّر، بينما ساعدت دهون أخرى في ربط دليل الـRNA، فخلقت غلافًا تعاونيًا يمسك المركب بكامله على سطح الجسيم.
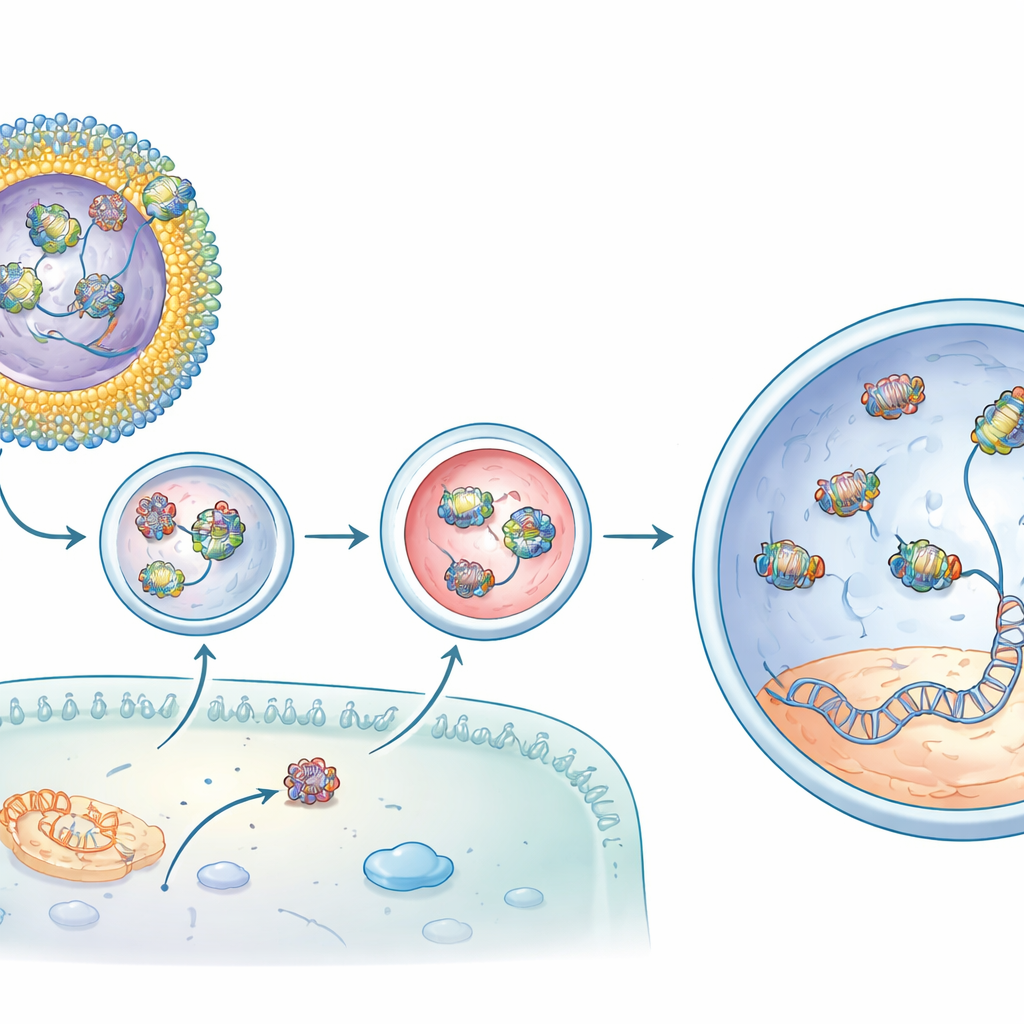
من الإصلاح الجزيئي إلى استعادة الاستجابة للضوء
عند حقن هذه الليبوزومات المحتوية على CBB11 الحاملة لمحرّر الأساس تحت شبكية فئران rd12، كانت النتائج لافتة. بالمقارنة مع المحرّر المحقون بمفرده، زادت التركيبة المحسّنة التصحيح المطلوب في الـDNA في الجين المستهدف بأكثر من رتبة واحدة من الحجم وأنتجت مستويات أعلى حتى من الـmRNA المصحح. أظهر التحليل الكيميائي استعادة الصبغة الشبكية الحساسة للضوء المفقودة في المرض. والأهم من ذلك، كشفت تسجيلات كهربائية من عيون الحيوانات أن خلايا القضيب (rod cells) استعادت كثيرًا من قدرتها على الاستجابة للضوء الخافت—حتى نحو ثلاثة أرباع إشارة فأر طبيعي في أفضل الحالات. كانت التغيرات غير المستهدفة في أماكن أخرى من الجينوم عند مستويات الخلفية، ما يشير إلى أن التحرير كان قويًا ودقيقًا في آن واحد.
ما الذي قد يعنيه هذا للعلاجات العينية في المستقبل
لغير المتخصصين، الرسالة الأساسية هي أن المؤلفين بنوا "حافلة ناقلة" قابلة لإعادة الاستخدام لمحرّرات البروتينات تعمل مباشرة في العين الحية. من خلال تزيين جسيمات دهنية آمنة تشبه تلك المستخدمة في اللقاحات بصبغة تلتقط البروتين، أنشأوا نظامًا يمكنه الإمساك بمحرّرات مختلفة على سطحه، توصيلها إلى خلايا الشبكية، تصحيح الطفرات المسببة للأمراض، واستعادة الرؤية بشكل ملحوظ في الفئران بعد علاج واحد. على الرغم من الحاجة إلى مزيد من العمل لتقييم السلامة بالكامل، تحسين الاستهداف، وتكييف الطريقة للاستخدام البشري، تشير هذه المنصة إلى أدوية مستقبلية دقيقة لمرة واحدة لأمراض الشبكية الوراثية وربما لحالات وراثية أخرى حيث يمكن لإصلاح الحمض النووي الموضعي والمدروس أن يحدث الفرق بين العمى والبصر.
الاستشهاد: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
الكلمات المفتاحية: علاج الجينات الشبكي, تحرير قواعد CRISPR, ليبوزومات, توصيل البروتين, العمى الوراثي