Clear Sky Science · ar
رؤى حول بنية وتعديل قناة TWIK-2 البشرية
لماذا تهم هذه البوابة الصغيرة في خلايانا
في أعماق خلايانا، تتحكم بوابات دقيقة من البروتين بتدفق الذرات المشحونة، مما يشكل كيفية إطلاق العصبونات للنبضات، وكيفية تقلص الأوعية الدموية، وكيفية استجابة جهاز المناعة. إحدى هذه البوابات، المسماة TWIK-2، رُبطت بارتفاع ضغط الدم الرئوي والالتهاب الضار، لكن حتى الآن كان العلماء يملكون معرفة ضئيلة حول تركيبها أو كيفية التحكم بها بالأدوية. تكشف هذه الدراسة البنية التفصيلية لـ TWIK-2 البشرية، تعرض سلوكها الكهربائي، وتحدد كيف يمكن استهدافها لتطوير أدوية مضادة للالتهاب.
قناة هادئة ذات تبعات صحية كبيرة
تنتمي TWIK-2 إلى عائلة كبيرة من قنوات البوتاسيوم «التسريبية» التي تساعد على تعيين الجهد الساكن للخلايا عبر السماح لأيونات البوتاسيوم بالعبور عبر غشاء الخلية. بينما دُرست أعضاء أخرى من هذه العائلة، مثل قنوات TREK وTASK، بكثافة وربطت بالألم والمزاج، بقيت TWIK-2 غير معروفة لأنها صعبة التسجيل وتعبّر بمستويات منخفضة في أنظمة المختبر القياسية. ومع ذلك، ربطت دراسات على الحيوانات والخلايا TWIK-2 بارتفاع ضغط الدم الرئوي، وإصابة الرئة الحادة، وفقدان السمع، وتنشيط مجمّع مناعي يُدعى NLRP3 inflammasome، الذي يسبب التهابًا ضارًا في الإنتان وأمراض أخرى. لذا فإن فهم كيفية عمل TWIK-2 ضروري لكل من البيولوجيا الأساسية وتصميم علاجات مستهدفة.
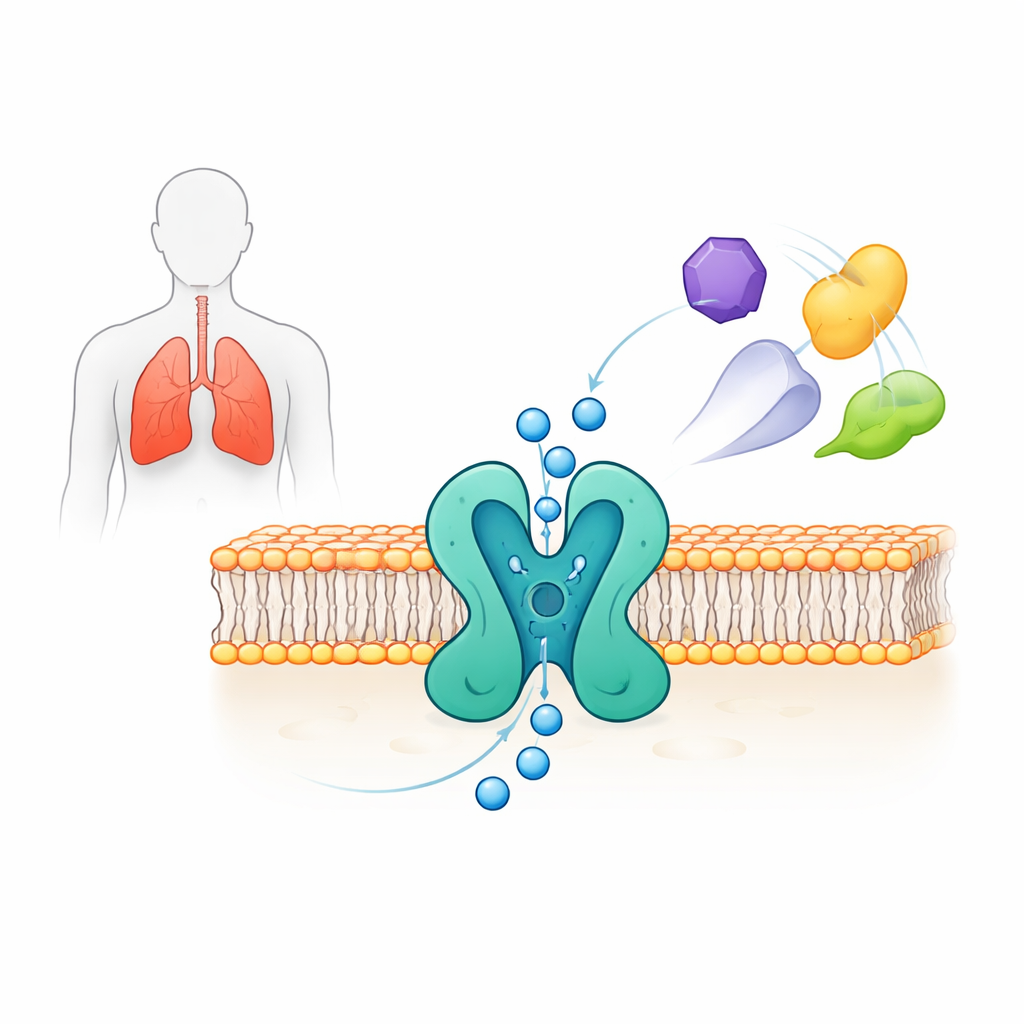
رؤية البوابة بتفاصيل ذرية
عبّر الباحثون عن نسخة كاملة الطول من TWIK-2 البشرية في خطوط خلوية بشرية واستخدموا مجهر إلكتروني بالتبريد أحادي الجسيمات لتحديد بنيتها ثلاثية الأبعاد بدقة تقارب 3.7 أنجستروم. تشكل القناة تجميعًا مكوّنًا من جزأين يخلقان معًا مسامًا مركزية لعبور أيونات البوتاسيوم. تحتوي كل نصف على أربعة مقاطع عابرة للغشاء وملوين «حلزونيين للمسامات» يشكلان منطقة ضيقة تسمى مرشح الانتقائية، حيث تُميّز البوتاسيوم عن الأيونات الأخرى. أعلاه، تنشئ هياكل «غطائية» مقوسة مسارين منفصلين لدخول الأيونات من خارج الخلية. تكشف البنية أيضًا عن عدم تماثل لطيف بين جانبي المسام يمنح TWIK-2 ترتيبًا شبه رباعي الأجزاء، وهو سمة مميزة لهذه العائلة من القنوات.
دهون مخفية ومسار أيوني مضبوط بدقة
على طول مسار توصيل الأيونات، رسم الفريق خريطة لكيفية تحرك أيونات البوتاسيوم من داخل الخلية، عبر «كمامة» كارهة للماء، صعودًا عبر مرشح الانتقائية، وخروجًا تحت الغطاء. أضيق نقطة لا تزال واسعة بما يكفي لمرور أيونات البوتاسيوم في صف واحد. رغم أن البروتين نُقّي دون إضافة جزيئات دهنية، أظهرت خرائط التبريد بالإلكترون كثافات أنبوبية محشورة قرب الجزء السفلي من المسام وفي جيوب جانبية بين الحلزونات. من المحتمل أن تمثل هذه الدهون أو ذيول المنظف التي التصقت بـ TWIK-2 أثناء التطهير، مما يوحي بأن الدهون الطبيعية في الغشاء قد تستقر في هذه الشقوق وتغير شكل الحلزونات المجاورة بشكل طفيف. تُعتقد مثل هذه التحولات، خصوصًا في الحلزون المسمى M4 وفي حلقات مرشح الانتقائية، أنها تضبط ما إذا كانت القناة مفتوحة أو مغلقة أو في حالة وسيطة.
استكشاف البوابة بالطفرات والمانعات
لربط البنية بالوظيفة، استخدم العلماء نظامًا آليًا للرقع الكهربائية لقياس التيارات من خلايا تعبر إما TWIK-2 الطبيعي أو نسخًا تم فيها تغيير أحماض أمينية محددة. وجدوا أن TWIK-2 يعتمد بشدة على الجهد الكهربائي لكنه، على عكس قرينه TWIK-1، غير حساس إلى حد كبير لتغير الحموضة الخارجية. جعلت طفرات في اثنين من بقايا الثريونين المحفوظة عند قاعدة مرشح الانتقائية القناة تفتح أسرع وتحمل تيارًا أكبر، مما يشير إلى أن هذين الموقعين يعملان كمفاصل رئيسية تثبت الحالة المغلقة. تغييرات عند مدخل ومخرج المسام عدّلت سرعة فتح القناة وإغلاقها، كاشفة مدى التحكم الدقيق في مسار الأيونات. بعد ذلك اختبر الفريق أربعة جزيئات صغيرة معروفة تعدّل قنوات ذات صلة. اثنتان منها، ML365 وNPBA، حظرتا TWIK-2 بقوة، بينما لم يكن للغير تأثير. بمقارنة كيف غيّرت الطفرات حساسية الدواء، يستنتج المؤلفون أن هذه المركبات من المحتمل أن ترتبط تحت مرشح الانتقائية وفي تجاويف مجاورة، وأن الأدوية المختلفة تستخدم أوضاع ربط متداخلة لكنها مميزة.
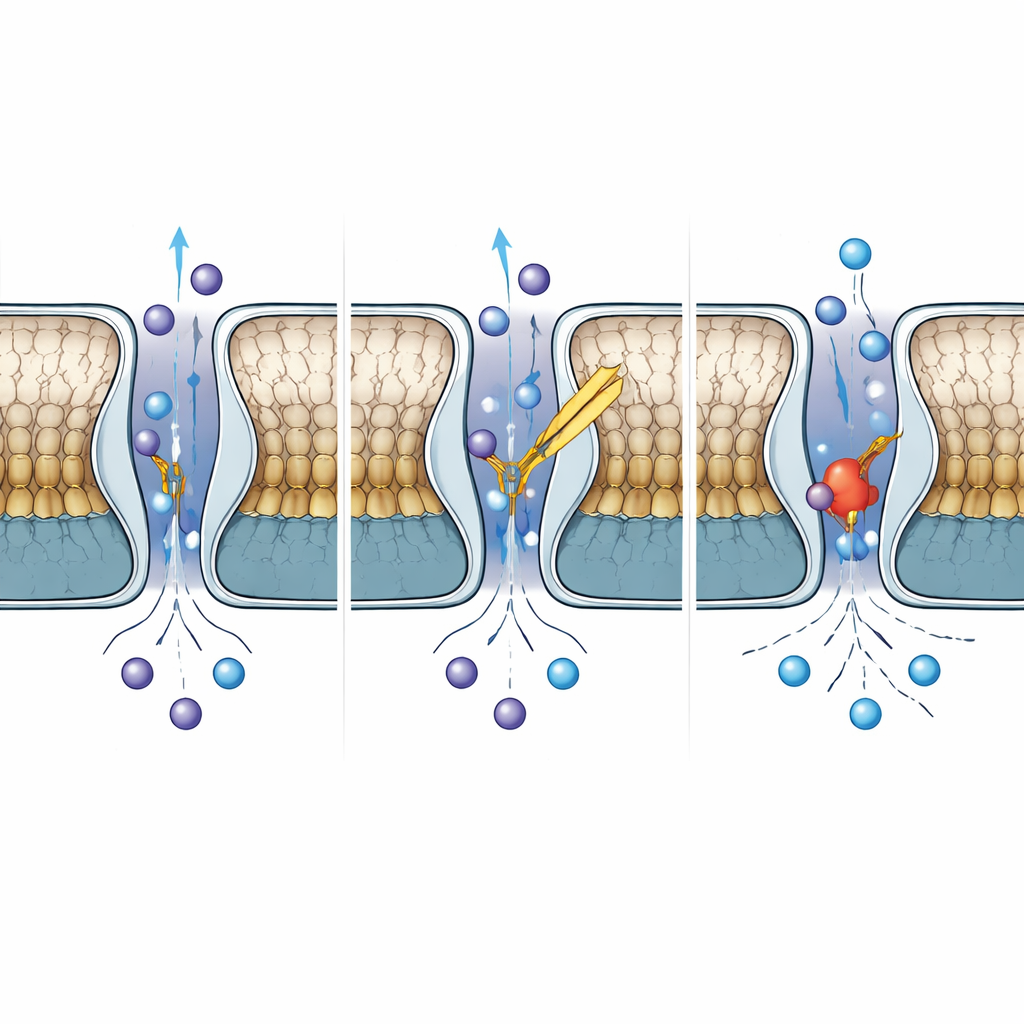
كيف تختلف TWIK-2 عن أقاربها
على الرغم من مشاركة TWIK-2 أكثر من نصف تسلسله مع TWIK-1، فإن سلوكهما يختلف بطرق مهمة. عندما قارن المؤلفون TWIK-2 مع تراكيب TWIK-1 المنشورة عند الرقم الهيدروجيني المحايد والحمضي، وجدوا أن منطقة الغطاء في TWIK-2 تشبه الشكل المثبط بالحموضة لـ TWIK-1، بينما يظل مرشح الانتقائية مرتبًا مثل الشكل الناقل والمفتوح. استبدل هيستيدين واحد في TWIK-1، المعروف بحساسيته للبروتونات ودخوله إلى المسام لحجب تدفق الأيونات عند الرقم الهيدروجيني المنخفض، بقاعدة تيروزين في TWIK-2. حتى عندما أعاد الفريق إدخال هيستيدين في هذا الموضع في TWIK-2، لم تصبح القناة حساسة للرقم الهيدروجيني، مما يوضح أن التحكم بالـ pH في هذه القنوات يعتمد على شبكة أوسع من البقايا والحركات، وليس مجرد حمض أميني «مفتاح» واحد.
من البنية إلى العلاجات المستقبلية
تجمع هذه الأعمال أول صورة عالية الدقة لـ TWIK-2 البشرية وتوضح كيف تشكل ميزات هيكلية محددة تدفق الأيونات، واستجابة الجهد، وقابلية القناة للمانعات الجزيئية الصغيرة. يفتح الاكتشاف أن مركبات موجودة يمكن أن تثبط TWIK-2 انتقائيًا، مقترنةً بمنصة فحص آلية قوية، الباب أمام بحوث واسعة النطاق للعثور على أدوية أكثر أمانًا وفعالية. وبما أن نشاط TWIK-2 في الخلايا المناعية رُبط بالالتهاب المفرط، خصوصًا في الرئتين، فيمكن أن تشكل مثل هذه الأدوية أساسًا لعلاجات مضادة للالتهاب تعمل عن طريق «خفض» نشاط هذه البوابة الصغيرة لكن القوية في غشاء الخلية.
الاستشهاد: Ma, Q., Hernandez, C.C., Navratna, V. et al. Insights into the structure and modulation of human TWIK-2. Nat Commun 17, 2201 (2026). https://doi.org/10.1038/s41467-026-69072-1
الكلمات المفتاحية: قناة البوتاسيوم TWIK-2, قنوات K2P ذات المسارين, بنية قنوات الأيونات بواسطة التبريد بالإلكترون, معدِّلات قنوات البوتاسيوم, التهاب رئوي