Clear Sky Science · ar
الخلايا العضلية الليفية موجبة التيناسين C تفاقم فرط تنسج النتوء الداخلي الوعائي عن طريق انتشار تفاعلات العصب-البلعم في الفئران
عندما تلتئم الأوعية الدموية بشكل خاطئ
تُنقذ إجراءات إعادة فتح الشرايين المسدودة، مثل توسيع الأوعية (بالون) وجراحة المجازة، أرواحًا كثيرة. ومع ذلك فإنها غالبًا ما تترك مشكلة خفْية: مع مرور الوقت قد يتكوّن ندب داخلي في الوعاء المعالج فيضيّق مجددًا ويعيد الخطر إلى المريض. تكشف هذه الدراسة في الفئران عن حوار غير متوقع ثلاثي الأطراف بين خلايا داعمة والأعصاب وخلايا الجهاز المناعي في جدار الوعاء يقود هذا الإفراط الضار في الالتئام، وتشير إلى جزيء يُدعى تيناسين C كهدف واعد لقطع هذه الدائرة.
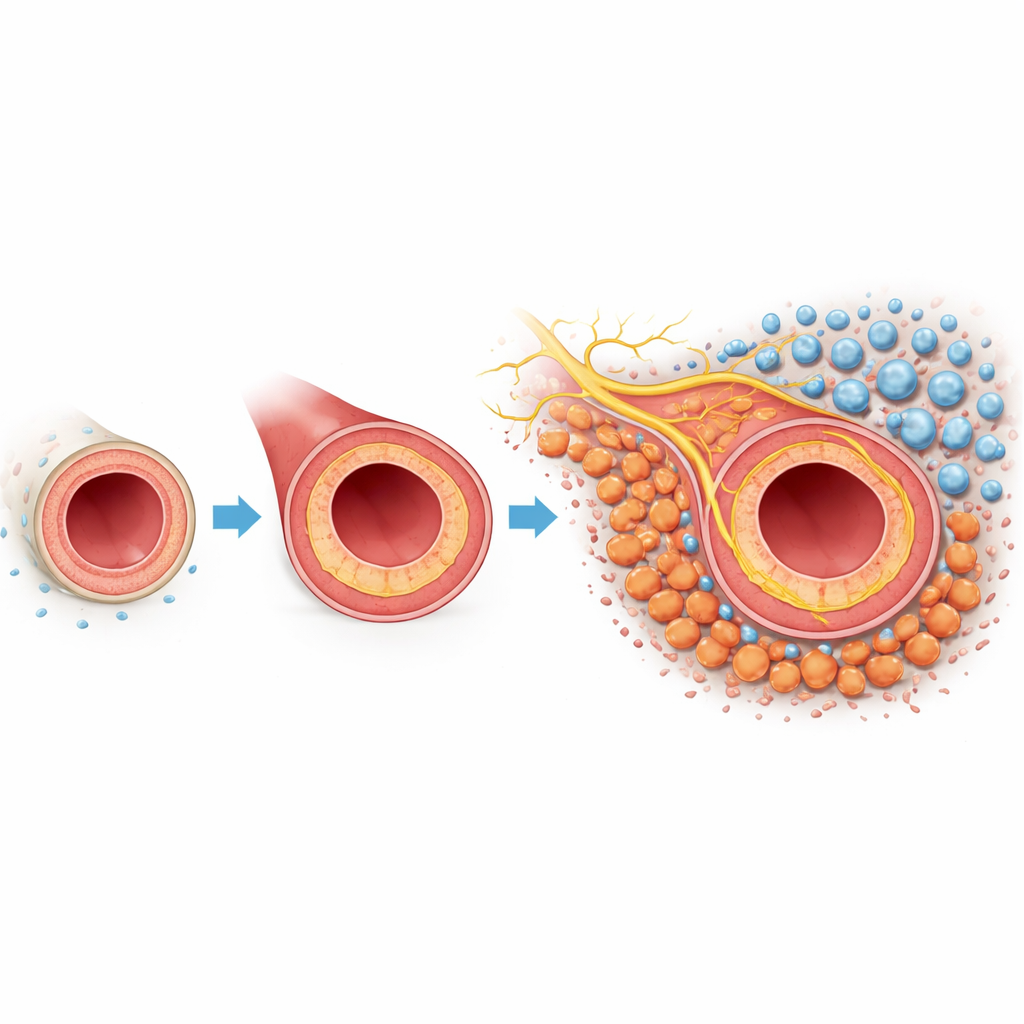
نظرة أقرب على ندوب الشرايين المشكلة للمشكلة
عندما يتعرّض شريان لإصابة أو يُعالج أثناء الجراحة، قد ينمو بطانة الوعاء الداخلية بشكل مفرط. هذا النمو الداخلي، المسمى فرط تنسج النتوء الداخلي، يثخن جدار الوعاء ويقلّل القناة التي يمر فيها الدم. تحتوي الطبقة الخارجية للوعاء، الغمد المحيطي (الأدڤنتيشيا)، على الخلايا الليفية — خلايا داعمة تحافظ عادةً على بنية الوعاء. في نموذج الفئران هذا، حيث قُطِع شريان السباتة جزئيًا لمحاكاة الإصابة، استخدم الباحثون تحليل التعبير الجيني أحادي الخلية وتحديد المواقع المكاني لحصر كل نوع خلوي رئيسي مشارك. وجدوا أن الخلايا الليفية كانت وفيرة بشكل خاص وغيرت سلوكها بشكل كبير بعد الإصابة، مما يوحي بأن هذه الخلايا قد تكون لاعبين أساسيين في استجابة التندب.
صعود خلايا التيناسين C المكونة للندب
بالغوص أعمق في تجمع الخلايا الليفية، اكتشف الفريق فئة مميزة ظهرت فقط بعد الإصابة. حملت هذه الخلايا سمات الخلايا العضلية الليفية — مستويات عالية من بروتين الانقباض α-أكتين العضلي الملس وآخر علامة تسمى بيريواستين — مشيرة إلى أنها تحولت إلى نمط إنتاج الندوب. وبشكل حاسم، أنتجت هذه الفئة أيضًا كميات كبيرة من تيناسين C، وهو بروتين في المصفوفة النسيجية نادر في الأنسجة البالغة السليمة لكنه وفير في المرض وإصلاح الأنسجة. أظهرت تجارب المختبر أن تعريض الخلايا الليفية الأدڤنتيشية الطبيعية لعامل نمو محول بيتا أو لتيناسين C إضافي دفعها لتصبح هذه الخلايا العضلية الليفية الموجبة لتيناسين C. ثم أفرزت الخلايا مزيدًا من تيناسين C، مكوّنة حلقة تعزيز ذاتي عبر زوج مستقبل سطحي محدد، الإنتغرين αvβ1، مما وسّع تدريجيًا تعداد الخلايا المكونة للندب.
تدخل الأعصاب وخلايا المناعة إلى الحي
لم تنته القصة عند تكوّن الندبة. باستخدام تصوير ثلاثي الأبعاد للعينة الكاملة وتقنيات التعبير المكاني، لوحظ أن الخلايا العضلية الليفية الغنية بتيناسين C تتجمع قرب ألياف عصبية نامية وخلايا مناعية تسمى البالعات في طبقة جدار الوعاء الخارجية. أظهرت الشرايين المصابة أعصابًا حسية كثيفة ومتداخلة ومزيدًا من البنى الشبيهة بالمشابك مقارنةً بالحالة الطبيعية، سواء في الفئران أو في عينات شريانية بشرية تعاني فرط تنسج النتوء الداخلي. حملت البالعات في هذه المناطق بصمة التهابية، منتجة جزيئات مثل IL-1β وTGF-β1 التي يمكن أن تغذي التندب أكثر. معًا رسمت البيانات صورة لبيئة مجهرية معاد تنظيمها تتداخل فيها الخلايا المكونة للندب والأعصاب والبالعات ماديًا وتؤثر على بعضها البعض.
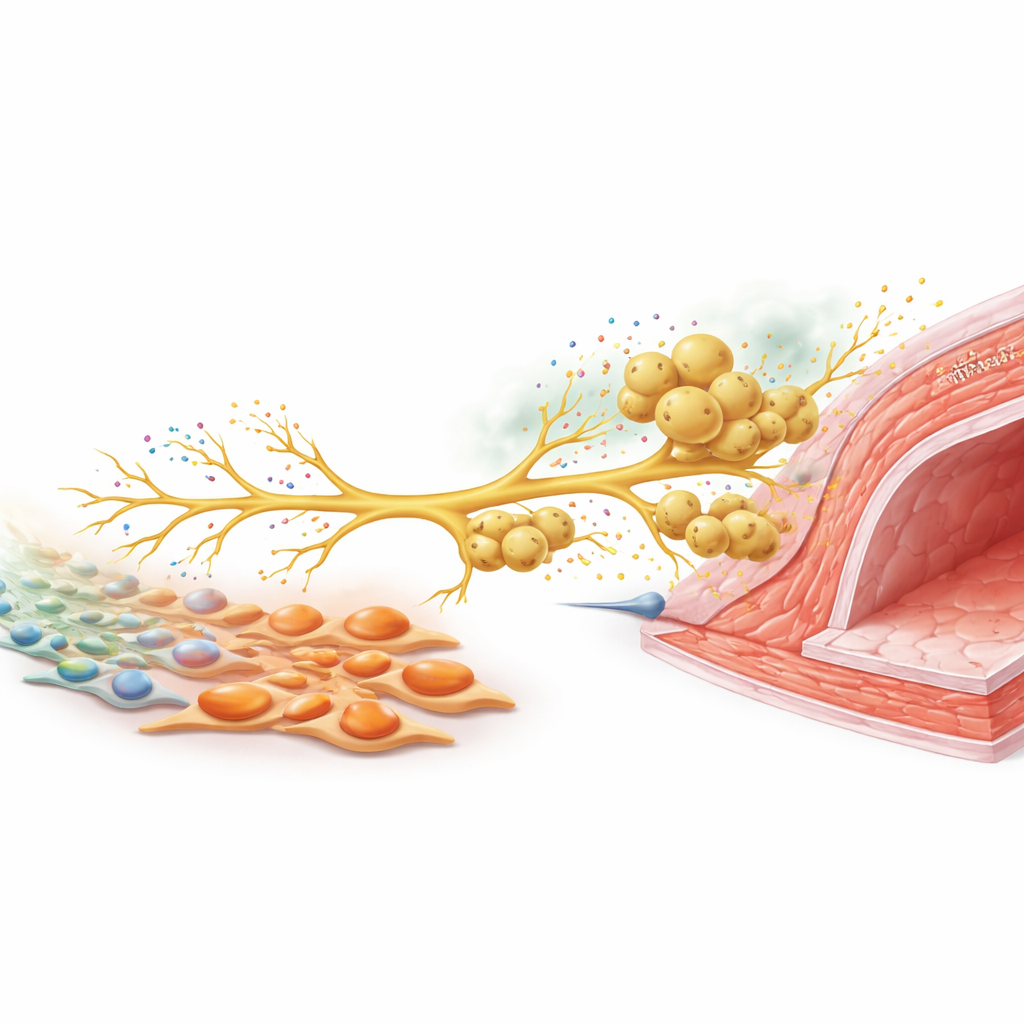
إشارة عصبية تستدعي مزيدًا من المدافعين
لفهم كيف تتواصل هذه الأنواع الخلوية، ركّز الفريق على الأعصاب الحسية التي تكشف المؤثرات الضارة. في الزرع، عززت الخلايا العضلية الليفية الغنية بتيناسين C نمو ألياف عصبية من عُقيدات الجذور الظهرية. في الفئران المصابة، زادت هذه الخلايا العصبية الحسية إنتاج CCL2، إشارة كيميائية معروفة جيدًا بجذب البالعات. عندما نمت الخلايا العصبية والبالعات معًا، هاجرت البالعات على طول الألياف العصبية النامية، تمامًا كما فعلت حول الشرايين في الحيوان الحي. قلّل إسكات CCL2 في الخلايا العصبية بشكل حاد من تجنيد البالعات. في الحيوانات، أدى تقليص نشاط الأعصاب الحسية بسمّ أو حذف تيناسين C بشكل انتقائي في الخلايا الليفية إلى خفض كثافة الأعصاب ومستويات CCL2 وتراكم البالعات، وفي النهاية تقليل تثخن جدار الوعاء. لم تضف المقاربة المزدوجة فائدة إضافية، مما يوحي بأنهما يعملان على نفس المسار.
لماذا تهم هذه المسار الجديدة
تلخّص النتائج دائرة شريرة: تحث الإصابة الخلايا الليفية على أن تصبح خلايا عضلية ليفية منتجة لتيناسين C؛ تعيد هذه الخلايا تشكيل المصفوفة وتحفز الأعصاب الحسية؛ تطلق الأعصاب المنشّطة CCL2، التي تجذب البالعات؛ وتفرز البالعات عوامل التهابية وتليفية تزيد من التندب وتضيّق الشريان. من خلال تحديد تيناسين C ومحور الأعصاب-البلعميات المتبع downstream كمحركات مركزية لهذه الحلقة، تشير الدراسة إلى أن العلاجات التي تستهدف هذا الجزيء أو شركاء إشاراته قد تساعد في إبقاء الشرايين المعالجة مفتوحة لفترة أطول، ما يوفر حماية أكثر ديمومة للمرضى بعد الإجراءات القلبية الوعائية.
الاستشهاد: Tong, X., Shi, G., Fang, Z. et al. Tenascin C+ myofibroblasts exacerbate vascular neointimal hyperplasia by propagation of nerve-macrophage interactions in mice. Nat Commun 17, 2199 (2026). https://doi.org/10.1038/s41467-026-69062-3
الكلمات المفتاحية: فرط تنسج النتوء الداخلي, تيناسين C, إعادة تشكيل الأوعية الدموية, الأعصاب الحسية, التهاب البالعات