Clear Sky Science · ar
باكليتاكسيل يدفع توسع البلاعم الحاملة لـ TREM2 مما يفسر فعاليته العلاجية الأدنى مقارنةً بناب‑باكليتاكسيل
لماذا تهم هذه الدراسة
يتلقى عدد كبير من النساء المصابات بسرطان الثدي أدوية كيميائية من فئة التاكانات، وأشهرها باكليتاكسيل أو نسخة حديثة مرتبطة بجسيمات ألبومين صغيرة تُعرف باسم ناب‑باكليتاكسيل. لطالما اشتبه الأطباء أن الدواء الأحدث يعمل في كثير من الأحيان بشكل أفضل، لكن الأسباب كانت غير واضحة. تغوص هذه الدراسة في بيانات المرضى وتجارب الحيوان لتُظهر أن الباكليتاكسيل العادي قد يساعد عن غير قصد انتشار السرطان إلى الرئتين عن طريق إعادة تشكيل خلايا الجهاز المناعي، وتحدد أيضاً وسيلة لدرء هذا التأثير الضار.
دواءان متشابهان، نتيجتان مختلفتان
قارن الباحثون أولاً الأداء الواقعي للباكليتاكسيل والناب‑باكليتاكسيل لدى آلاف النساء المصابات بسرطان الثدي. من خلال تجميع نتائج 17 دراسة سريرية شملت 6,486 مريضة، وجدوا أن ناب‑باكليتاكسيل حقق معدلات انكماش أورام أعلى ومعدلات اختفاء تام للسرطان في الثدي والعقد اللمفاوية القريبة قبل الجراحة. كانت هذه الميزة أقوى بشكل خاص لدى المرضى الذين عولجوا بعد فشل العلاجات السابقة. ومع أن الدوائين أعطيًا بجرعات متقاربة ومصممان لاستهداف الخلايا السرطانية المنقسمة بنفس الطريقة إلى حد كبير، فإن ذلك يوحي بأن هناك اختلافاً يتجاوز القتل المباشر للورم.
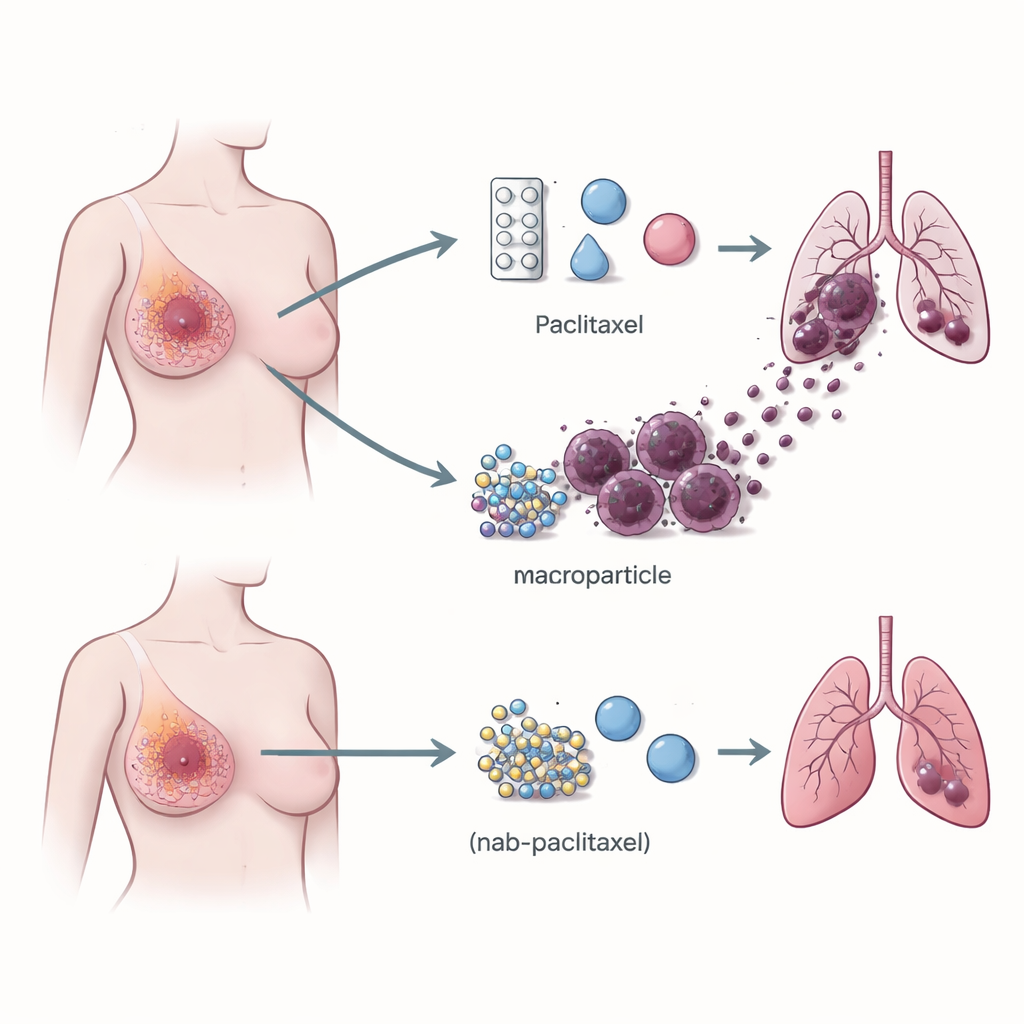
خلايا مناعية تساعد السرطان على الانتقال
تحولت الأنظار إلى البيئة المناعية للورم—خليط خلايا الدم البيضاء التي يمكنها إما محاربة السرطان أو، وكثيراً ما يحدث بشكل غير متوقع، مساعدته على النمو. باستخدام تسلسل الحمض النووي الريبي أحادي الخلية، الذي يقرأ نشاط الجينات في آلاف الخلايا الفردية، قارن الفريق أوراماً من مرضى عولجوا بالباكليتاكسيل مقابل ناب‑باكليتاكسيل. وجدوا أن الأورام المعالجة بالباكليتاكسيل احتوت على عدد أكبر بكثير من البلاعم الحاملة لمستقبل يُدعى TREM2 على سطحها. كانت هذه البلاعم الإيجابية لـ TREM2 مركزة عند حواف الورم وكانت أكثر وفرة بكثير لدى المرضى الذين طورت لديهم نقائل رئوية لاحقاً مقارنةً بمن بقيت لديهم الحالة محدودة. تثبت هذه النمطية نفسها في مجموعات مرضى أكبر وفي نماذج الفئران، مما يقيم رابطاً قوياً بين هذا النوع من البلاعم وخطر انتشار السرطان.
عندما يضمر العلاج الأورام لكنه يغذي الانتشار
في الفئران الحاملة لأورام ثديية، فعل الباكليتاكسيل ما يُتوقع منه: أبطأ أو قلص الأورام الأولية. لكن في الوقت عينه زاد من عدد مستوطنات السرطان في الرئتين وعزز البلاعم الإيجابية لـ TREM2 في الأورام وفي مجرى الدم. على النقيض، قلل ناب‑باكليتاكسيل من حجم الورم دون أن يدفع نحو نقائل رئوية أو يوسع هذه البلاعم، مع أنه كان فعالاً بالمثل في تصغير الورم الرئيسي. عندما حُذف الجين المسؤول عن TREM2 في الفئران، أو عندما قللوا من TREM2 باستخدام أوليغونوكليوتيدات مضادة‑المعنى (قطع قصيرة من الـDNA تثبط جينات معينة)، استمر الباكليتاكسيل في تقليص الأورام الأولية لكنه فقد إلى حد كبير قدرته على تعزيز الانتشار الرئوي. يشير ذلك إلى أن البلاعم الحاملة لـ TREM2 ليست مجرد مراقبين سلبيين؛ بل شركاء مطلوبون في نقائل تُحفزها الباكليتاكسيل.
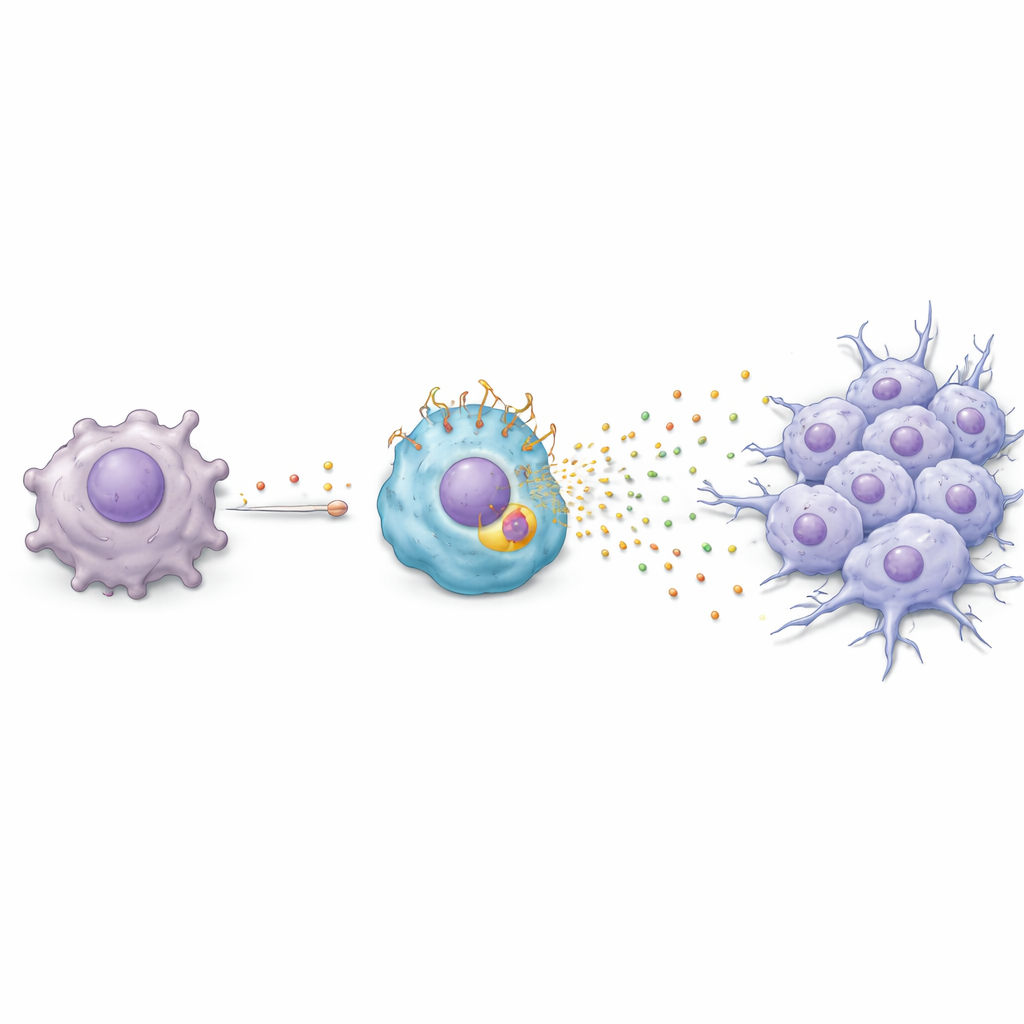
تفاعل كيميائي متسلسل من الورم إلى الخلية المناعية
سأل الفريق بعد ذلك كيف يدفع الباكليتاكسيل البلاعم إلى التحول إلى هذه الحالة الضارة الغنية بـ TREM2. اكتشفوا سلسلة تفاعلات: يحفز الباكليتاكسيل خلايا السرطان على تشغيل جين استجابة للضغط يُدعى ATF3، الذي يقوم بدوره بزيادة إنتاج عامل نمو يُسمى FGF2. تُفرج خلايا السرطان عن FGF2 إلى محيطها، حيث يؤثر على البلاعم القريبة. في تلك البلاعم، يقوم FGF2 بتفعيل منظم آخر، EGR1، الذي يرفع مستويات TREM2. بمجرد أن يرتفع TREM2، تبدأ البلاعم بإفراز مزيج من البروتينات—بما في ذلك Serpin E1 وHGF وCCL3 وCXCL2—التي تدفع خلايا السرطان إلى شكل أكثر حركة وغزوًا يعرف بالانتقال الظهاري‑اللحائي (epithelial‑mesenchymal transition). في الأطباق المخبرية وفي الفئران، جعل هذا الحوار الكيميائي خلايا الورم أكثر ميلاً للهجرة والغزو، وهما خطوتان أساسيتان نحو النقائل.
تحويل السلاح ذو الحدين إلى أداة أكثر أماناً
من منظور مبسط، الرسالة الرئيسية أن الباكليتاكسيل يمكن أن يعمل كسيف ذو حدين: بينما يهاجم الأورام، فإنه أيضاً يوجّه خلايا مناعية معينة لمساعدة السرطان على الهروب إلى أعضاء بعيدة. يبدو أن ناب‑باكليتاكسيل يتفادى إطلاق هذا الخلل المناعي المحدد. والخبر المشجع هو أن حجب TREM2—أو أجزاء من مسار الإشارة FGF2–EGR1–TREM2—يمكن أن يفصل فوائد الباكليتاكسيل في تصغير الأورام عن مخاطره التي تعزز النقائل في نماذج حيوانية. إذا ثبت أن استراتيجيات مماثلة آمنة وفعالة في البشر، قد يتمكن الأطباء من الاستمرار في استخدام دواء كيميائي مألوف ومتوافر على نطاق واسع مع كبح ميوله لتشجيع انتشار السرطان، مما يؤدي إلى نتائج طويلة الأمد أفضل للمرضى.
الاستشهاد: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
الكلمات المفتاحية: سرطان الثدي, باكليتاكسيل, البيئة الميكروية للورم, البلاعم, النقائل