Clear Sky Science · ar
تنظيم الماء بين الواجهات لنقل الأكسجين إلى روابط بنزيليك C(sp3)–H عبر تفعيل الكوفالينس بين النيكل والأكسجين في التنجستن
تحويل الماء والزيت إلى مواد كيميائية مفيدة
لطالما رغب الكيميائيون في طريقة أنظف لتحويل جزيئات بسيطة مستمدة من النفط إلى مكونات أكثر قيمة للبوليمرات والأدوية والمنتجات اليومية. تُظهر هذه الدراسة كيف أن "ضبط" الطبقة الرقيقة من الماء التي تلامس القطب بعناية يمكن أن يسمح للماء العادي بتزويد الأكسجين لجزيئات الهيدروكربون عنيدة، مما يقلل النفايات واستهلاك الطاقة في العملية.
لماذا يهم الحصول على الأكسجين من الماء
العديد من المواد الكيميائية الصناعية تُصنَّع بإضافة الأكسجين إلى الهيدروكربونات—وهي جزيئات مبنية أساساً من الكربون والهيدروجين. اليوم غالباً ما يتطلب ذلك استعمال عوامل مؤكسدة قوية ودرجات حرارة مرتفعة، ما يستهلك كميات كبيرة من الطاقة ويُنتج انبعاثات تُسخّن المناخ. الماء مصدر رخيص وآمن ومتوافر للأكسجين، لكن إقناعه بمشاركة ذلك الأكسجين مباشرةً مع روابط الكربون–الهيدروجين الصعبة يتطلب عادة جهودًا كهربائية عالية جدًا. تحت تلك الظروف القاسية يُهدر معظم التيار الكهربائي في تفكيك الماء إلى غاز الأكسجين بدل إنتاج منتجات مفيدة.
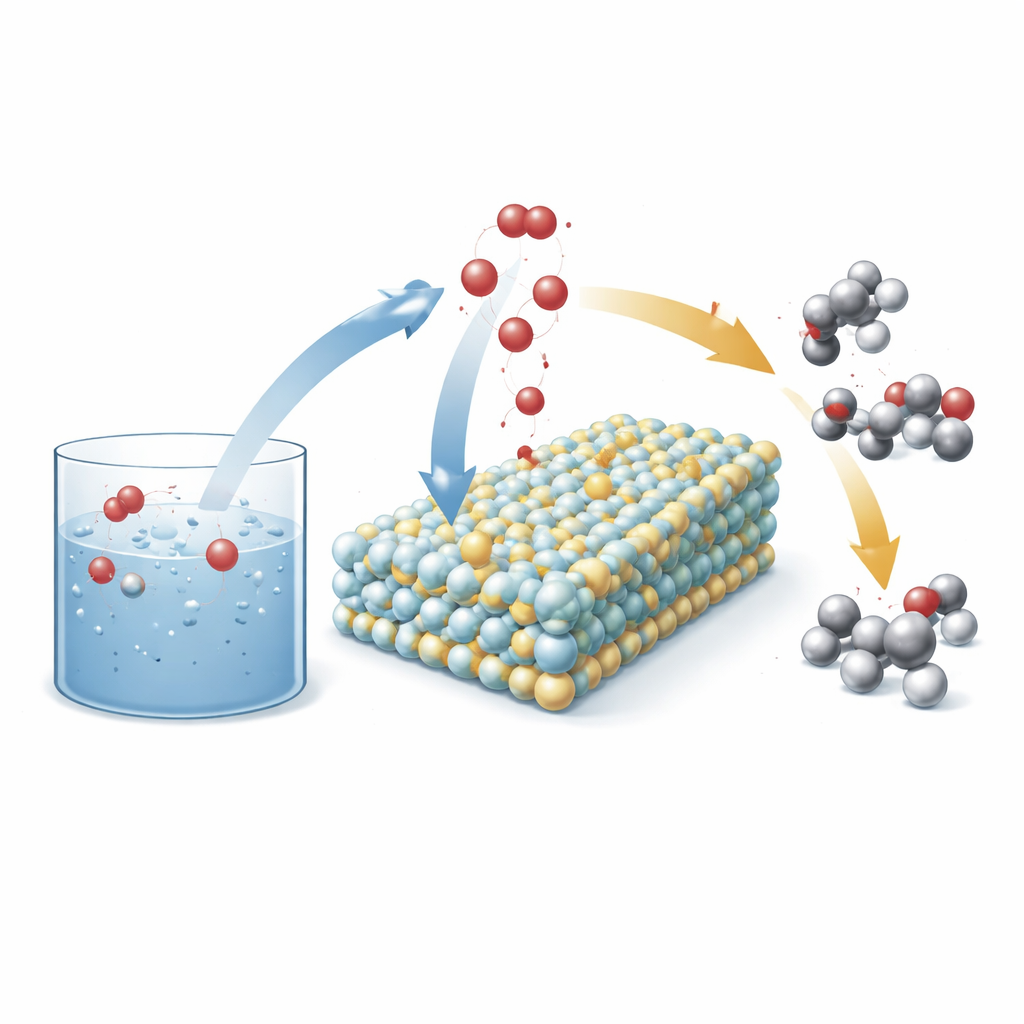
قطب ذكي يعيد ترتيب الماء
صمم الباحثون نوعاً جديداً من الأنود (القطب الموجب في خلية كهروكيميائية) مبنياً من جزيئات صغيرة من كربيد التنجستن تتحول أثناء التشغيل إلى مادة غير متبلورة من التنجستن–الأكسجين. أضافوا ذرات النيكل منفردة داخل هذا الإطار. في ظروف التفاعل، يهاجر الأكسجين من الماء إلى الصلب، محولاً السطح إلى أكسيد تنجستن منشّط بالنيكل مع العديد من المواقع التفاعلية المكشوفة. يعمل هذا السطح المعاد بناؤه كمنصة يلتقي فيها الماء وجزيئات الهيدروكربون لتبادل الأكسجين بطريقة مُتحَكَّمَة، مفضلاً تكوين منتجات قيِّمة مثل الكحولات والكيتونات بدلاً من الأحماض والمنتجات الثانوية المؤكسدة مفرطاً.
تخفيف قفص الماء عند السطح
اكتشاف رئيسي هو أن ذرات النيكل تشوِّش بشكل طفيف طريقة تكدس جزيئات الماء مقابل القطب. عادةً يشكل الماء عند سطح مشحون شبكة كثيفة من الروابط الهيدروجينية، تشبه شبكة مشدودة تُبطئ الحركة. تُظهر المحاكاة الحاسوبية والقياسات الطيفية تحت الحمراء الحساسة أنه بالقرب من المناطق المحوَّضة بالنيكل تصبح هذه الشبكة أرخى، مع روابط هيدروجينية أقل ومزيد من جزيئات الماء "الحرة". هذا يفتح قنوات يمكن للماء من خلالها الانتشار بسهولة أكبر نحو مواقع التنجستن–الأكسجين التفاعلية. نتيجة لذلك، يمكن لقطع حاملة للأكسجين من الماء أن تصل إلى السطح بسرعة أكبر وبوتيرة أعلى، تغذي التفاعل بدلاً من الهروب كغاز أكسجين.
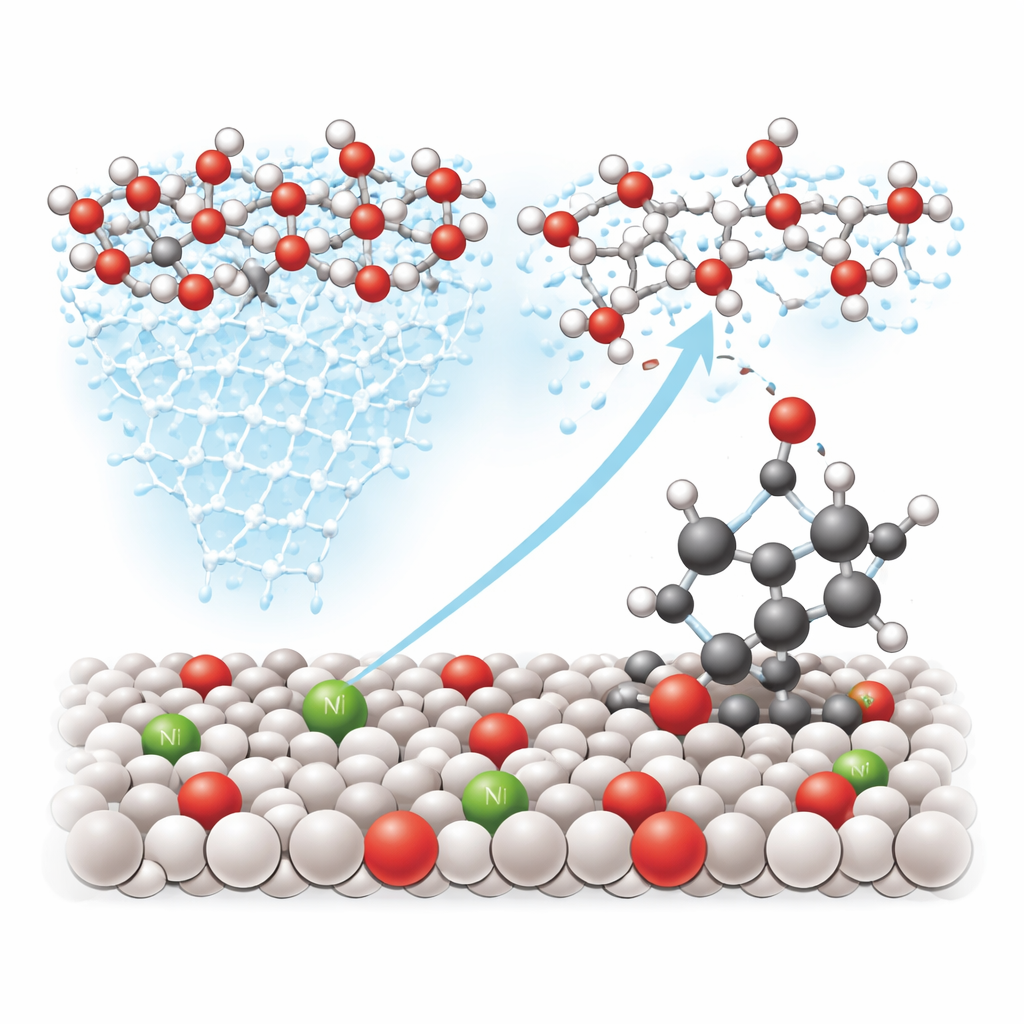
توجيه الأكسجين إلى الروابط الصحيحة
بعيداً عن تحسين حركة المرور عند السطح، يضبط النيكل أيضاً البنية الإلكترونية لذرات التنجستن المجاورة، مما يجعل أماكن معينة جيدة خصوصاً في جذب وتنشيط الماء. تُظهر تجارب الفريق باستخدام النظائر—نسخ خاصة من الأكسجين والهيدروجين يمكن تتبعها—أن الأكسجين النشط يأتي من الماء الذي انقسم حديثاً وليس من كتلة الأكسيد نفسه. تلتقط لقطات طيفية جسراً قصير العمر بين التنجستن، والأكسجين، والكربون البنزيلي في جزيئات مثل إثيل بنزين. تؤكد الحسابات النظرية أنه على السطح المعدل بالنيكل يصبح من الأسهل لذرة أكسجين أن تهاجم موقع الكربون–الهيدروجين هذا بدلاً من اتباع مسار تفكيك الماء المعتاد الذي يُنتج غاز الأكسجين، مما يوجّه التفاعل نحو منتجات مؤكسنة مفيدة.
كفء، انتقائي، ومصمم ليصمد
في الاختبارات، يحول القطب المنشط بالنيكل مجموعة من روابط الكربون–الهيدروجين البنزيليّة إلى كحولات وكيتونات بكفاءات فاراداي—نسبة الشحنة الكهربائية التي تُستخدم في الكيمياء المرغوبة—تكون عادة فوق 50%، وتصل إلى أكثر من 56% في الحالات المحسّنة. يعمل النظام لعدة دورات دون فقدان النشاط، مع الحفاظ على بنيته النيكل–التنجستن. وبما أنه يستخدم الماء كمصدر الأكسجين الوحيد ويتجنّب عوامل مؤكسدة كيميائية مُضافة، فإنه يقدم كفاءة طاقية تنافسية وتكاليف مواد أقل مقارنةً بطرق متقدمة أخرى. ورغم أن النطاق الحالي يركز على المواقع البنزيلية، فإن المبدأ الأساسي—استخدام مضافات ذرية لإعادة تشكيل الماء بين الواجهات وإعادة توجيه مسارات التفاعل—يشير إلى مجموعة أدوات أوسع لأكسدة أكثر صداقة للبيئة تعمل بالكهرباء لروابط الكربون–الهيدروجين الخاملة.
ما الذي يعنيه هذا لكيمياء أنظف
تُظهر هذه الدراسة أن تغييرات صغيرة على المستوى الذري يمكن أن يكون لها آثار كبيرة على سلوك الماء عند القطب ومكان انتهاء الأكسجين. باستخدام ذرات النيكل لتخفيف بنية الماء بين الواجهات وضبط المواقع التفاعلية بدقة، يحول المؤلفون الماء إلى مانح أكسجين فعّال للروابط الهيدروكربونية الصعبة التنشيط، مع كبح تشكّل غاز الأكسجين غير المرغوب فيه. على المدى الطويل، يمكن لاستراتيجيات من هذا النوع أن تساعد في إعادة تصميم كيمياء الأكسدة في الصناعة الكيميائية، مما يجعلها أكثر كفاءة في استهلاك الطاقة وصداقة للمناخ عبر استخدام الكهرباء والماء بدلاً من المؤكسدات القاسية والمواد المشتقة من الأحافير.
الاستشهاد: Leng, BL., Lin, X., Dong, HY. et al. Regulating interfacial water for oxygen transfer to benzylic C(sp3)–H bonds via Ni-activated tungsten-oxygen covalency. Nat Commun 17, 2355 (2026). https://doi.org/10.1038/s41467-026-69054-3
الكلمات المفتاحية: التحفيز الكهربائي, أكسدة الماء, تنشيط رابطة C–H بنزيليك, أكسيد التنجستن محوَّض بالنيكل, كيمياء خضراء