Clear Sky Science · ar
تسلسل الحمض النووي الريبوزي المزدوج داخل الكائن الحي يكشف العوامل المؤثرة الأساسية في تعطيل الحاجز الظهاري بواسطة مُمْرِض خارجي
كيف يتسلل بعض الجراثيم عبر أسوار خلايانا
تُبطن أعضاؤنا بخلايا مكتظة بإحكام تعمل كجدران، تحافظ على الدم والميكروبات والسموم في مكانها. ومع ذلك، تنجح بعض الجراثيم في الانزلاق بين هذه الخلايا والانتشار عبر الجسم. تكشف هذه الدراسة بتفصيل حيّ كيف يصل البكتيريا المسببة للليبْتُوسْبيريوْسيس، وهو مرض خطير منتشر عالمياً، بهدوء إلى أعضاء مثل الكبد والكليتين، ثم يستخدم خدعة ذكية تعتمد على الكالسيوم داخل خلايانا ليفتح هذه الحواجز الواقية.
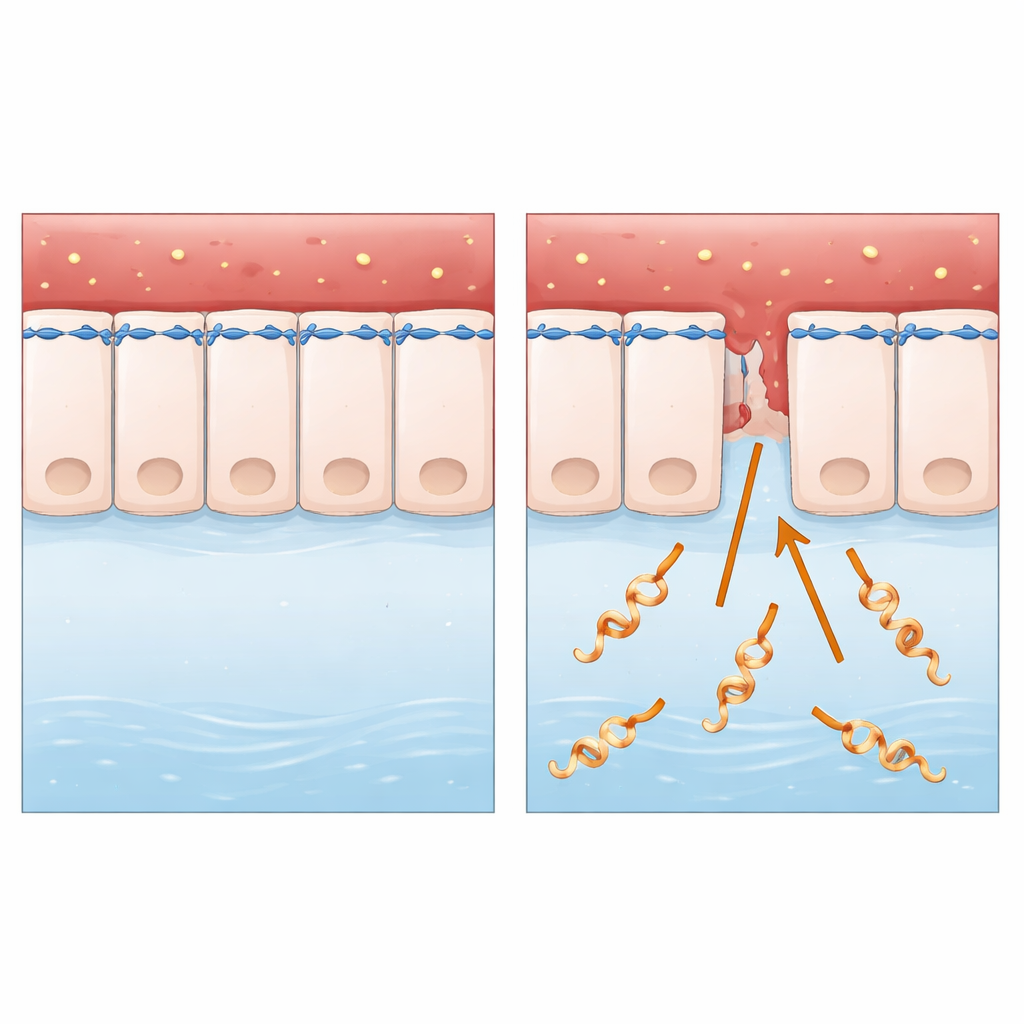
غازي خفي لأنسجة الحيوانات والإنسان
تركز الأبحاث على Leptospira interrogans، بكتيريا لولبية الشكل تنتقل أساساً من الحيوانات إلى البشر عبر الماء أو التربة الملوثة. بعد دخولها عبر شقوق صغيرة في الجلد أو الأغشية المخاطية، تتجول في مجرى الدم ويمكن أن تُحدث مرضاً شديداً، بما في ذلك فشل الكبد والكلى ونزفاً داخلياً. وعلى خلاف العديد من الميكروبات المدروسة جيداً، تعيش Leptospira خارج الخلايا وتفتقر إلى بعض “الأسلحة الجزيئية” الكلاسيكية التي يبحث عنها العلماء عادة. وهذا جعلها حالة اختبار مثالية لطرح سؤال أساسي: كيف تعبر بكتيريا بسيطة تبدو حرة العيش طبقات خلوية سليمة بهذه الكفاءة؟
مراقبة حوار جينات العائل والجرثوم في آن واحد
لالتقاط عملية العدوى داخل حيوان حي، استخدم الفريق تسلسل الحمض النووي الريبوزي المزدوج في الهامستر، كنموذج للليبْتُوسْبيريوْسيس الحاد. تقرأ هذه الطريقة أي الجينات شغالة أو مطفأة في كل من العائل والمُمْرِض في نفس الوقت. أصاب العلماء الهامسترات وجمعوا أنسجة الكبد والكلى بعد يوم ويومين. في البداية، وعلى الرغم من الأعداد العالية للبكتيريا، لم تُظهر خلايا الحيوان تغيرات كبيرة في نشاط الجينات، مما يوحي بأن Leptospira تنزلق في البداية تحت رادار الجهاز المناعي. إلا أنه بحلول اليوم الثالث، أبدت كلا العضوين استجابة قوية، خاصة الكبد: تغيّرت بشدة الجينات المشاركة في الالتهاب وروابط الخلايا والبنية الداخلية الخلوية، مما يشير إلى إعادة تشكيل نشطة للحواجز النسيجية.
تفكيك سحاب الخلايا من الخارج إلى الداخل
تُحكم طبقات الخلايا بواسطة الوصلات الضيقة والوصلات الالتصاقية، التي تربط الخلايا المجاورة بعضها ببعض وتؤمنها بحلقة من الأكتين والمايوسين، نفس زوج البروتينات الذي يساعد العضلات على الانقباض. أظهرت الميكروسكوبية لخلايا طلائية بشرية مُصابة بـLeptospira تغيُّر شكلها، وفتحًا للفجوات بين الخلايا وضعفًا أو اختلالًا في مواقع بروتينات الوصلات الأساسية. ومن المهم أن الخلايا لم تمت، ما يعني أن الحاجز كان يتفكك وليس يُدمّر. كما لاحظ الباحثون إشارات ضغوط في مصانع طي البروتينات داخل الخلايا، لكن حجب هذا الإجهاد لم يعِد الوضع إلى سابقه عند الوصلات، ما دلّهم على سبب آخر.
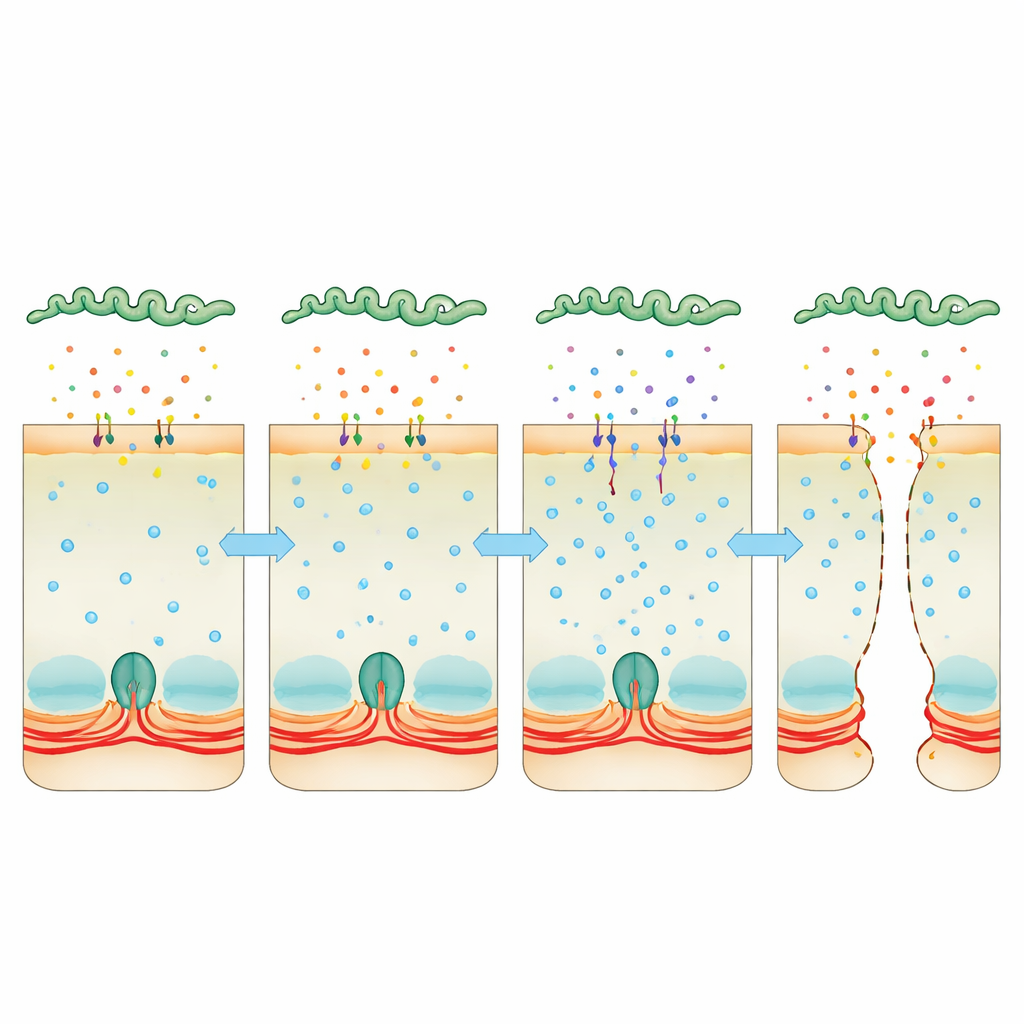
استغلال الكالسيوم كعَتَلة خفية
توجّه الانتباه إلى الكالسيوم، الإشارة العامة داخل الخلايا التي يمكن أن تشد أو تريح حلقة الأكتين–المايوسين. تراكم الكالسيوم في الخلايا المصابة، وربط ذلك بزيادة نشاط كيناز سلسة المايوسين الخفيفة، إنزيم يجعل الحلقة الانقباضية تشد الوصلات. عندما استخدم الفريق مركباً يمتص الكالسيوم، أو أدوية تثبط الكالمدولين أو هذا الكيناز، بقيت طبقات الخلايا أكثر تماسكا وصعّب ذلك على البكتيريا أن تتسلل. في الوقت نفسه، كشفت التسلسلات العميقة لحمض الريبي النووي للبكتيريا أن Leptospira داخل العائل تعزز بشدة إنتاج بروتينين «معدّلين للضراوة» يشبهان السموم. تُفرَز هذه البروتينات إلى المحيط، وتلتصق بخلايا العائل وتوجد داخلها. عندما افتقرت البكتيريا إلى واحد أو كلا هذين البروتينين، أصبحت أقل قدرة بكثير على عبور طبقات الخلايا أو إحداث مرض مميت، ولم يعد السائل المُفرَز منها يرفع مستويات الكالسيوم أو يفكك الوصلات بنفس الفعالية.
ماذا يعني ذلك للمرض والدفاعات المستقبلية
معاً، ترسم النتائج قصة واضحة. بعد أن تتسلل Leptospira إلى الجسم تقريبا دون أن تُلاحظ، تبدأ بإفراز بروتينات شبيهة بالسموم والمعدّلة للضراوة. ترتبط هذه البروتينات بالخلايا الطلائية وتُخلّ بتوازن الكالسيوم داخلها، مما يفعّل بدوره مسارًا انقباضياً يسحب «سحاب» الخلايا الذي يربط الخلايا المجاورة ببعضها. ومع ارتخاء الوصلات الضيقة والالتصاقية، تظهر فجوات مجهرية تسمح للبكتيريا بالمرور بين الخلايا، واستعمار الأعضاء وإحداث مرض شديد. من خلال تحديد هذا الآلية المدفوعة بالكلسيوم والبروتينات البكتيرية المسؤولة عنها، تفتح الدراسة طريقًا نحو استراتيجيات جديدة — مثل حجب هذه البروتينات أو مسار إشارتها — لتعزيز أسوار خلايانا والحد من انتشار الليبتوسبيريوْسيس وربما عدوى أخرى تستغل تكتيكات مماثلة.
الاستشهاد: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
الكلمات المفتاحية: الليبْتُوسْبيريوْسيس, الحاجز الظهاري, إشارة الكالسيوم, سموم بكتيرية, تفاعلات العائل والمُمْرِض