Clear Sky Science · ar
تحسين nDIA-MS باستخدام عوامل زيادة الشحنة يمكّن التنميط الكلي لتحولات ذائبية البروتينات الناتجة عن الأدوية
لماذا يهم سلوك البروتين أكثر من العدّ البسيط
يمكن أن تغير الأدوية ليس فقط كمية البروتين الذي تصنعه الخلية، بل أيضاً المكان الذي يذهب إليه هذا البروتين وما إذا كان حراً أم يتكتّل ويلتصق بهياكل خلوية. هذه التحولات في «المكان» و«الحالة» التي توجد فيها البروتينات داخل الخلايا مرتبطة ارتباطاً وثيقاً بأمراض مثل السرطان والتنكس العصبي، ومع ذلك يصعب قياسها على نطاق واسع. تقدم هذه الدراسة طريقة سريعة وقوية لمسح آلاف البروتينات البشرية دفعة واحدة لرصد كيف تتغير ذائبيتها — أي ما إذا كانت في حالة حرة أو أكثر ارتباطاً — عندما تتعرّض الخلايا لدوائين مستخدمين على نطاق واسع في التجارب.
طريقة أسرع وأوضح لمراقبة البروتينات
يعتمد المؤلفون على تقنية أساسية في الأحياء الحديثة: مطيافية الكتلة، وهي تقنية تزن وتعد شظايا البروتينات. تتفوق الطرق القياسية بالفعل في إخبارنا بكمية كل بروتين موجود، لكنها تواجه صعوبة في كشف تغيّر حالة البروتين، مثل الانتقال إلى الحمض النووي أو الاندماج في مركّبات كثيفة. هنا، يحسّن الباحثون نسخة من مطيافية الكتلة تسمى الاكتساب المعتمد على البيانات بمنافذ ضيقة (nDIA-MS). بإضافة مساعدين كيميائيين صغار، يُعرفون بعوامل زيادة الشحنة، إلى السائل الناقل الذي يحمل الببتيدات عبر الجهاز، يعزّزون الشحنات الكهربائية على هذه الشظايا ويقوون الإشارة بشكل كبير.
بعد اختبار مضافين شائعين لعوامل زيادة الشحنة، ثنائي ميثيل السلفوكسيد (DMSO) و/أو م-نتروبنزيل كحول (mNBA)، وجدوا أن 3% DMSO يعطي أكبر زيادة إجمالية في الإشارة وأعلى عدد من البروتينات المكتشفة، بينما يكون mNBA أفضل في زيادة عدد وشحنة شظايا الببتيد الفردية. مع الإعداد المحسّن، يمكن للفريق تحديد نحو 9600 بروتين بشري من مجرد ميكروغرام واحد من هضم خلوي قياسي في جريان لمدة 15 دقيقة — وهو مزيج لافت للسرعة والعمق للتجارب الروتينية. يهيئ هذا الأداء استخدام nDIA-MS ليس فقط لعد البروتينات، بل لاستقصاء كيف تستجيب حالتها الفيزيائية للإجهاد.
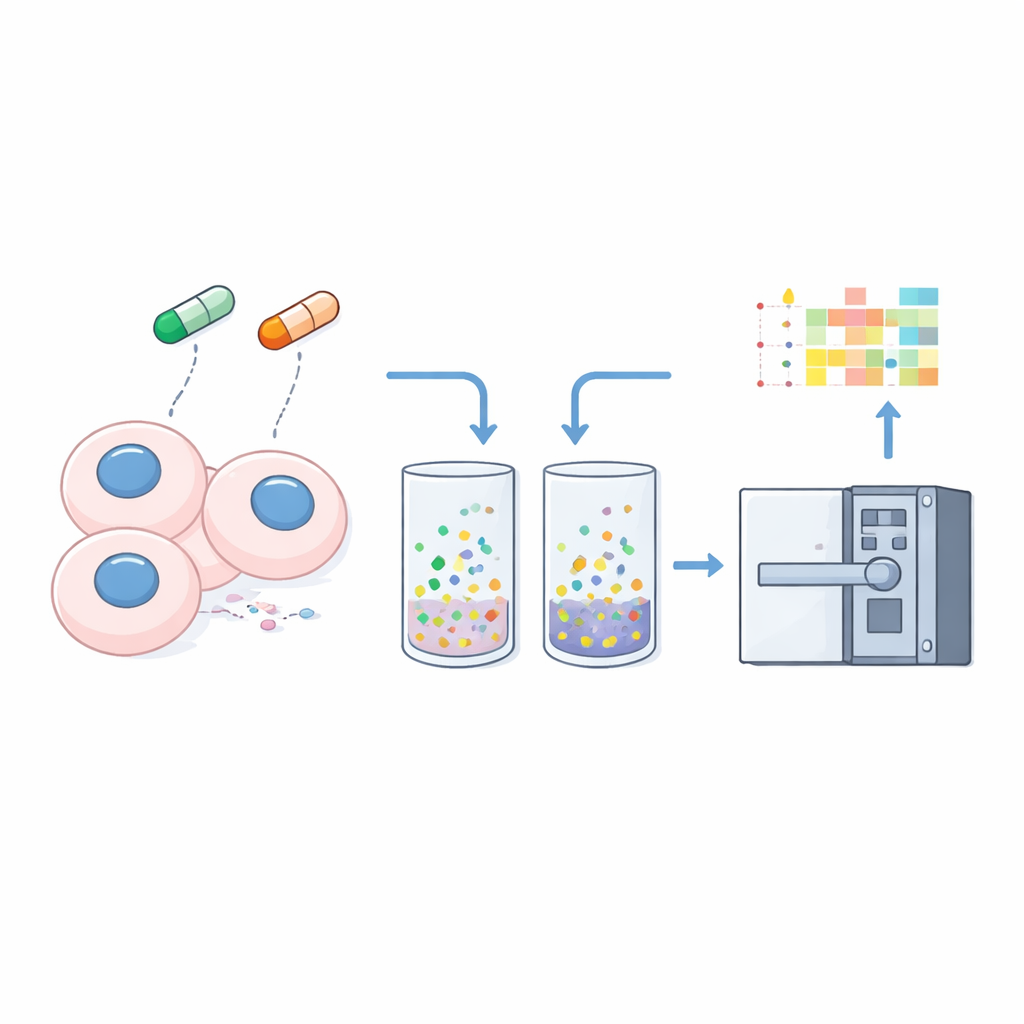
تحويل الذائبية إلى مقياس للتغير الخلوي
لتحويل الذائبية إلى إشارة قابلة للقياس، يعالج الباحثون الخلايا بعناية بمذيب لطيف يستخلص البروتينات الحرة القابلة للذوبان، تاركاً مادة مرتبطة بإحكام بالحمض النووي أو الأغشية أو هياكل أخرى. يحللون كلٍ من المستخلص الكلي للخلايا وهذا «الطرد غير القابل للذوبان» من ثلاث خطوط خلوية سرطانية باستخدام طريقة nDIA-MS المحسّنة. بمقارنة وفرة كل بروتين في الطرد نسبةً إلى عينة الخلايا الكلية، يحسبون «نسبة عدم الذائبية» بسيطة — القيم الأعلى توحي بارتباط أقوى بالهياكل الخلوية، والقيم الأقل توحي بحالة أكثر ذوباناً وحراً.
ثم يعرض الفريق الخلايا لمدة ساعة فقط لدوائين: MG132، وهو مانع للبروتيازوم يمنع الخلايا من تحطيم البروتينات غير المرغوب فيها، وML‑792، مثبط لتفعيل SUMO يتداخل مع نظام وسم البروتينات المهم. هذا التعرض القصير مقصود؛ يهدف إلى التقاط التحولات السريعة والمبكرة في سلوك البروتين قبل أن تتكشف تغييرات التعبير الجيني بالكامل. حتى خلال هذه النافذة القصيرة، يمكنهم قياس تغيّرات الذائبية والوفرة لـ 8694 بروتيناً والتأكد من أن عملية الفصل تفصل بوضوح البروتينات القابلة للذوبان الكلاسيكية، مثل التوبولين، عن البروتينات المرتبطة بالكروماتين، مثل الهيستونات.
أدوية تعيد تشكيل خريطة البروتينات داخل الخلية
تُحدث MG132 وML‑792 إعادة تشكيل واسعة النطاق لكنها مميزة لذائبية البروتينات. يجعل MG132 أكثر من ألف بروتين أقل قابلية للذوبان وأكثر من ستمائة أكثر قابلية للذوبان عبر خطوط الخلايا الثلاثة. العديد من البروتينات المتأثرة تقع عند مفترق طرق مراقبة جودة البروتين، واستجابة تلف الحمض النووي، وتنظيم الجينات، والالتهاب الذاتي (autophagy) — نظام تنظيف الخلية. على سبيل المثال، تصبح مكونات مركب منشط البروتيازوم والموائمات التي تساعد على وسم البروتينات المعيبة أقل ذوباناً، ما يوحي بأنه عندما يُحجب التحلل، فإن عوامل مراقبة الجودة الأساسية نفسها قد تُحبس على هياكل مثل الكروماتين أو أغشية الخلية. تنتقل بروتينات الالتهاب الذاتي ولاعبي استجابة التلف، بما في ذلك منظم الإجهاد HSF1، أيضاً نحو حالات أكثر عدم ذوبان تشبه المكثفات، متماشية مع تكوّن أجسام الإجهاد النووية.
بالمقابل، يستهدف ML‑792 بقوة بروتينات مشاركة في النسخ ونظام SUMO نفسه. يصبح مئات البروتينات إما أكثر أو أقل ذوباناً عند حجب تفعيل SUMO، وتنتقل بروتينات SUMO الأساسية إلى المخزن القابل للذوبان، كما هو متوقع. تبرز الدراسة سلوكيات لافتة: تصبح وحدات فرعية من بوليميراز RNA III أقل قابلية للذوبان، مشيرةً إلى تغيير في الاستيراد النووي أو ارتباطها بالكروماتين؛ أما كابحات رئيسية مرتبطة بالأجسام النووية، مثل SP100 وDAXX، فتصبح أكثر ذوباناً، مما يدل على أن علامات SUMO تساعد في إبقائها محجوزة في تلك المقصورات. عند تطبيق كلا الدوائين منفردين أو بالتتابع، يظهر بعض البروتينات، بما في ذلك NAB2 وSMAD2 وRB1، تحولات متناسقة أو حتى متعاكسة في الذائبية، كاشفةً عن تداخل دقيق بين نظامي الوسم باليوبكويتين وSUMO في التحكم بتوطين البروتين.
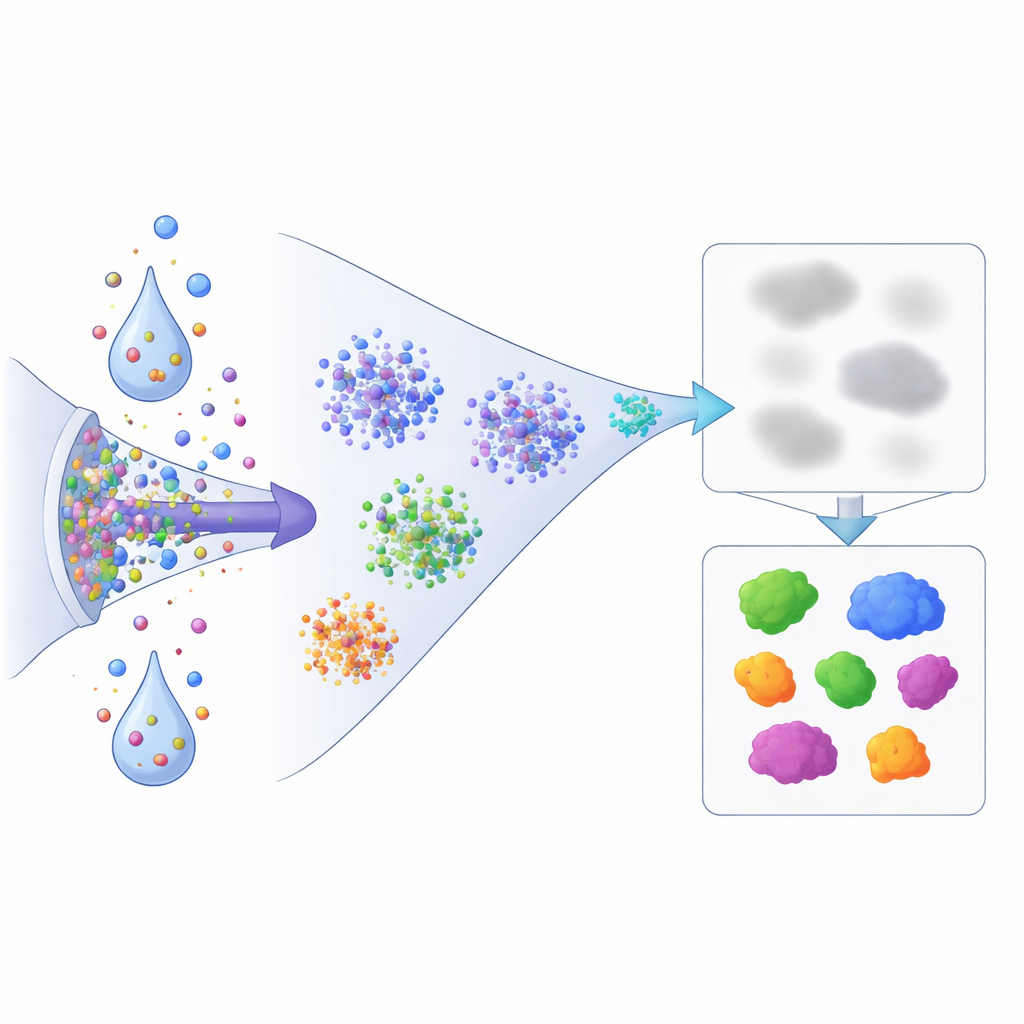
ما معنى ذلك لاكتشاف الأدوية مستقبلاً
للغير متخصصين، الرسالة الأساسية هي أن البروتينات لا تكتفي بالزيادة أو النقصان في الكمية عندما تتعرض الخلايا للإجهاد أو للعلاج؛ بل تتحرّك وتتكاثف وتتغير درجة ارتباطها بالهياكل الخلوية. تقدم هذه الدراسة وسيلة واسعة النطاق وسريعة المدى لمراقبة تلك التحولات أثناء حدوثها. بدمج سير عمل مضبوط لمطيافية الكتلة مع مقارنة بسيطة بين القابل للذوبان وغير القابل للذوبان، يبين المؤلفون أن أدوية تجريبية شائعة تعيد تنظيم المشهد الداخلي للبروتينات بسرعة بطرق قد تفلت من قياسات الوفرة التقليدية. تفتح المنهجية الباب لرسم خرائط كيفية إعادة الأدوية المرشّحة تشكيل حالات البروتين في أنحاء الخلية، مما يساعد الباحثين على كشف أهداف غير متوقعة، ومسارات استجابة للإجهاد، ونقاط فشل قد تكون حاسمة لفهم كل من التأثير العلاجي والآثار الجانبية.
الاستشهاد: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
الكلمات المفتاحية: ذائبية البروتيوم, مطيافية الكتلة, مثبط البروتيازوم MG132, مثبط السومويلation ML-792, تحولات حالة البروتين