Clear Sky Science · ar
الهيكل الداخلي المصمم لجزيئات دهنية نانوية ذات قشرة ونواة يعزز إطلاق المَسْكالَة (mRNA) من الحويصلات الداخلية بفعالية
لماذا يهم هذا الحيلة الجديدة في التوصيل
العديد من الأدوية الحديثة الأكثر إثارة، من لقاحات كوفيد-19 إلى علاجات السرطان التجريبية، مبنية على الرنا المرسال، أو mRNA. لكن هناك مشكلة مزمنة: بعد دخول هذه السلاسل الهشة إلى خلايانا، يُحتجز معظمها ويُدمر داخل أكياس داخلية صغيرة تسمى الحويصلات (endosomes). تقدم هذه الدراسة إعادة تصميم ذكية للفقاعات الدهنية الصغيرة المعروفة بجزيئات الدهن النانوية، التي تحمل mRNA. عبر إعادة تنظيم بنيتها الداخلية حول نواة ذهبية صلبة، حسّن الباحثون بشكل كبير كمية mRNA التي تُحرر إلى فضاء الخلية العامل، حيث يمكنها بالفعل تصنيع بروتينات مفيدة.
منح الناقلين الصغار خطة جسمية أفضل
تعتمد لقاحات وعلاجات mRNA الحالية في الغالب على جسيمات طرية وشبه غير منتظمة مصنوعة من مزيج من الدهون التي تحيط بالـ mRNA. نظريًا، يجب أن تصبح الدهون “القابلة للتأين” في هذه الجسيمات موجبة الشحنة في داخل الحويصلات الحمضي وتُمزق غشاء الحويصلة، محررةً mRNA. عمليًا، تلغي الشحنة السالبة لـ mRNA الكثير من هذا التأثير، بحيث يصل نحو 2 بالمئة فقط من الـ mRNA الموصل إلى آلات صنع البروتين داخل الخلية. طرح المؤلفون سؤالًا بسيطًا لكنه قويًا: بدلًا من تغيير كيمياء الدهون فقط، ماذا لو أعادوا هندسة البنية الداخلية للجسيم للتحكم في مكان تواجد الـ mRNA والدهون بالنسبة لبعضها البعض؟
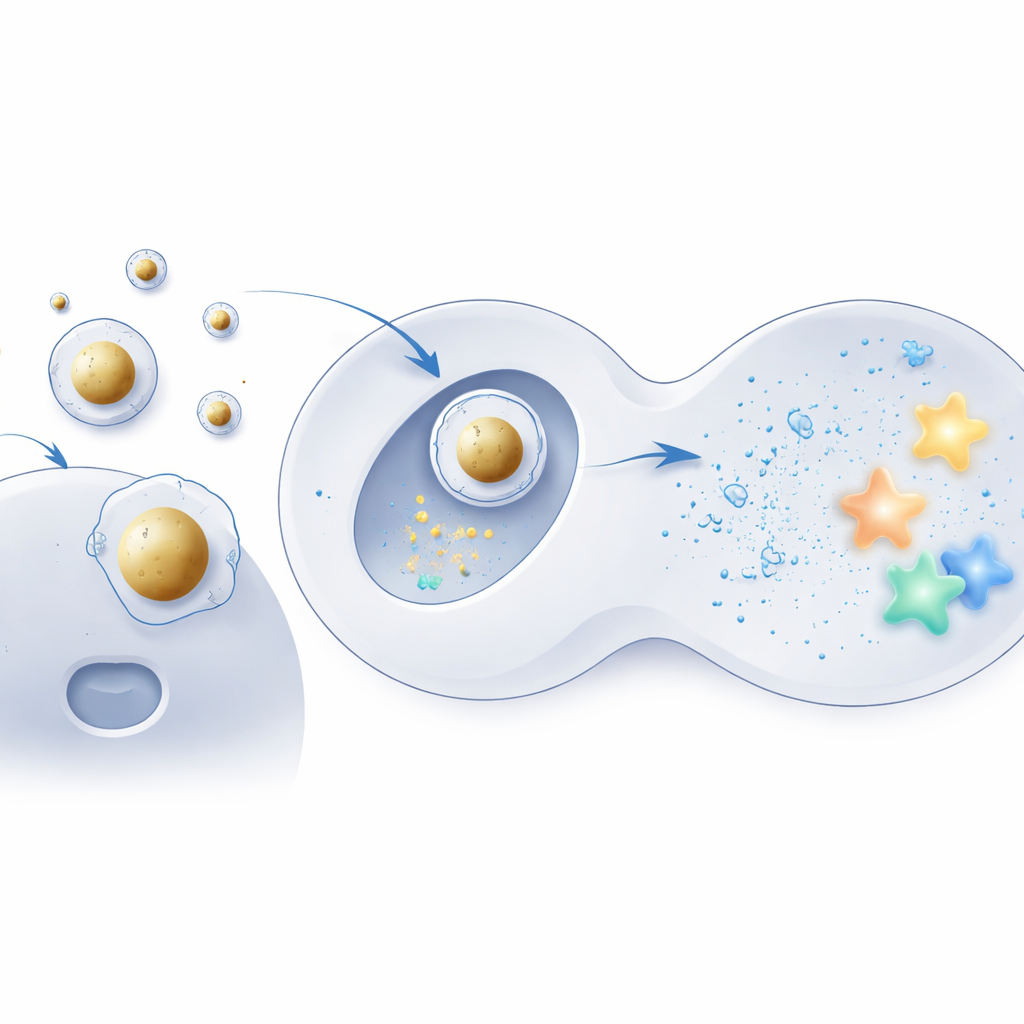
بناء غلاف توصيل متمركز حول الذهب
لاختبار هذه الفكرة، استخدم الفريق كرات ذهبية صغيرة كنوى صلبة وغطّوها بنفس الدهون القابلة للتأين المستخدمة في التحضيرات التقليدية. تم تكثيف الـ mRNA المشحون سالبًا أولًا على هذه النوى، ثم غُلف التجميع بمزيج مألوف من الدهون المساعدة والجزيئات المثبتة، مكوّنًا بنية منتظمة من نواة وقشرة. أظهرت الميكروسكوبي الإلكترونية والمحاكيات الحاسوبية أن هذه “جسيمات الذهب-الدهنية النانوية” كانت متجانسة للغاية، مستقرة ترموديناميكيًا، وحافظت على شكلها جيدًا في ظروف مائية تشبه الجسم. والأهم أن تركيبة الدهون الإجمالية ظلت كما هي في الجسيمات القياسية، مما يبرز بنية الداخل—وليس المكونات—كالتغيير الرئيسي.
كيف يعزز الداخل المعاد ترتيبه الهروب
في بيئة الحويصلة الحمضية المعتدلة، تصبح النواة المعتمدة على الذهب موجبة بشدة، فَتجذب الـ mRNA المشحون سالبًا إلى الداخل بينما تدفع الدهون القابلة للتأين المشحونة موجبة إلى الخارج نحو الغشاء المحيط. هذا الفصل المدفوع بالشحنة يركز الدهون التي تُحدث تمزقًا في الغشاء بالضبط حيث تكون مطلوبة. في اختبارات أغشية نموذجية وفي كريات الدم الحمراء، كانت الجسيمات الجديدة أكثر فاعلية في اختراق الأغشية عند pH منخفض بينما تظل هادئة عند pH محايد، وهي ميزة أمان مرغوبة. في خلايا حية، أظهر تصوير الـ mRNA المفلور زيادة بنحو الضعف في الهروب من الحويصلات وزيادة مذهلة تقارب ~100 ضعف في مدى انتشار الـ mRNA عبر السيتوبلازم مقارنة بالجسيمات التقليدية.
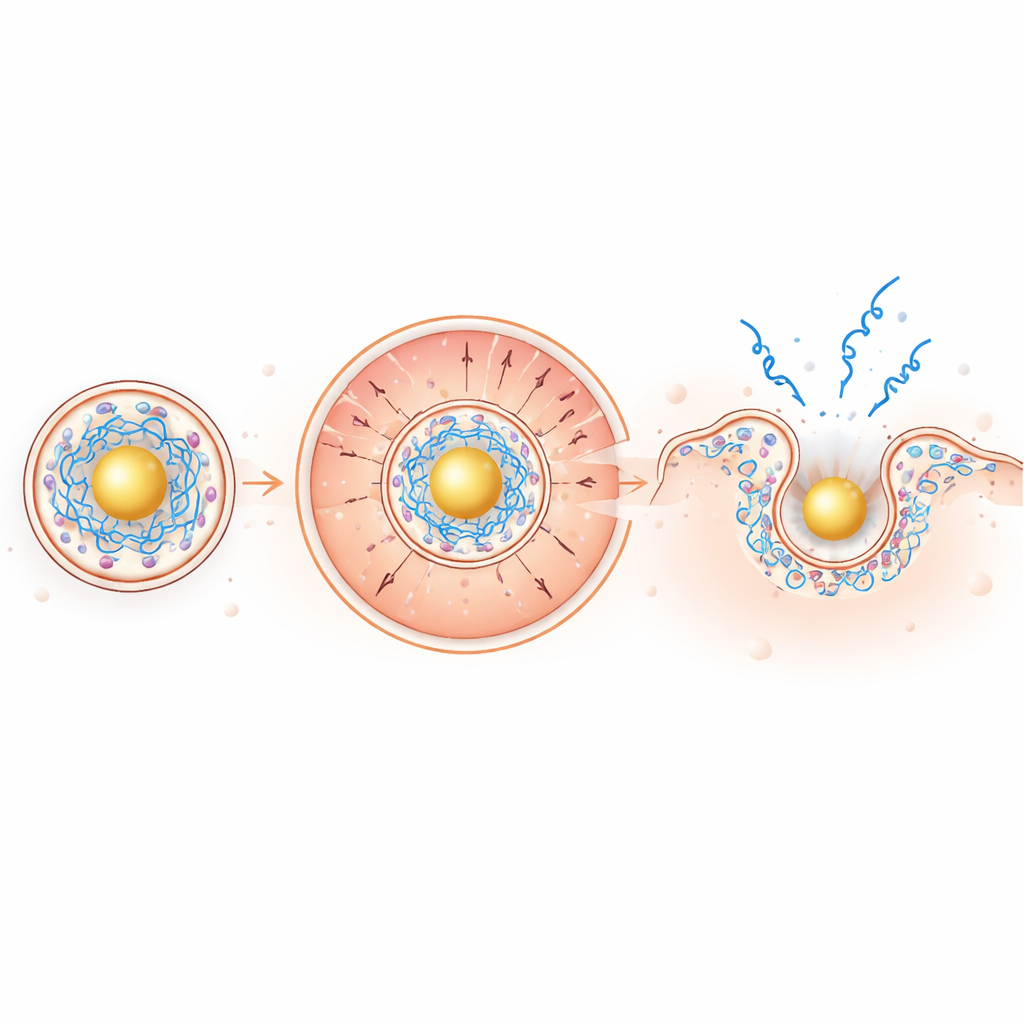
من الأطباق إلى الفئران: إشارات أقوى وحماية أعلى
ترجمت هذه المزايا الفيزيائية إلى مكاسب بيولوجية حقيقية. عبر عدة أنواع خلوية، أدت الجسيمات ذات النواة الذهبية إلى إنتاج بروتينات تقريرية أعلى بكثير من التحضيرات القياسية، لا سيما عند الجرعات المنخفضة. في الفئران، عززت إنتاج البروتين الموجه بواسطة mRNA بنسبة تصل إلى خمسة إلى سبعة أضعاف بعد الحقن في العضلات أو الأوردة، دون تغيير مواقع تراكم الجسيمات في الجسم. عند استخدامها لتوصيل لقاح mRNA لبروتين السبايك لفيروس SARS‑CoV‑2، ضاعفت الجسيمات المصممة تقريبًا مستويات الأجسام المضادة بعد الجرعة الأولى وزادتها أكثر بعد المعزّز، مع إنتاج أجسام مضادة مقوية أكثر فعالية في تحييد الفيروس. في نموذج صعب لسرطان الثدي الثلاثي السلبية، أدت لقاحات mRNA المحمولة بواسطة الجسيمات الجديدة إلى تقلص الأورام بفعالية أكبر، وخفض إشارات نشاط الورم، وطالت فترة النجاة بشكل ملحوظ.
السلامة ومسار نحو أدوية مستقبلية
رغم استخدام الذهب كنواة، بدا أن الجسيمات مقبولة جيدًا في الفئران. لم تظهر أوزان الجسم، مؤشرات الالتهاب، وفحوصات الأنسجة سمية كبيرة، وعادت مستويات الذهب في الأعضاء إلى نحو الطبيعي خلال يومين. يؤكد المؤلفون أن الذهب يعمل أساسًا كدعامة لإثبات المفهوم: يمكن أن يُطبق نفس مبدأ التصميم الداخلي على مواد آمنة أو قابلة للتحلل الحيوي الأخرى. الرسالة الأساسية لغير المتخصصين هي أن طريقة تعبئة الـ mRNA داخل حاملها الصغير يمكن أن تكون مهمة بقدر أهمية ما نعبئه به. من خلال إعطاء الجزيئات الدهنية النانوية ترتيبًا داخليًا أكثر انضباطًا، يقدم هذا العمل طريقة جديدة لتجاوز عنق الزجاجة القديم في توصيل mRNA—ما يفتح الباب أمام لقاحات وعلاجات أكثر فاعلية عبر الأمراض المعدية والسرطان وما بعدها.
الاستشهاد: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
الكلمات المفتاحية: توصيل mRNA, جزيئات دهنية نانوية, الهروب من الحويصلات الداخلية, النانوطب, لقاحات الرنا