Clear Sky Science · ar
العلاج المُركَّب المستهدف والمعتمد على التشكيل فوق الجيني يعزِّز المناعة المضادة للأورام عبر تثبيت التعبير المعتمد على GATA6 لمستضد MHCI في سرطان القناة البنكرياسية الغُدي
لماذا يهم هذا البحث لسرطان البنكرياس
سرطان القناة البنكرياسية الغُدي واحد من أكثر السرطانات فتكًا، ويرجع ذلك إلى حدٍّ كبير إلى قدرته على الاختباء من الجهاز المناعي ومقاومته لمعظم الأدوية. تكشف هذه الدراسة عن حالة خلوية ورمية محددة، يقودها جين يُسمى GATA6، تجعل خلايا سرطان البنكرياس أكثر وضوحًا لهجوم المناعة. ويبين المؤلفون أيضًا كيف يمكن لمزيج من نوعين من الأدوية أن يحافظ على هذه الحالة الضعيفة ويعزز قدرة خلايا T القاتلة على مهاجمة الأورام في نماذج تجريبية.
حالة خلوية ورمية تدعو الجهاز المناعي
ليست كل خلايا سرطان البنكرياس متشابهة في سلوكها. بعض الخلايا تحتفظ بهوية أكثر انتظامًا تشبه الخلايا الطلائية، بينما تنتقل أخرى نحو حالة أكثر قدرة على الحركة وعدوانية تشبه الحالة الميزنكيمية. عامل النسخ GATA6 يساعد في الحفاظ على الهوية الطلائية ويرتبط بنتائج أفضل لدى المرضى. في مجموعات مرضى كبيرة، احتوت الأورام ذات مستويات GATA6 المرتفعة على المزيد من الخلايا المناعية، بما في ذلك خلايا CD8 «القاتلة»، مقارنة بالأورام التي بها القليل أو لا شيء من GATA6. باستخدام تصوير مكاني متقدم على عينات أورام بشرية، وجد الباحثون أن خلايا السرطان الإيجابية لـGATA6 كثيرًا ما كانت مجاورة لخلايا CD8، وأبدت مستويات أعلى من جزيء يسمى MHCI، الذي يعمل كعلم يبيّن لخلايا T ما يوجد داخل الخلية. تشير هذه الملاحظات إلى أن GATA6 يميِّز مجموعة من خلايا الورم تكون بطبيعتها أكثر وضوحًا للجهاز المناعي. 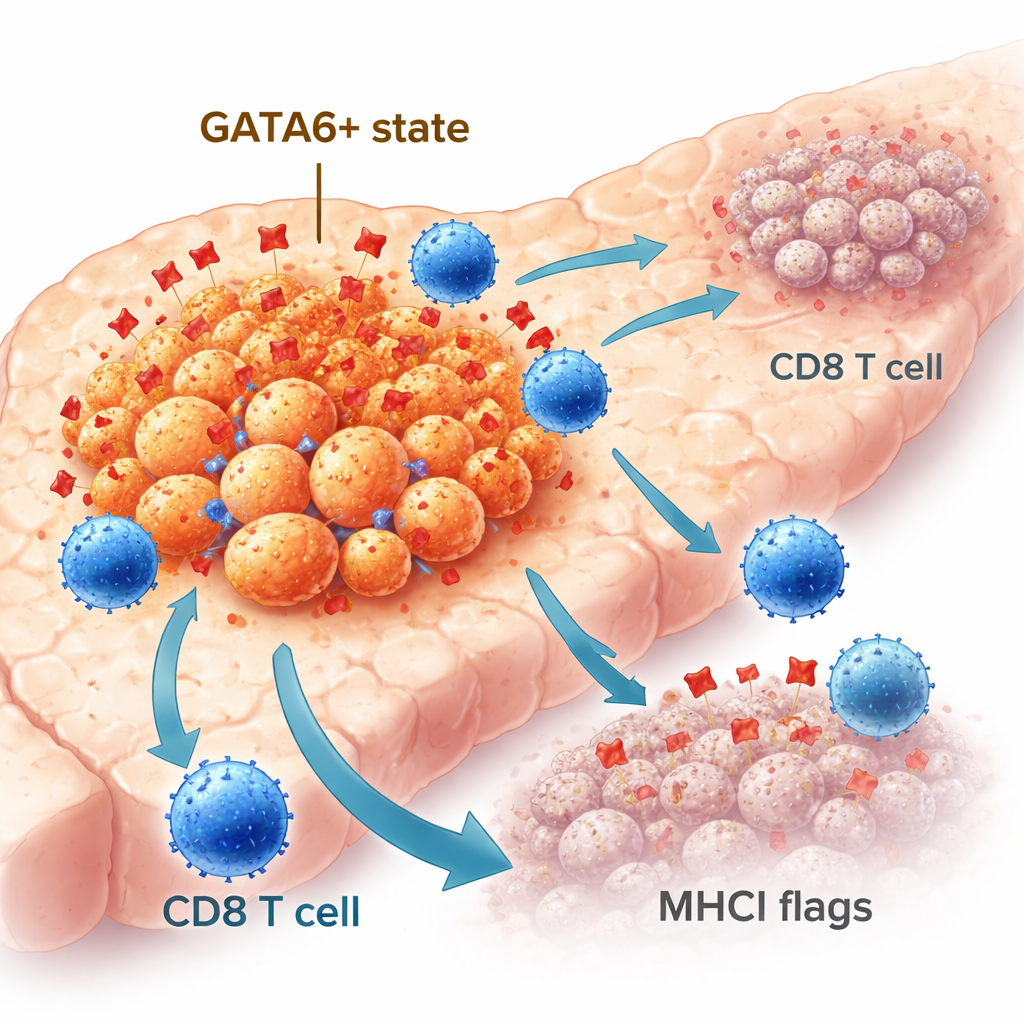
علاج مستهدف يعزز وضوح الورم — لكنه يأتي بتكلفة
سأل الفريق بعد ذلك ما إذا كانت الأدوية المستهدفة يمكن أن تزيد هذا الوضوح أكثر. ركزوا على مثبطات MEK، وهي فئة من الأدوية التي تعيق مسار إشارة نمو نشطًا كثيرًا في سرطان البنكرياس. في خطوط خلايا سرطان البنكرياس لدى الفئران وفي أورام نمت في فئران وفي نماذج مُستَنسَخة من مرضى، أدت مثبطات MEK إلى زيادة MHCI على سطح خلايا الورم التي تعبر عن GATA6 بمستويات عالية، مما يجعلها أهدافًا أفضل محتملة لخلايا T. عندما عولجت أورام ذات GATA6 عالٍ بمثبطات MEK في الفئران، تباطأ نمو الورم، ارتفع مستوى MHCI، ودخلت الأورام مزيد من خلايا CD8 الحاملة لجزيئات سامة خلوية. إن تعطيل GATA6 مباشرة، إما بحذف الجين أو بتحلل البروتين بسرعة، ألغى هذه الزيادة في MHCI الناجمة عن مثبط MEK والسيطرة على الورم الناتجة عنها، مما يبرهن أن GATA6 أساسي لهذا الأثر المفيد.
كيف تتكيف الأورام: الانزلاق إلى حالة أصعب في القتل
ومع ذلك، جاءت القصة مع تطور مفاجئ. المعالجة طويلة الأمد بمثبطات MEK دفعت العديد من خلايا الورم إلى الانتقال من الحالة الطلائية الإيجابية لـGATA6 إلى حالة أكثر ميزنكيمية ومنخفضة GATA6 مرتبطة بمقاومة العلاج. في كلٍ من نماذج الفئران والنماذج المستمدة من المرضى، أظهرت الأورام المعالجة بمثبطات MEK في نهاية المطاف خلايا أقل إيجابية لـGATA6، ومؤشرات أكثر على الانتقال الطلائي إلى الميزنكيمية، وفائدة إجمالية أقل دوامًا. رغم أن الخلايا الفردية الإيجابية لـGATA6 كانت لا تزال ترفع MHCI استجابةً للدواء، فإن تقلص حجم هذه الفئة حدَّ من التحسن الكلي في عرض مولدات الورم، مما يساعد على تفسير سبب خيبة أمل مثبطات MEK وحدها في التجارب السريرية لسرطان البنكرياس.
أدوية فوق جينية تُبقي الأورام في الحالة الضعيفة
لمواجهة هذا الهروب التكيفي، لجأ الباحثون إلى مثبطات نزع الأسيتيل عن الهيستون، أو مثبطات HDAC، وهي فئة من الأدوية فوق الجينية المعروفة بتأثيرها على هوية الخلايا ووضوحها المناعي. في مزروعات خلوية ونماذج فئران، أعاد الجمع بين مثبطات MEK ومثبطات HDAC من الفئة I مثل الدوماتينوستات التعبير عن GATA6 الذي كَفَّته مثبطات MEK، وأعاد مَنعَ العلامات الدالة على الانتقال الطلائي إلى الميزنكيمية، وزاد أكثر من مستويات MHCI على خلايا الورم. والأهم من ذلك، أن هذا العلاج المركب أدى إلى تغلغل وتنشيط أقوى لخلايا CD8 ومزيد من موت خلايا الورم في أورام الفئران المزوَّعة في موضعها وفي نموذج فأري معدل وراثيًا يحاكي سرطان البنكرياس البشري عن قرب. أزال استنفاد خلايا CD8 معظم الفائدة، مما يؤكد أن الفاعلية الأساسية لهذا المزيج قائمة على تمكين خلايا T القاتلة.
نحو علاجات مركبة أذكى لسرطان عنيد
بجمع هذه النتائج، تقترح الدراسة استراتيجية تستخدم مثبطات MEK المستهدفة ومثبطات HDAC فوق الجينية معًا لتثبيت حالة خلوية ورمية يقودها GATA6، غنية بمستضد MHCI وبالتالي سهلة التعرف عليها من قبل الجهاز المناعي. من خلال زيادة عدد الخلايا الإيجابية لـGATA6 وتعزيز «أعلام» MHCI الخاصة بها، يعزز هذا المزيج تغلغلًا أعمق لخلايا CD8، ونشاطًا سمًّا أقوى، وبقاؤًا أطول في نماذج فأرية عدوانية لسرطان البنكرياس. وبينما يمكن أن تحمل مثبطات HDAC آثارًا جانبية مهمة والعمل ما زال قبل سريري، تشير هذه الأبحاث إلى نهج علاجي مستقبلي قد يُقرن أدوية مستهدفة للمسارات مع معدِّلات فوق جينية مختارة بعناية لجعل أورام البنكرياس أكثر عرضة لدفاعات الجسم المناعية. 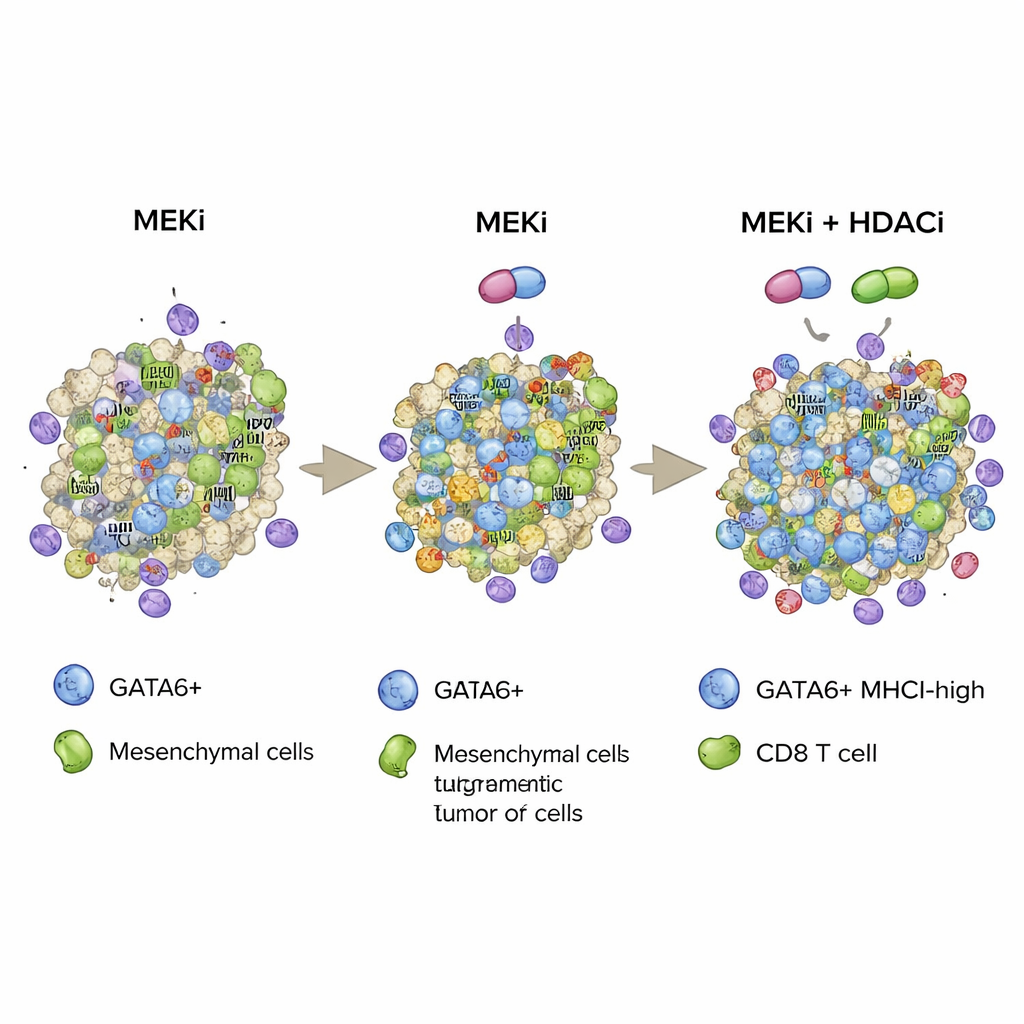
الاستشهاد: Peng, J., Yang, J., Antonopoulou, G. et al. Combined targeted and epigenetic-based therapy enhances antitumor immunity by stabilizing GATA6-dependent MHCI expression in pancreatic ductal adenocarcinoma. Nat Commun 17, 1476 (2026). https://doi.org/10.1038/s41467-026-69013-y
الكلمات المفتاحية: سرطان البنكرياس, مناعة الورم, GATA6, مثبط MEK, مثبط HDAC