Clear Sky Science · ar
المصفوفة خارج الخلوية تُسهِم في تجمع الخلايا الورمية الدائرة في انتقال سرطان الثدي ثلاثي السلبي
كيف تتكاتف خلايا سرطان الثدي المارقة في مجرى الدم
عند انتشار سرطان الثدي، يحدث ذلك غالبًا لأن خلايا سرطانية منفردة تنفلت إلى مجرى الدم وتؤسس أورامًا في أعضاء بعيدة. تطرح هذه الدراسة سؤالًا بسيطًا في ظاهره لكنه ذا تداعيات كبيرة: كيف تتمكن أكثر خلايا سرطان الثدي عدوانية، التي فقدت «اللاصق» التقليدي الذي يجعلها تتماسك، من السفر على شكل تجمعات محكمة — ولماذا يجعلها ذلك قاتلة أكثر؟
غطاء سكري لزج يحلّ محل اللزوجة الخلوية التقليدية
ركز المؤلفون على سرطان الثدي ثلاثي السلبي (TNBC)، وهو نوع عدواني يميل إلى طرح خلايا ورمية دائرة (CTCs) في الدم. في كثير من السرطانات، تكون تجمعات CTCs أكثر قدرة على إحداث انبثاثات من الخلايا المفردة. عادةً تُحْفَظ هذه التجمعات بواسطة وصلات التلاصق الظهارية — تجمعات بروتينية خاصة تعمل كـ «مسمار» جزيئي بين الخلايا المتجاورة. لكن خلايا TNBC تفقد في كثير من الأحيان بروتينات هذه الوصلات، مما يثير مفارقة: بدون الغراء التقليدي، ما الذي يُبقي تجمعاتها متماسكة؟ من خلال تفحّص قواعد بيانات جينية كبيرة للسرطان، وجد الباحثون أن أورام TNBC غنيةً بجينات مرتبطة بالهياكل الخارجية للخلية المعروفة بالمصفوفة خارج الخلوية. برز جين واحد، HAS2، الذي يصنع إنزيمًا ينتج الهيالورونان (HA)، وهو بوليمر سكري طويل يغطي الخلايا. كانت مستويات عالية من HAS2 وHA مرتبطة بقوة بملامح أورام عدوانية وقابلة للانبثاث.
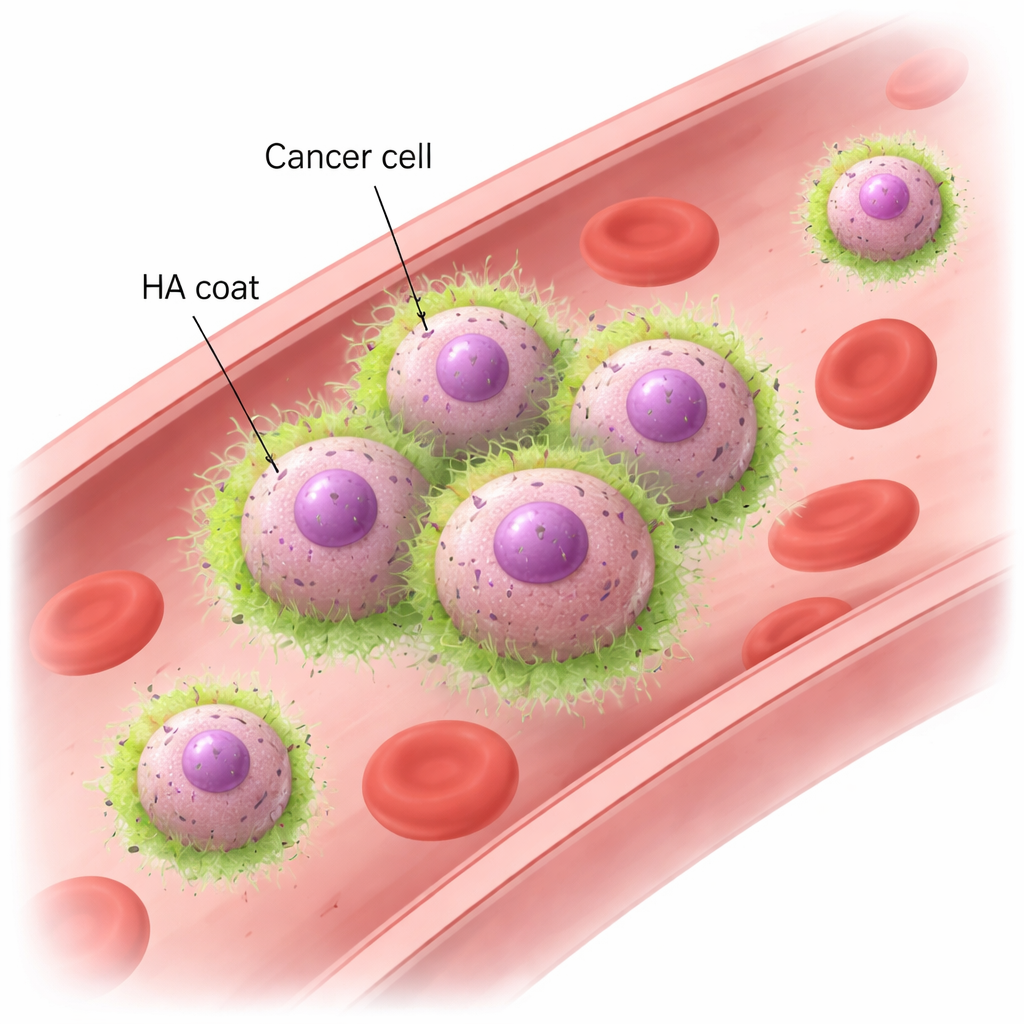
الهيالورونان وCD44: طريقة جديدة للخلايا لتتشابك
باستخدام نماذج فأرية وسلالات خلوية بشرية لسرطان الثدي، أظهر الفريق أن خلايا TNBC المسببة للانبثاث تشكّل تجمعات بسرعة عند تعريضها لسائل دوّار يحاكي تدفق الدم. تبقى هذه التجمعات متماسكة حتى تحت قوى مماثلة لتلك في الأوعية الدموية الحقيقية، بينما تتفتت خلايا سرطان الثدي الأقل عدوانية وتنجرف كخلايا مفردة. أظهرت الميكروسكوبية أن الخلايا المسببة للانبثاث ملفوفة بـ«غطاء» HA يصبح مركزًا بالضبط عند مواضع اتصال الخلايا ببعضها. إزالة HA بواسطة إنزيمات، أو خفض تعبير HAS2، جعل الخلايا تفقد قدرتها على التجمع تحت التدفق، على الرغم من أنها ما زالت تستطيع الترسب معًا عند تركها ساكنة. الشريك الأساسي على سطح الخلية هو CD44، مستقبل سطحي شائع يرتبط بـHA. الخلايا التي تفتقر إلى CD44 لم تعد قادرة على الاحتفاظ بـHA على سطحها أو تشكيل تجمعات. وعلى العكس، اكتسبت خلايا غير متجمعة معدّة وراثيًا لإنتاج كل من HAS2 وCD44 قدرة قوية على التجمع. أظهرت هذه التجارب أن تفاعل HA مع CD44 ضروري وكافٍ لجعل الخلايا السرطانية تلتصق ببعضها في دم متحرك بسرعة.
نتوءات دقيقة وأقفال ميكانيكية تبني تجمعات قوية
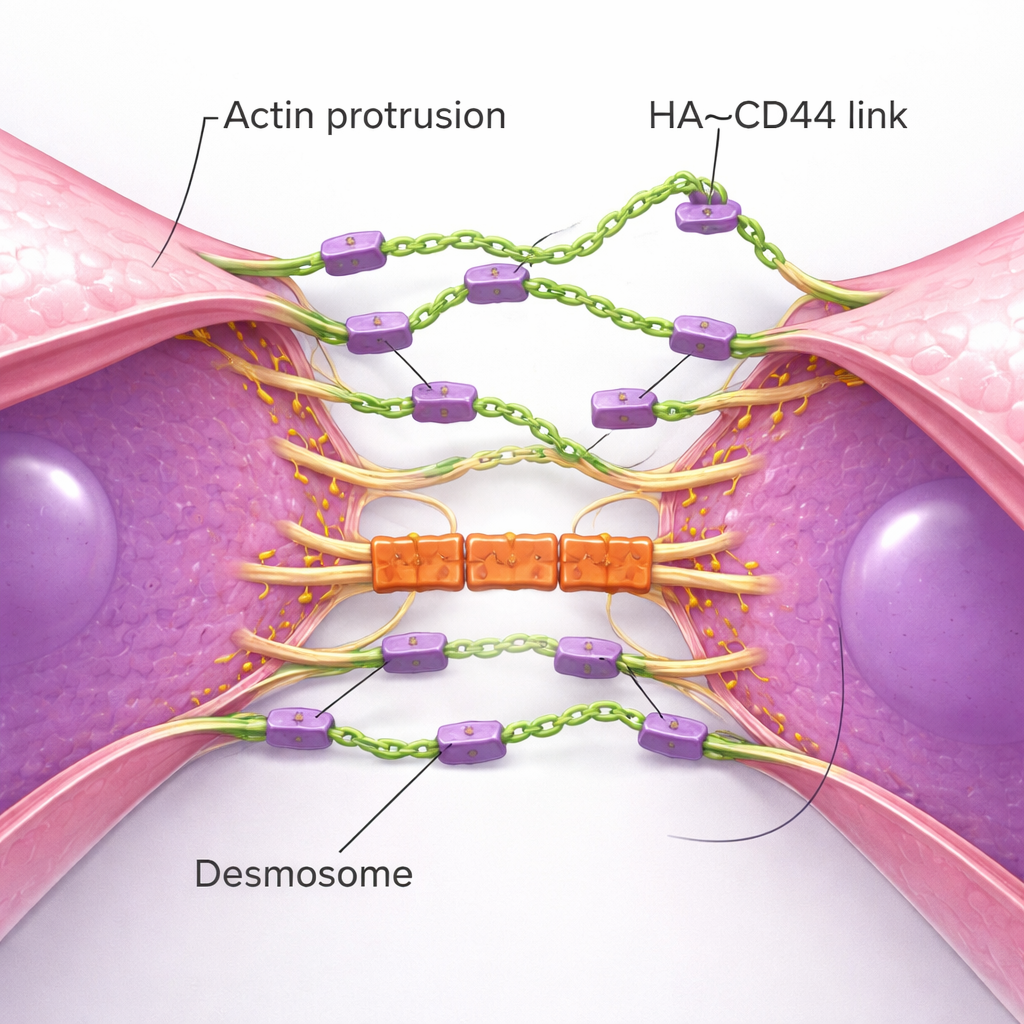
كشفت التصويرات عالية الدقة عن الرقصة الفيزيائية لكيفية تكوّن التجمعات. تُمدد خلايا TNBC المفردة العديد من النتوءات الرقيقة القائمة على الأكتين — شبيهة بمجسات — المحشوة بـCD44 والمُطهَّمة بقِمم من HA. عندما تقترب خليتان، تلتقي هذه المجسات أولًا من كل طرف، مُشكِّلة جسورًا أولية من HA–CD44. مع مرور الوقت، تنزلق النتوءات جنبًا إلى جنب، جاذبةً أجساد الخلايا الكاملة حتى تستوي مساحات واسعة من الأغشية قرب بعضها البعض. يذكّر هذا العملية بكيفية بناء الخلايا الظهارية الطبيعية لوصلات التلاصق، لكن هنا تدفعها طبقة سكرية مرنة بدلًا من سلاسل بروتينية صلبة. ومع نضوج منطقة الاتصال، تنضم مجموعة أخرى من البنى: الديسموزومات، وصلات قوية تربط الأغشية الخلوية بالهيكل الداخلي. تتراكم بروتينات الديسموزوم فقط بعد تأسيس الاتصال المعتمد على HA وتعمل كـ «أقفال» ميكانيكية تساعد التجمعات على مقاومة قوى التمزق في تدفق الدم. عندما انخفضت مكونات الديسموزوم، تكوّنت التجمعات لكنها انقسمت عند إجهاد قصّي أعلى.
لماذا يهم التجمع للبقاء والانبثاث
تبين أن نظام التجمع المعتمد على HA أكثر من وسيلة للبقاء مترابطًا؛ فقد عزز البقاء مباشرة. تحت تدفق دم محاكٍ مطول، أظهرت التجمعات الغنية بـHA مستويات أقل بكثير من أنواع الأكسجين التفاعلية الضارة ومعدلات وفاة خلوية أقل بكثير من الخلايا المفردة المحرومة من HA. في نماذج الفئران، أنتجت خلايا TNBC التي تفتقر إلى HAS2 عددًا أقل بكثير من CTCs، وشكّلت تجمعات صغيرة فقط، وأدت إلى عدد أقل بكثير من الانبثاثات الرئوية — رغم أن أورامها الأولية نمت بنفس القدر. عندما تم حقن تجمعات مُكوَّنة مسبقًا من خلايا ضابطة وخلايا ناقصة HAS2 في الفئران، كانت الخلايا الفقيرة من HA أقل احتمالًا بكثير لاستعمار الرئتين بنجاح. علاوة على ذلك، استطاعت CTCs المغطاة بـHA «استقطاب» خلايا أخرى — سواء خلايا سرطانية افتقرت للـHA أو خلايا مناعية طبيعية مثل العدلات — إلى تجمعات مختلطة، بشرط أن تعبّر تلك الشركاء عن CD44. أظهرت عينات دم مرضى من نساء مصابات بـTNBC النقيلي نفس النمط: غالبًا ما حملت CTCs غطاء HA، مع تجمع HA عند نقاط الاتصال بين الخلايا الورمية وبين الخلايا الورمية وغير الورمية.
ما الذي يعنيه هذا للمرضى والعهود العلاجية المستقبلية
لغير المتخصص، الخلاصة الأساسية هي أن بعض أخطر خلايا سرطان الثدي لا تسافر كمنفردين بل كفرق صغيرة متعاونة تمسكها طبقة خارجية سكرية ومستقبلها، بدلًا من «المسامير» الخلوية التقليدية الموجودة في الأنسجة الطبيعية. يساعد هذا النظام المعتمد على HA–CD44 الخلايا الورمية على النجاة في وجه تدفق الدم القاسي، والانضمام إلى بعضها البعض وإلى خلايا دم داعمة، وزرع أورام جديدة في أعضاء بعيدة بكفاءة أكبر. إن استهداف إنتاج HA (على سبيل المثال، عن طريق تثبيط HAS2) أو حجب تفاعله مع CD44 قد يضعف هذه التجمعات ويصعّب انبثاث TNBC، ما يقدم زاوية جديدة للعلاجات المضادة للانبثاث في المستقبل.
الاستشهاد: Bobkov, G.O., Patel, K.J., Lege, B.M. et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis. Nat Commun 17, 1352 (2026). https://doi.org/10.1038/s41467-026-69007-w
الكلمات المفتاحية: سرطان الثدي ثلاثي السلبي, الخلايا الورمية الدائرة, الهيالورونان, CD44, الانبثاث