Clear Sky Science · ar
الإشريكية القولونية تعزز نقائل سرطان القولون والمستقيم عبر الحفاظ على حلقات المحفِّز-المروِّج من خلال إطلاق شَبَكات خلايا العدلات خارج الخلوية
الميكروبات المعوية والطريق السري للسرطان
غالبًا ما يقتل سرطان القولون والمستقيم ليس بسبب الورم الأصلي في الأمعاء، بل لأن خلايا السرطان تنتقل إلى الكبد وتستقر هناك. تكشف هذه الدراسة عن متواطئ غير متوقع في تلك الرحلة: بكتيريا معوية شائعة، الإشريكية القولونية. من خلال تتبع سلسلة الأحداث من البكتيريا في الأمعاء إلى الأورام العدوانية في الكبد، يوضح الباحثون كيف يمكن للميكروبات وخلايا المناعة وبنية الحمض النووي داخل الخلايا السرطانية أن تتعاون لتغذية عملية النقائل—ويقترحون طرقًا جديدة لقطع هذه السلسلة.
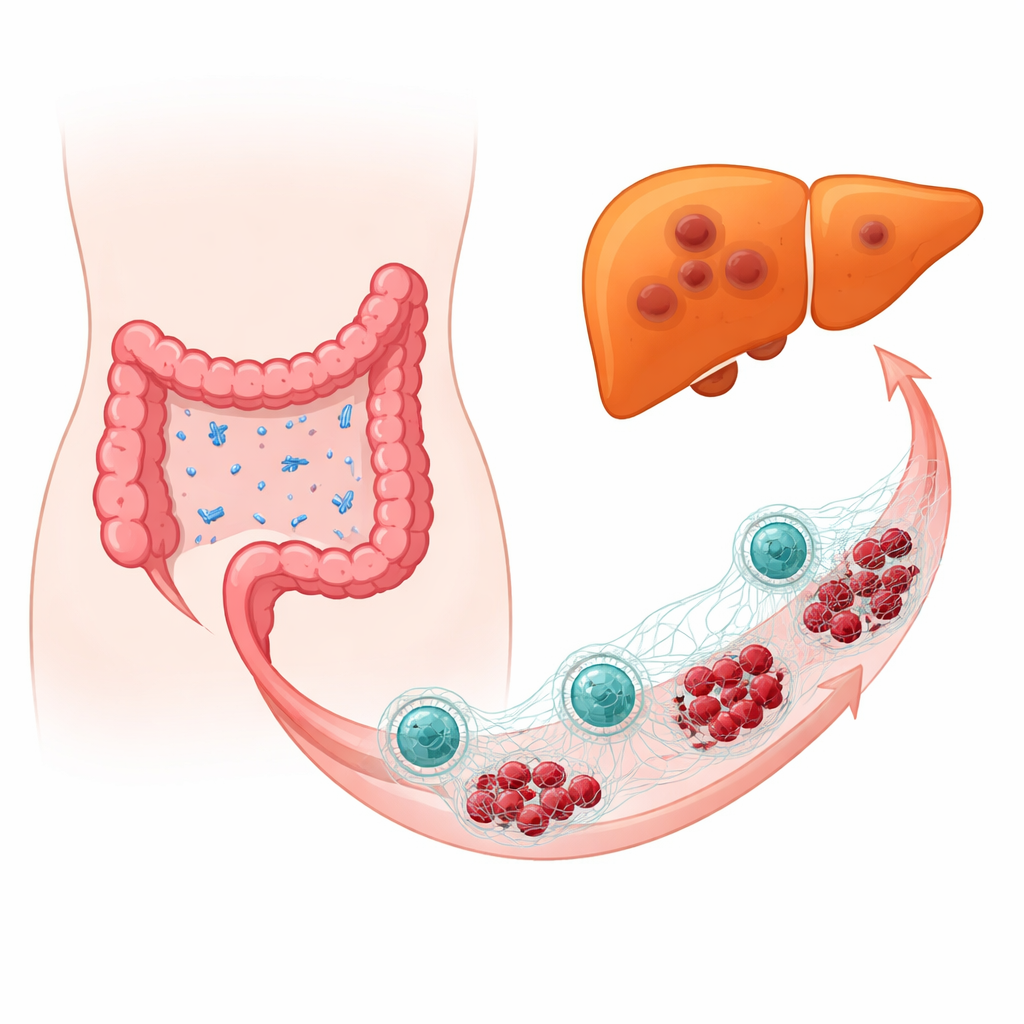
عندما تتحول البكتيريا الصديقة إلى معادية
فحص الفريق عينات أورام من أشخاص مصابين بسرطان القولون والمستقيم، مقارنًين بين من انتشر لديهم السرطان إلى الكبد ومن لم ينتشر لديهم. باستخدام تحليل دقيق معتمد على الحمض النووي لوصف الميكروبات، وجدوا أن الإشريكية القولونية كانت أكثر وفرة بكثير في الأورام التي سبق وأن زرعت نقائل في الكبد. في نماذج الفئران وفي فئران ذات أجهزة مناعية مخصصة للإنسان، أدى إدخال الإشريكية القولونية عمدًا بالقرب من أورام القولون والمستقيم إلى زيادة حجم وتواتر نقائل الكبد، ودفع خلايا الورم نحو حالة أكثر حركة وغزوًا. حتى عندما أُزيل معظم الفلورا المعوية الطبيعية بالمضادات الحيوية وأُعيد إدخال الإشريكية القولونية وحدها، بقيت البكتيريا قادرة على تعزيز نمو الورم وانتشاره، مما يشير إلى دور الإشريكية القولونية نفسها بدلاً من اضطراب عام في الميكروبيوم.
شبكات مناعية تساعد السرطان على الهروب
برزت العدلات—الخلايا المناعية الطليعية التي عادةً ما تحاصر وتقتل الميكروبات—كوسطاء حاسمين. استجابةً للإشريكية القولونية، أطلقت العدلات هياكل شبيهة بالشبكة تُسمى شَبَكات خارج الخلوية، مكونةً من حمض نووي وبروتينات سامة. هذه الشَبكات مُصمَّمة لالتقاط البكتيريا، لكن في هذا السياق حمت الخلايا السرطانية وأعطتها قوة غير مقصودة. عندما حلل الباحثون هذه الشبكات بالإنزيمات أو عرقلوا إنزيمات رئيسية لازمة لتكوينها، تقلصت نقائل الكبد وبدت الأورام أقل عدوانية. كما أن استنفاد العدلات أعطى تأثيرًا وقائيًا مشابهًا، مما يشير إلى مفارقة: رد فعل مناعي يفترض أن يحارب العدوى قد تم اختطافه لمساعدة السرطان على الانتشار.
من إشارات كهربائية إلى مفاتيح جينية
كيف يمكن لشَبَكات الحمض النووي اللزجة خارج الخلية أن تغيّر ما يحدث داخل النواة بعمق؟ يكمن الجواب في الكالسيوم، الأيون البسيط الذي يعمل كإشارة كهربائية داخل الخلايا. أظهرت الدراسة أن شَبَكات العدلات زادت مستوى بروتين قناة، TRPC1، على خلايا سرطان القولون والمستقيم. سمحت TRPC1 بدخول كميات إضافية من الكالسيوم إلى الخلية، مما فعّل منظمًا حساسًا للكالسيوم يُدعى NFATC3 وخلق حلقة تغذية راجعة حافظت على مستويات TRPC1 مرتفعة. هذا الطوفان الكلسي شجّع بروتينين صغيرين، S100A8 وS100A9، على الالتحام ثم الارتباط ببروتين رئيسي ضابط للنمو هو STAT3. انتقلت الثلاثية إلى النواة، حيث قامت بشيء لافت للنظر: ساعدت على ثني ولفّ الحمض النووي بحيث تلامست مناطق تنظيمية بعيدة مع مواقع بدء الجينات، مثبتةً ماديًا «حلقات المحفِّز–المروّج» التي ترفع مستوى تعبير جينات معيّنة.
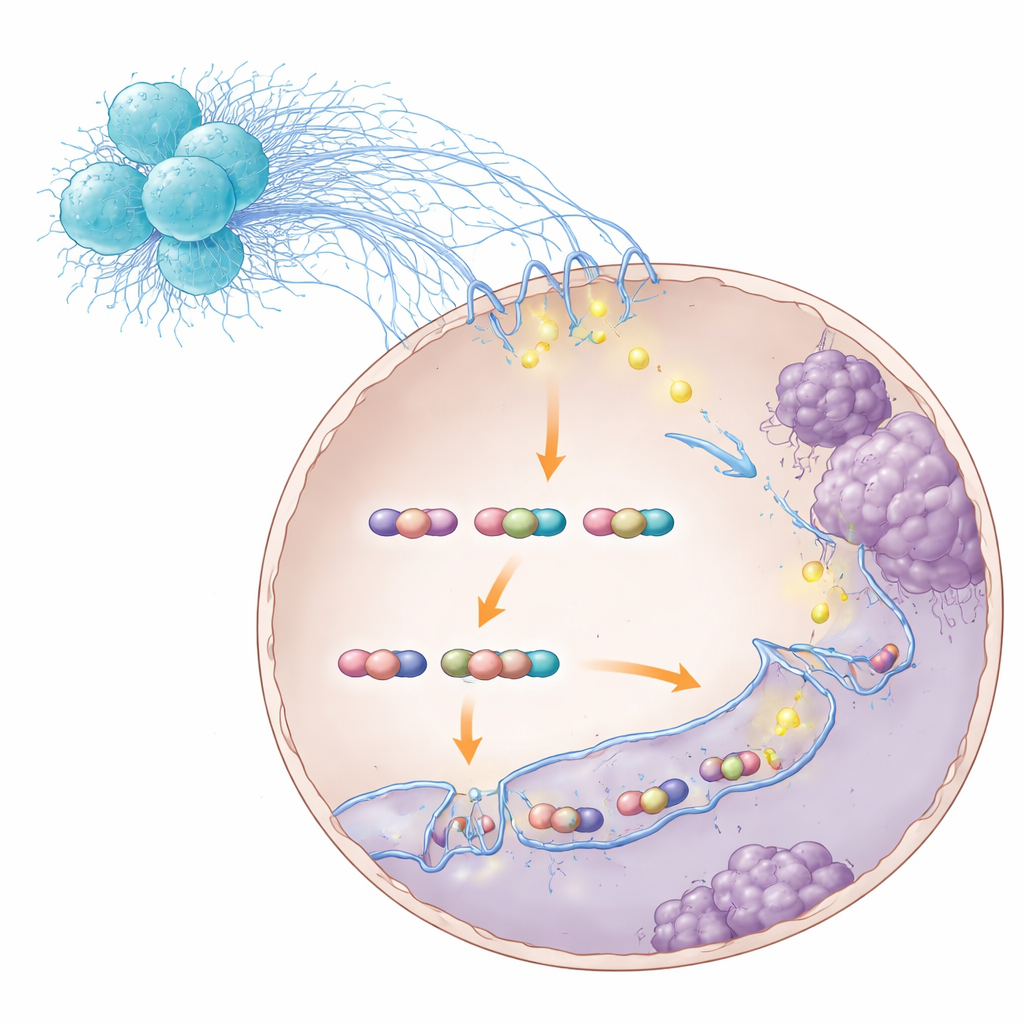
إعادة توصيل خلايا السرطان لصالح النقائل
من خلال رسم الاتصالات ثلاثية الأبعاد على طول الجينوم، وجد الباحثون أن مركب STAT3–S100A8/9 شجع حلقات تفضّل جينات متورطة في حركة الخلايا والغزو. كان أحد الجينات البارزة هو TNS1، الذي يدفع الخلايا إلى تخفيف روابطها والتنقل بسهولة أكبر. عندما تعطل مركب STAT3–S100A8/9، ضعفت أو اختفت الكثير من هذه الحلقات، انخفضت مستويات TNS1، وفقدت الخلايا السرطانية جزءًا من قدرتها على الغزو وزرع الكبد. ومن المهم أن هذا التعطيل لم يمنع STAT3 من الارتباط بالحمض النووي تمامًا—بل زعزع بنية الحلقات التي كانت تضخّم برامج النقائل. في نماذج حيوانية، أدى حجب خطوات مختلفة في هذه السلسلة—من جزيء إشارة بكتيري مثل RIPK2 في العدلات، إلى S100A8/9، إلى STAT3 نفسه—إلى تقليل نقائل الكبد وتحسين البقاء على قيد الحياة.
قطع الحلقة بين الجراثيم والأورام
للغير متخصصين، الرسالة الأساسية هي أن بكتيريا معوية شائعة قادرة على مساعدة سرطان القولون والمستقيم على الانتشار عبر إثارة خلايا مناعية لإلقاء شَبَكات حمض نووي، ثم استخدام تلك الشَبَكات لدفع تتابع معتمد على الكالسيوم يعيد برمجة كيفية تشغيل جينات السرطان. بدلًا من الاعتماد على مضادات حيوية واسعة الطيف، التي قد تضر بالميكروبات المفيدة وتقلل فاعلية العلاج المناعي للسرطان، تشير هذه النتائج إلى أهداف دوائية أدق: حسّاسات بكتيرية مثل RIPK2، سلسلة TRPC1–الكالسيوم–S100A8/9، وحلقات الحمض النووي التي يقودها STAT3 وتُبقي جينات متعلقة بالنقائل في وضعية تشغيل مرتفعة. قد يوفّر قطع هذه السلسلة في نقطة أو أكثر استراتيجية جديدة لمنع تحول سرطان القولون والمستقيم من مشكلة محلية في الأمعاء إلى مرض قاتل في الكبد.
الاستشهاد: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
الكلمات المفتاحية: نقائل سرطان القولون والمستقيم, الميكروبيوم المعوي, شَبَكات العدلات خارج الخلوية, إشارة STAT3, تنظيم الجينات عبر التغيرات فوق الجينية