Clear Sky Science · ar
تصميم مثبط تساهمي يمنح نشاطًا ضد صيغتي KRAS G12C المرتبطتين بـGDP وGTP
لماذا هذا مهم لعلاجات السرطان المستقبلية
لطالما اعتُبرت الأورام السرطانية الناتجة عن طفرات في جين يُدعى KRAS من بين الأصعب علاجًا. مؤخرًا، وصلت أدوية جديدة تُعطّل أحد الأشكال الطافرة الشائعة، KRAS G12C، إلى المرضى وبدأت تغيّر هذه الصورة. تستكشف هذه الورقة فكرة أكثر طموحًا: هل يمكننا تصميم أدوية تحجب KRAS G12C في كلا وضعي التشغيل الرئيسيين داخل الخلية، وهل سيجعل ذلك علاج السرطان أسرع أو أقوى أو أكثر دوامًا؟
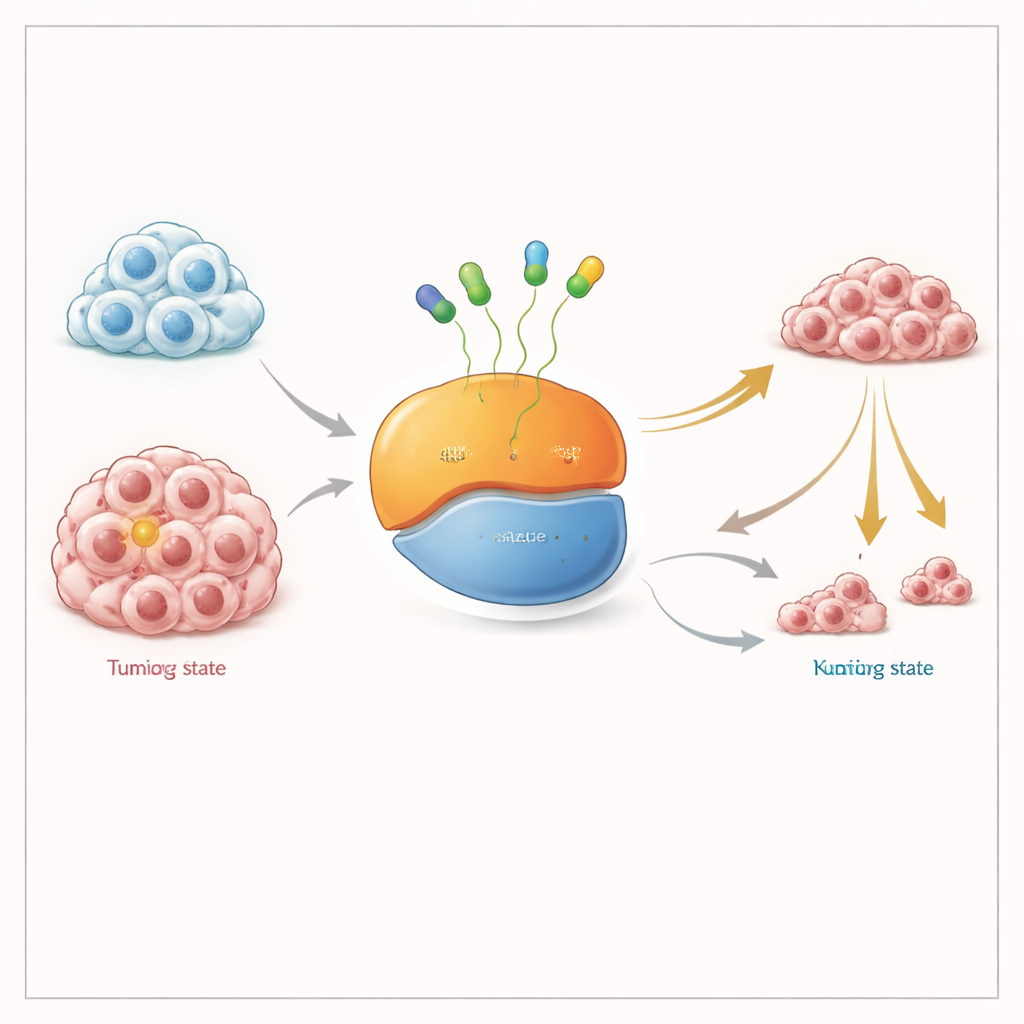
إيقاف مفتاح جزيئي في موضعين
يعمل بروتين KRAS كمفتاح صغير لتشغيل إشارات نمو الخلايا. ينتقل بين حالة «إيقاف» حيث يرتبط بجزيء ناقل للطاقة يدعى GDP، وحالة «تشغيل» حيث يحمل جزيئًا آخر هو GTP. تبقي طفرة KRAS G12C هذا المفتاح في حالة تشغيل جزئية وتغذي نمو الورم. الأدوية الحالية المعتمدة من إدارة الغذاء والدواء ترتبط بالشكل غير النشط وتثبّته؛ ومع مرور الزمن، ومع دوران المزيد من KRAS عبر ذلك الشكل، يتعطل المخزون الإجمالي للبروتين الطافر. جادل كثير من العلماء بأن دواءً قادرًا على التقاط KRAS في كلا الحالتين، النشطة وغير النشطة، ينبغي أن يكون أكثر فعالية، خاصة في الأورام التي تتكيّف عن طريق إبقاء المزيد من KRAS في الحالة النشطة.
تصميم نوع جديد من الخطاف الجزيئي
انطلق الباحثون لبناء مثل هذه الأدوية متعددة الأغراض. ركزوا على شق صغير بجوار منطقة مرنة في KRAS تُسمى Switch II، حيث ترتبط الأدوية الحالية بالفعل. بدلاً من تغيير مدى تماسك جزيئاتهم داخل ذلك الشق، أعادوا تصميم جزء «رأس الحرب» الذي يُكوّن رابطة كيميائية دائمة مع السيستئين الطافر في الموضع 12. من خلال النمذجة الحاسوبية وتخليق عشرات المتغيرات، اكتشفوا رأس حربٍ ذا ثلاثة أجزاء يقترب من السيستئين بزاوية مختلفة قليلاً. هذا التحول الطفيف يخلق مساحة كافية للجزيء الأكبر GTP، مما يسمح للمركبات الجديدة بالارتباط بـKRAS سواء حمل GDP أو GTP. أكدت الاختبارات البيوكيميائية أن المركبات الرائدة يمكنها تعطيل شراكة KRAS مع شريك إشاراتي رئيسي، RAF، في كلتا الحالتين.
رؤية كيف يعيد البروتين تشكيل نفسه
لفهم سبب فعالية هذه الجزيئات، حدّد الفريق هياكل بلورية عالية الدقة للمُثبط مرتبطًا بـKRAS. أظهرت هذه اللقطات أن رأس الحرب الجديد يتفاعل في موقع غير اعتيادي على السقالة الكيميائية، مسببًا انفصال ذرة فلور وتكوين رابطة تساهمية عند كربون مختلف عن مثبطات السرطان النموذجية التي تستهدف السيستئين. تساعد هذه الكيمياء المعدلة الدواء على الالتحام بجيب Switch II حتى عندما يكون GTP حاضرًا. كما كشفت البُنى أن ارتباط المُثبط يدفع جزيء ماء صغيرًا ويُعيد ترتيب حلقة أخرى بدقة، Switch I، التي تتلامس عادة مع البروتينات الناقلة للإشارة الأسفلية. يُحدث هذا التشكيل «الكلوستيري» سحبًا لحمضين أمينيين معًا لتكوين جسر ملحي محكم، مشوِّهًا السطح بحيث لا تستطيع RAF الالتحام وتمرير إشارات النمو.
إيقاف سريع، لكن لا تأثير طويل الأمد أقوى
مسلحين بهذه الرؤى البنائية، صقّل الباحثون جزيئين رائدين يلتصقان بكفاءة وانتقائية بـKRAS G12C، مع تجنُّب كبير لباقي البروتينات الحاوية على سيستئين. في خطوط خلايا سرطانية، أغلقت هذه المثبطات ذات الحالتين بسرعة ناقل إشارة رئيسي يُعرف بمسار MAPK، كما ظهر بقياس فقدان وسم كيميائي على بروتين ERK وكبح قوي لنمو الخلايا. أعطلت KRAS داخل الخلايا أسرع من دواء مرجعي يستهدف الحالة غير النشطة فقط. في نماذج أورام الفئران، أظهر مركب رائد توافرًا فمويًا جيدًا، وشكل روابط تساهمية سريعًا مع الهدف، وصغّر الأورام أو أبطأ نموها. ومع ذلك، عندما قارن الفريق بين مثبطات ذات الحالتين وأخرى تستهدف الحالة غير النشطة على مدى أطول، حققت الفئتان في النهاية مستويات مماثلة من تعطيل KRAS، وكبت المسار، والسيطرة على الورم.
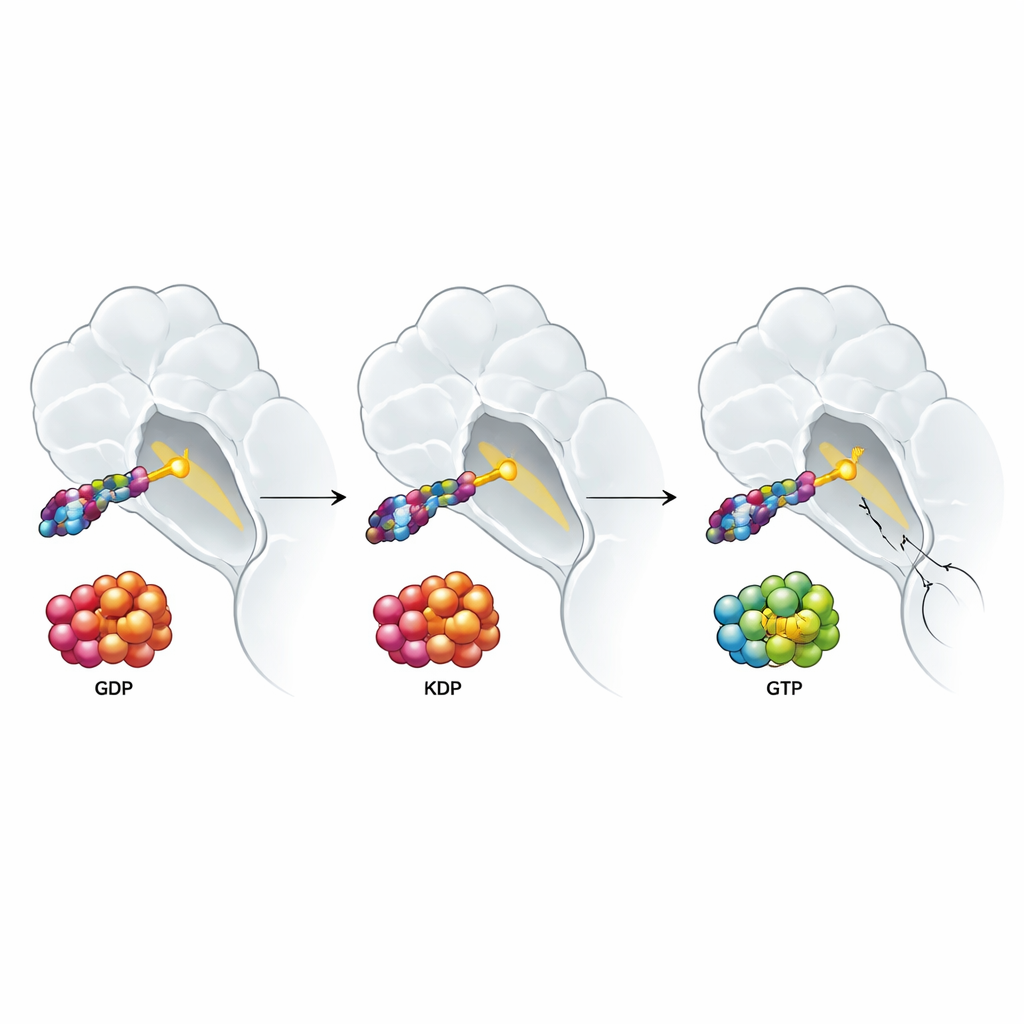
لماذا تفوز إشارات النمو من المحيط السرطاني
استقصت الدراسة أيضًا كيف تؤثر الإشارات من بيئة الورم على أداء هذه الأدوية. عوامل نمو مثل EGF وHGF، الشائعة حول العديد من الأورام، تدفع بروتينات RAS نحو الشكل النشط المحمّل بـGTP ومعروفة بأنها تخفف استجابة العلاجات الموجهة. قد يتوقع المرء أن دواءً يرتبط بالشكل النشط لـKRAS G12C سيتجنب هذه المشكلة. لكن المؤلفين وجدوا أن كلًا من المثبطات متعددة الحالتين وتلك الموجهة للحالة غير النشطة فقدت فعاليتها عند وجود مثل هذه عوامل النمو. أشارت تجارب مفصلة إلى سبب مفاجئ: تنشيط أشكال RAS الطبيعية غير المطافرة (H‑RAS وN‑RAS)، والتي يمكنها تجاوز KRAS G12C ومواصلة تدفق إشارات النمو. عندما حذف الباحثون H‑RAS وN‑RAS في خط خلية سرطان رئة، اختفت مقاومة عوامل النمو إلى حد كبير لكل أنواع أدوية استهداف KRAS G12C، بينما كان الدواء الذي يعيق خطوة أسفل الطريق الإشارية أقل تأثرًا في الأساس.
ماذا يعني هذا للمرضى وتطوير الأدوية
بشكل عام، تُظهر هذه الدراسة أنه من الممكن كيميائيًا وبنيويًا بناء أدوية تساهمية تستهدف KRAS G12C وتلتقط البروتين في حالتيه النشطة وغير النشطة، وأن هذه المثبطات ذات الحالتين قادرة على إيقاف الإشارة بسرعة أكبر من الأدوية الحالية. ومع ذلك، لم يتحول هذا الارتباط السريع إلى تحكم واضح أفضل في الورم أو حل لمشكلة مقاومة عوامل النمو في النماذج ما قبل السريرية. بالنسبة للمرضى، يشير ذلك إلى أن مجرد إضافة نشاط ضد الشكل النشط من KRAS قد لا يكون كافيًا؛ قد تكون هناك حاجة إلى استراتيجيات تركيبية تعالج أيضًا أعضاء عائلة RAS الأخرى أو نقاطًا إشارية أدنى في المسار. مع ذلك، يوسع رأس الحرب الجديد والمخطط البنيوي المعروض هنا أدوات استهداف KRAS وسيلهم أجيالًا مستقبلية من علاجات السرطان الدقيقة.
الاستشهاد: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
الكلمات المفتاحية: KRAS G12C, مثبط تساهمي, تثبيط ذو حالتين, إشارة MAPK, مقاومة الدواء