Clear Sky Science · ar
دائرة محددة جزيئياً من القشرة البازالية‑القشرية الأمامية‑المهاد تنظم الأبعاد الحسية والعاطفية للألم في ذكور الفئران
لماذا تهم هذه الدائرة الدماغية للألم
الألم أكثر من مجرد وخزة حادة أو ألم خافت؛ فهو يحمل أيضاً حمولة عاطفية ويمكن أن يعيد تشكيل مزاجنا وسلوكنا لسنوات. كثير من مرضى الألم المزمن لا يحصلون على ارتياح كبير من الأدوية الحالية وغالباً ما يواجهون آثاراً جانبية خطيرة. تكشف هذه الدراسة في ذكور الفئران عن دائرة دماغية معرفة بدقة تساعد الدماغ على تضخيم الألم أو تهدئته، سواء من حيث شدة الإحساس أو مدى انزعاجه. من خلال وضع خريطة لهذه المسار والتحكم فيه، تشير النتائج إلى طرق جديدة وأكثر استهدافاً لتخفيف الألم المزمن دون الاعتماد فقط على المسكنات التقليدية.
طريق خفي من عقل التفكير إلى مركز الألم
ركز الباحثون على القشرة الجبهية الوسطى، منطقة أمامية من الدماغ تشارك في اتخاذ القرار والعاطفة والتحكم بالألم، وعلى المهاد، المركز العميق الواصل الذي يشكل كل من شدة وعدم راحة الألم. اكتشفوا أن مجموعة محددة من الخلايا في القشرة الجبهية الوسطى، تُميَّز بواسطة جين يُسمى Foxp2، تشكل مساراً خروجياً رئيسياً إلى المهاد. تقع هذه الخلايا بشكل أساسي في أعمق طبقة قشرية وتبث محاور طويلة إلى نوى مهادية معينة، بينما تتجاهل إلى حد كبير أهداف القشرة الجبهية الشائعة الأخرى. باستخدام طرق تتبع ورسم خرائط للدماغ بأكمله، أظهر الفريق أن الخلايا المعلمة بـ Foxp2 ترتبط بقوة بثلاثة مناطق مهادية معروفة بتأثيرها على معالجة الألم: نواة البراتاينيال، والمهاد الظهري المتوسط، والمهاد البطني الوسيط. 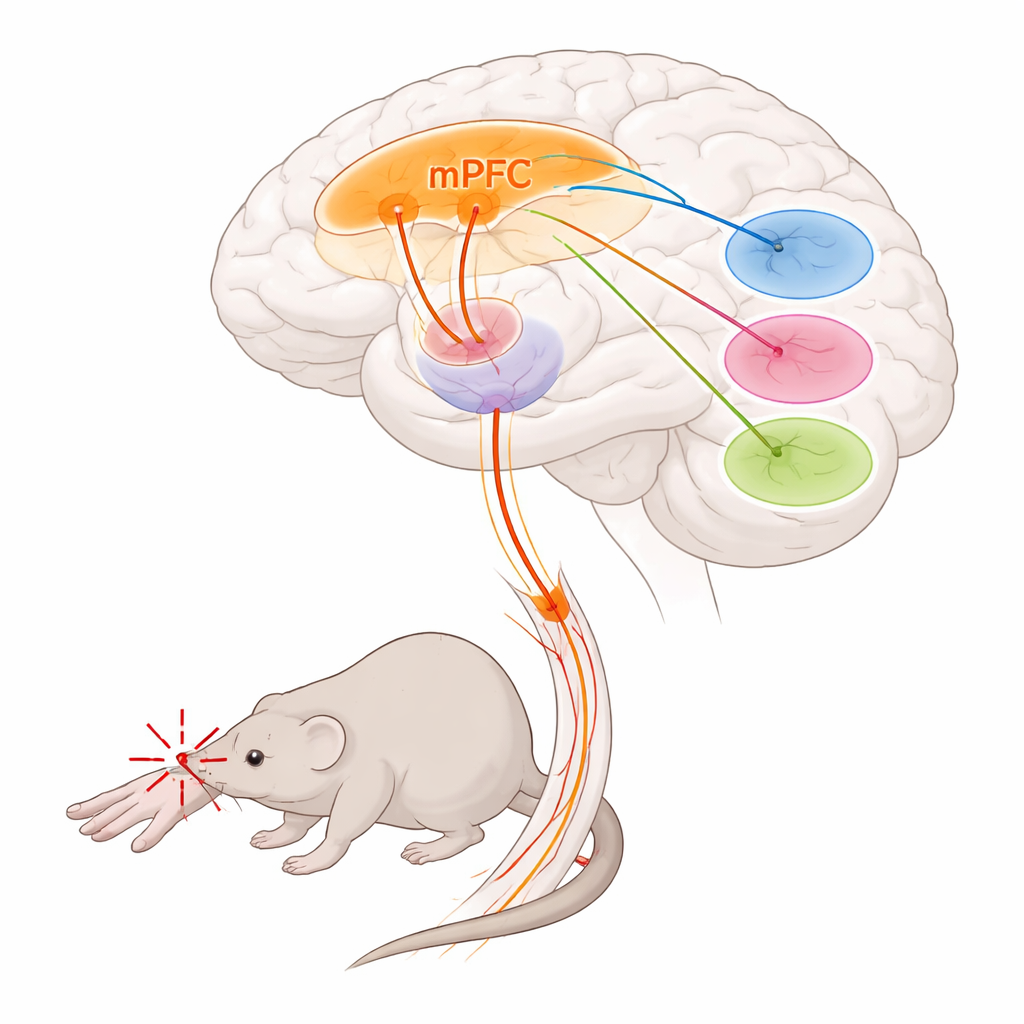
عند وقوع الألم، يهدأ مركز تحكم رئيسي
لمعرفة كيف يتصرف هذا المسار أثناء الألم، زرع العلماء عدسات دقيقة فوق القشرة الجبهية الوسطى وسجلوا نشاط خلايا Foxp2 مفردة في فئران يقظة. خلال قرصات ميكانيكية قصيرة، والألم الكيميائي المستحث بالفورمالين، والألم الالتهابي طويل الأمد، خفت نشاط هذه الخلايا باستمرار: أظهرت معظمها نوبات نشاط أقل أثناء الحلقات المؤلمة وفي الأيام التالية للإصابة الالتهابية. لم يكن هذا الصمت طفيفاً؛ ففي بعض الحالات أصبحت أكثر من ثلث إلى ما يقرب من نصف الخلايا أقل نشاطاً بشكل واضح. وتشير النتيجة إلى أن حالات الألم الحاد والمزمن قد تعكس، جزئياً، إسكات نظام فرملة قشري طبيعي كان سيساعد في كبح الألم لو بقي نشطاً.
تشغيل وإيقاف الدائرة يعيد تشكيل الألم
ثم تساءل الفريق عما إذا كان هذا الهدوء مجرد أثر جانبي للألم أو سبب له. باستخدام أدوات جينية، قاموا إما بحجب مخرج خلايا Foxp2 طويل الأمد أو زياد نشاطها لفترة وجيزة. أدت الخَفْض المستمر للنشاط إلى جعل الفئران أكثر حساسية للمس والحرارة، مما يشير إلى أن هذا المسار يقي عادة إشارات الألم الواردة. في المقابل، رفعت تنشيط قصير الأمد عتبة المؤثرات المؤلمة، وخفضت لعق الأطوار المتأخرة في اختبار الفورمالين (مقياس للألم الالتهابي المستمر)، وجعلت الفئران تفضل البيئات التي تم فيها تشغيل الدائرة، مؤشراً على تخفيف العبء العاطفي للألم. من خلال إضاءة فروع محددة من المسار، أظهر الباحثون أن الإسقاطات إلى المهاد البراتاينيال تقلل كل من الحساسية الجسدية واستجابات التأقلم، بينما تضبط الإسقاطات إلى المهاد الظهري المتوسط والمهاد البطني الوسيط بشكل أساسي الأبعاد العاطفية والسلوكية. تكشف هذه النتائج معاً عن مخطط توصيل مفصّل يقسم فيه فروع مختلفة من نفس مجموعة القشرة الأمامية التحكم في جوانب مختلفة من تجربة الألم.
الضبط الكيميائي: دفعة كولينرجية لتخفيف الألم
ما الذي يتحكم في هذه الخلايا القشرية المسؤولة عن تخفيف الألم؟ كشفت تجارب التتبع عن مدخلات قوية من منطقة كولينرجية في القاعدة الأمامية للدماغ تُسمى الشريط القطري الأفقي. العديد من الخلايا التي ترسل إشارات من هذه المنطقة إلى خلايا Foxp2 تستخدم الأستيل كولين، الناقل الذي يشارك في الانتباه والتنبيه. أدى تنشيط هذا الإسقاط الكولينرجى إلى خفض الحساسية الميكانيكية وسلوكيات التأقلم وهدأ فرط الحساسية الالتهابي، رغم أنه لم يغير بوضوح النبرة العاطفية السلبية للألم. على الجانب المستقبل، وُجد أن خلايا Foxp2 غنية بنوع معين من مستقبلات الأستيل كولين، المعروفة بمستقبل النيكوتين α4β2. أدى توصيل منبه انتقائي لمستقبل α4β2 مباشرة إلى القشرة الجبهية الوسطى إلى جعل الفئران أقل حساسية للحرارة واللمس المؤلمين، حتى في حالات الالتهاب المزمن، وعزز نشاط خلايا Foxp2. إزالة هذه الخلايا ألغت فائدة الدواء، مما يوضح أن هذا المستقبل يخفف الألم تحديداً من خلال إثارة هذا النوع الخلوي. 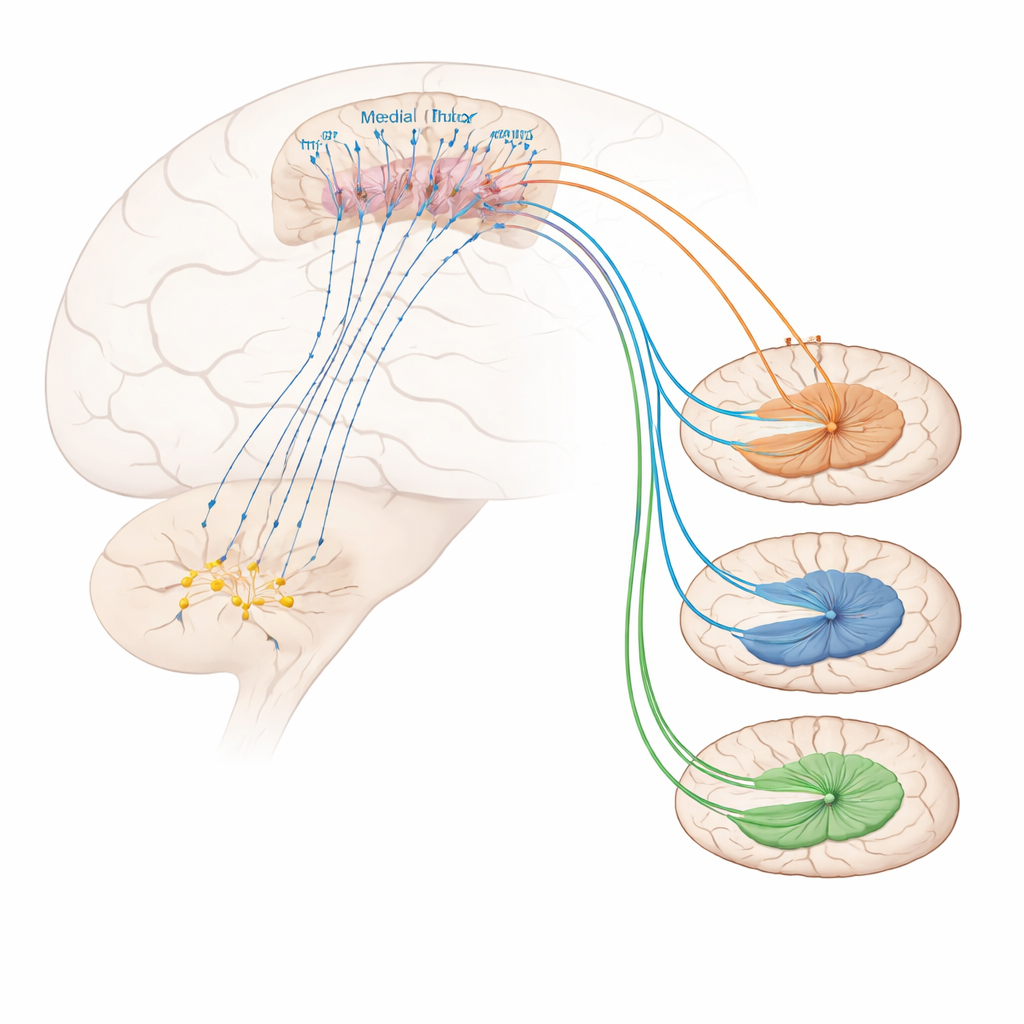
ماذا يعني هذا لعلاجات الألم المستقبلية
بعبارات بسيطة، تحدد الدراسة مساراً ثلاثي الخطوات دقيقاً: منطقة كولينرجية «مشغِّلة» في القاعدة الأمامية للدماغ، ومجموعة متخصصة من خلايا التحكم في القشرة الجبهية الوسطى، ومحاور ثلاثية مهادية مميزة تتحكم بشكل منفصل في مدى قوة الإحساس بالألم، ومدى سوءه عاطفياً، وكيفية تفاعلنا معه. يبدو أن الألم يطفي هذه الدائرة؛ إعادة تنشيطها، إما بالتحفيز المباشر أو عبر استهداف مستقبلات الأستيل كولين الخاصة بها، يخفف من الوجع والضيق المصاحب للألم الالتهابي في ذكور الفئران. وبينما لا يزال الكثير من العمل مطلوباً لترجمة هذه النتائج إلى البشر وإلى أشكال أخرى من الألم المزمن، تبرز النتائج استراتيجية واعدة: بدلاً من تخدير كل الإحساس، قد تستعيد العلاجات المستقبلية أو تضبط بدقة دوائر تخفيف الألم في الدماغ للحصول على علاج أطول أمداً وأكثر فعالية وربما أكثر أماناً.
الاستشهاد: Xie, G., Liu, Y., Qi, X. et al. A molecularly defined basalo-prefrontal-thalamic circuit regulates sensory and affective dimensions of pain in male mice. Nat Commun 17, 2134 (2026). https://doi.org/10.1038/s41467-026-69001-2
الكلمات المفتاحية: الألم المزمن, القشرة الجبهية الوسطى, المهاد, الإشارة الكولينرجية, مستقبلات النيكوتين