Clear Sky Science · ar
تعديل تساهمي لحمض غلوتاميك مستوحى من تكنولوجيا HaloTag
تحويل «مرساة» البروتين إلى هدف دوائي
تعمل العديد من أدوية السرطان الحديثة عن طريق الالتحام ببروتينات داخل خلايانا. لكن بعض أهم البروتينات لا تملك «مقابض» سهلة يمكن للأدوية أن تمسك بها. تقدم هذه الدراسة خدعة كيميائية ذكية، مستوحاة من أداة مختبرية شائعة تُدعى HaloTag، للالتصاق بموقع على بروتين يصعب الوصول إليه عادة ويشارك في تنظيم إشارات نمو مرتبطة بالسرطان. قد تفتح هذه الفكرة طرقًا جديدة لتصميم أدوية تغلق مسارات تحفّز الورم بطريقة أكثر دوامًا.
لماذا تستهدف معظم الأدوية التساهمية نفس الموقع
في السنوات الأخيرة أصبح ما يُسمى بالأدوية التساهمية الموجهة فئة مثيرة من الأدوية. تحمل هذه الجزيئات مجموعة كيميائية ذات تفاعل خفيف تشكل رابطة دائمة مع حمض أميني محدد على البروتين، مؤمنة الدواء في مكانه. تكاد كل هذه الأدوية تستهدف السيستئين، وهو حمض أميني نادر نسبياً لكنه تفاعلي بدرجة عالية. بالمقابل، فإن حمضين أمينيين آخرين، الأسبارتات والغلوتامات، أكثر شيوعًا وغالبًا ما تكونان حاسمتين لشكل البروتين ووظيفتهما، لكن مجموعاتهما الحامضية (الكربوكسيلات) أقل تفاعلًا في البيئة المائية داخل الخلية. هذا يجعل من الصعب تعديلها انتقائيًا، ولم تكن هناك سوى أمثلة قليلة ناجحة على أدوية تساهمية تستهدف الغلوتامات أو الأسبارتات قبل هذا العمل.
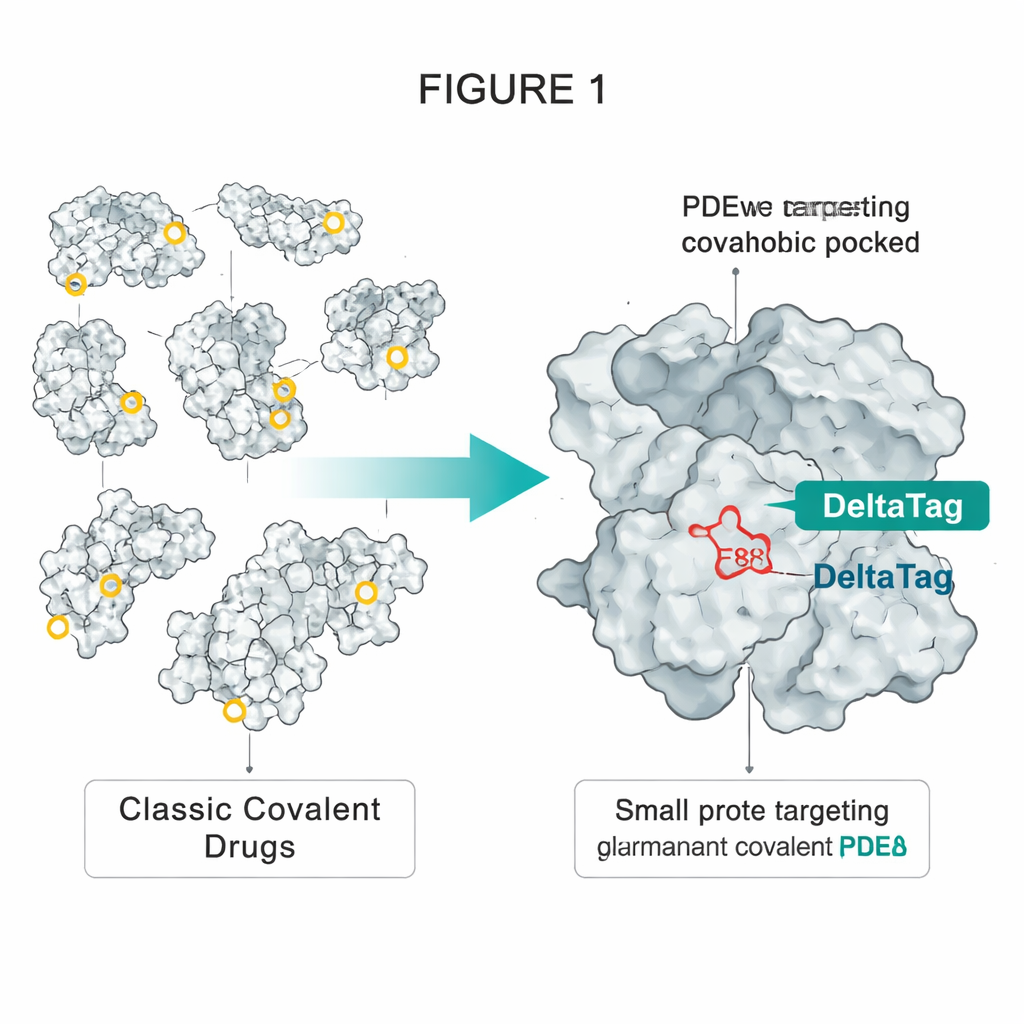
اقتراض خدعة من تكنولوجيا HaloTag
استلهم المؤلفون أفكارهم من HaloTag، وهو بروتين مهندَس يُستخدم على نطاق واسع ويمكن وسمه بشكل دائم بصبغات فلورية. في HaloTag، يتفاعل أسبارتات موضوع بعناية داخل جيب زلق مع سلسلة كلوروألكان بسيطة على الصبغة، مكوّنًا رابطة إسترة مستقرة. لاحظ الفريق أن بروتينًا آخر، PDEδ، يمتلك جيبًا هيدروفوبيًا مشابهًا إلى حد ما ويحتوي على غلوتامات مفردة متاحة تُدعى E88. ينقل PDEδ بروتينات إشارية مُعدَّلة بالدهون مثل GTPase الصغير Rheb عبر الخلية، مساعدًا إياها على الوصول إلى الأغشية حيث تُفعّل مجمعات تعزيز النمو مثل mTORC1. كانت مثبطات PDEδ غير التساهمية السابقة قادرة على إيقاف هذا النقل، لكن تأثيرها كان محدودًا لأن بروتينًا آخر، Arl2، يستطيع إزالتها من الجيب مع مرور الوقت.
تصميم DeltaTag للالتصاق بالغلوتامات
لتجاوز مشكلة «الطرد»، بدأ الباحثون من مثبط PDEδ معروف عالي الألفة وأعادوا تصميم أحد سلاسل جانبيه ليحمل «رأس حرب» هالوألكاني مشابه لتلك المستخدمة في رابطات HaloTag. من خلال عدة جولات من التعديلات الهيكلية الموجهة بهياكل بلورات البروتين، توصلوا إلى مركب سمّوه DeltaTag. الخاصية الأساسية فيه مجموعة فنيل إيثيل بروميد موضوعة بحيث، عندما يستقر الجزيء في جيب الدهون في PDEδ، يكون البروميد محاذيًا بدقة ليتفاعل مع E88. أكدت القياسات الفيزيائية الحيوية وهياكل الأشعة السينية عالية الدقة أن DeltaTag يشكل رابط إستري تساهمي على نحو انتقائي مع هذه الغلوتامات وأن الأحماض الأمينية الأخرى التي قد تكون أكثر تفاعلية على PDEδ تظل غير متأثرة. المركب تفاعلي بما يكفي لوضع وسم على البروتين بكفاءة، ومع ذلك مستقر بما يكفي في الماء ووجود مضاد الأكسدة الكبريتي الرئيسي في الخلية، الغلوتاثيون، لتجنب إلحاق أضرار عشوائية واسعة النطاق.
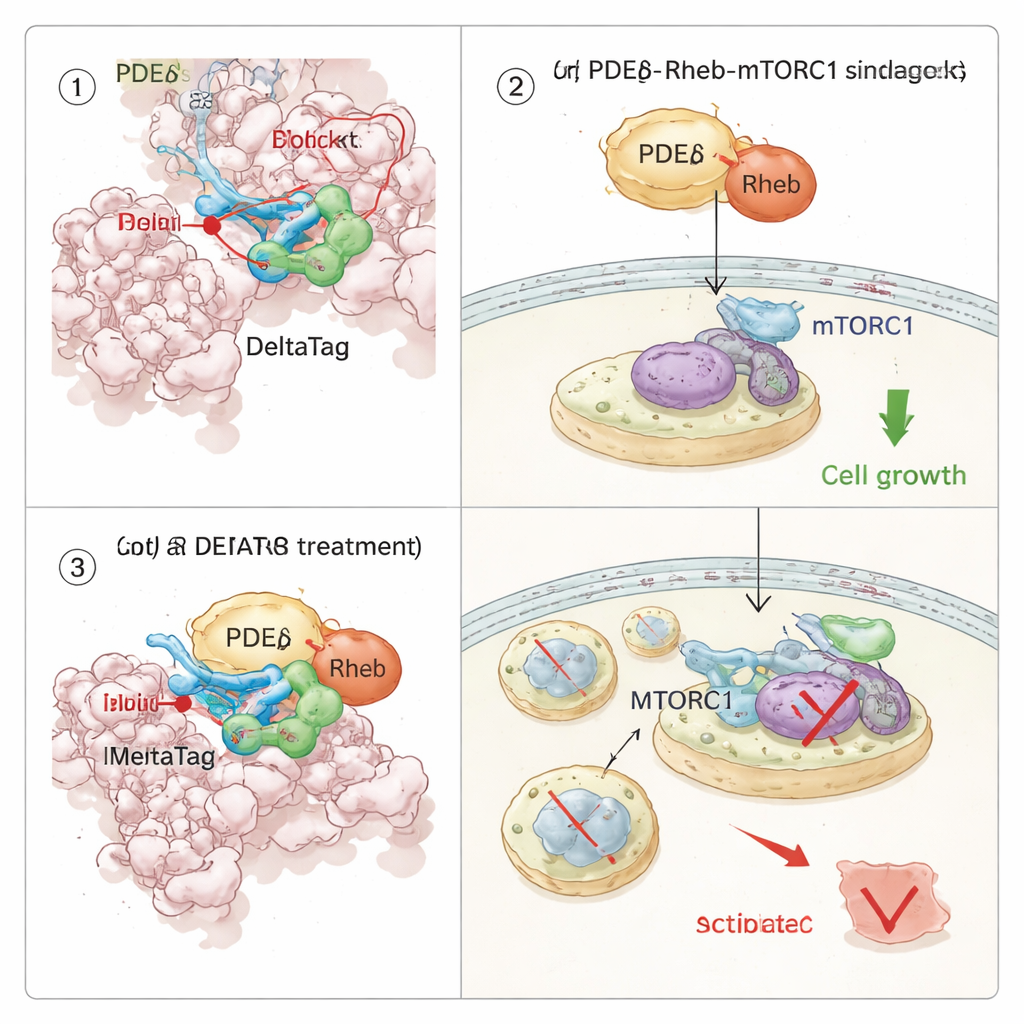
إعادة توصيل مسار نمو داخل خلايا السرطان
نظرًا لأن PDEδ يصاحب Rheb، وRheb بدوره يشغّل مسار النمو mTORC1، سأل الفريق كيف سيؤثر التثبيط التساهمي لـ PDEδ على شبكة الإشارات الخلوية. باستخدام تتبُّع الاستقرار الحراري عبر آلاف البروتينات، أظهروا أن DeltaTag يرتبط بشكل انتقائي بـ PDEδ في مستخلصات الخلايا ويؤثر على بروتينات مرتبطة بمحور Rheb–mTOR. في تجارب التصوير الحي للخلايا، تسبب DeltaTag في إعادة تموضع Rheb من نمط مشتت في داخل الخلية إلى أغشية داخلية أكثر تجمّعًا، بما يتوافق مع تعطيل دورته الطبيعية. كشفت تحليلات الفسفور البروتينية الشاملة وفرمونات وسترن بلوت مركّزة أن نشاط mTORC1، المتتبع عبر فسفرة بروتين ريبوزومي يسمى S6، انخفض بمرور الوقت، بينما ارتفعت إشارات تعويضية في مسارات ذات صلة. ومن المهم أنه في عدة خطوط خلوية بشرية سرطانية مدفوعة بطفرات KRAS وتعتمد على إشارات mTOR القوية، أبطأ DeltaTag التكاثر الخلوي بشكل أكثر فعالية من مثبطات عكسية قريبة الصلة، وكان تأثيره أضعف في خلايا تفتقر إلى PDEδ، مما يدعم أن آثاره الأساسية مستهدفة.
فتح باب لأنواع جديدة من الأهداف الدوائية
تُظهر هذه الدراسة أنه من الممكن بناء جزيئات صغيرة تشكل رابطة دائمة ومحددة للغاية مع غلوتامات مفردة مدفونة في جيب دهن على بروتين، باستخدام كيمياء هالوألكان بسيطة نسبيًا مستعارة من HaloTag. في نظام النموذجي PDEδ، توفِّر تلك الرابطة التساهمية حجبًا أكثر دوامًا لمسار نمو مرتبط بالسرطان مقارنة بالأدوية العكسية السابقة. وعلى نحو أوسع، يمكن تطبيق نفس منطق التصميم على بروتينات أخرى تمتلك تجاويف هيدروفوبية لكنها تفتقر إلى الأحماض الأمينية «التفاعلية» المعتادة، طالما أنها تقدم غلوتامات أو أسبارتات موضعية استراتيجية. مع مزيد من التحسين، قد تصبح مثبطات تساهمية تستهدف الغلوتامات مثل DeltaTag أدوات مفيدة في الكيمياء الحيوية الدوائية ونقاط انطلاق محتملة لعلاجات جديدة تستهدف بروتينات يصعب علاجها حاليًا.
الاستشهاد: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
الكلمات المفتاحية: مثبطات تساهمية, استهداف الغلوتامات, PDEδ, إشارة mTOR, تصميم أدوية السرطان