Clear Sky Science · ar
تباينات نهاية البروتين تؤثر على اتزان البروتينات
كيف يشكّل نهاية البروتين الصحة
ينتهي كل بروتين داخل خلايانا بذيل صغير مكوَّن من بضع وحدات فقط. قد يبدو هذا الذيل هامشيًا، لكن هذه الدراسة تكشف أنه يحدد بصمت أي البروتينات تبقى وأيها يُزال سريعًا. بما أن مستويات البروتينات تقف وراء السرطان والاضطرابات الوراثية واستجابة الخلايا للإجهاد، فإن فهم هذه الذيول يفتح طرقًا جديدة لقراءة مخاطر المرض وحتى تصميم علاجات مستقبلية.
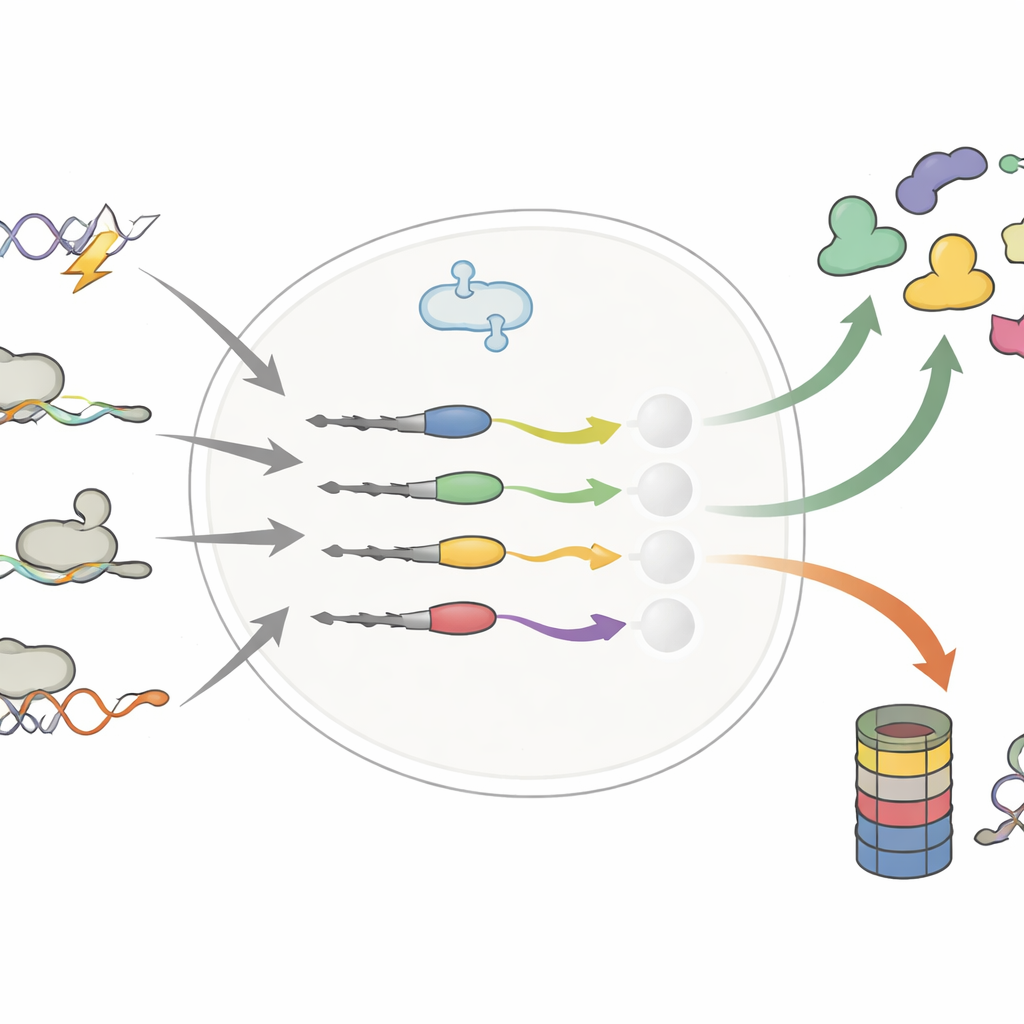
تغييرات صغيرة في ذيل البروتين تؤدي إلى اختلافات كبيرة في العمر
ركز الباحثون على الطرف البعيد من البروتينات — الطرف C — حيث حتى بضعة وحدات إضافية أو مستبدلة قد تظهر نتيجة طفرات في الحمض النووي أو التشكيل البديل للـ RNA أو تجاوز الرايبوسوم لإشارة التوقف المعتادة. أشارت أعمال سابقة إلى أن هذه الذيول «الخاطئة» تعمل أساسًا كعلامات للتخلص، مرسلة البروتينات المعيبة إلى آلة التفكيك الخلوية. من خلال المقارنة المنهجية لآلاف الذيول الطبيعية والمعدّلة، تُقلب هذه الدراسة تلك النظرة المبسطة. تظهر المجموعة أن الذيول المعدّلة يمكن أن تقصر أو تطيل عمر البروتين، وأحيانًا تثبّت محركات السرطان أو تزعزع مثبطات الورم.
متى تساعد أو تضر الأخطاء الجينية البروتينات
أحد المصادر الرئيسية لتغيّر الذيول هو طفرات «الاستمرار دون توقف» (nonstop)، التي تمحو إشارة التوقف العادية فيستمر الرايبوسوم داخل مقطع من الـ RNA عادة ما يكون ساكنًا. اختبر الباحثون أكثر من 3000 طفرة nonstop مرتبطة بالأمراض باستخدام موصِل ثنائي اللون يقيس مدى حماية كل ذيل أو ضعفها لبروتين نموذج. في المتوسط، جعلت الذيول المتحولة البروتينات أقل ثباتًا من نظيراتها الطبيعية، لكن جزءًا كبيرًا أظهر العكس: نحو واحدة من كل عشر طفرات nonstop سببت تثبيت البروتين، بينما أضعفت قرابة الثلث استقراره. أثّرت هذه التغيرات على بروتينات معروفة مسرطنة ومثبطات أورام، ما يوحي بأن طفرات تبدو طفيفة قد تُغيّر فعليًا توازن نمو الخلايا وموتها.
تنوّع مدمج من النسخ البديلة وتجاوز التوقف
ليست كل اختلافات الذيول حوادث. جيناتنا تنتج بشكل روتيني نسخًا بروتينية متعددة عبر التشكيل البديل للـ RNA وقراءة التوقف المبرمجة. من خلال تنقيب في فهارس الجينات البشرية، وجد المؤلفون أن ما يقرب من ثلثي الجينات تصنع بروتينات لها أكثر من تصميم ذيل واحد، وكثير منها يختلف فقط في الوحدات القليلة الأخيرة. اختبارات أمثلة مختارة أظهرت أن هذه النسخ المتقاربة غالبًا ما تمتلك أعمارًا نصفية مختلفة بوضوح. بعض الذيول الناتجة عن التجاوز جعلت البروتينات أكثر ثباتًا، وأخرى أقل. يقترح هذا أن الخلايا تستخدم اختلاف الذيول كزر ضبط دقيق، لتعديل مدة بقاء أشكال بروتينية معينة في أنسجة أو حالات مختلفة.
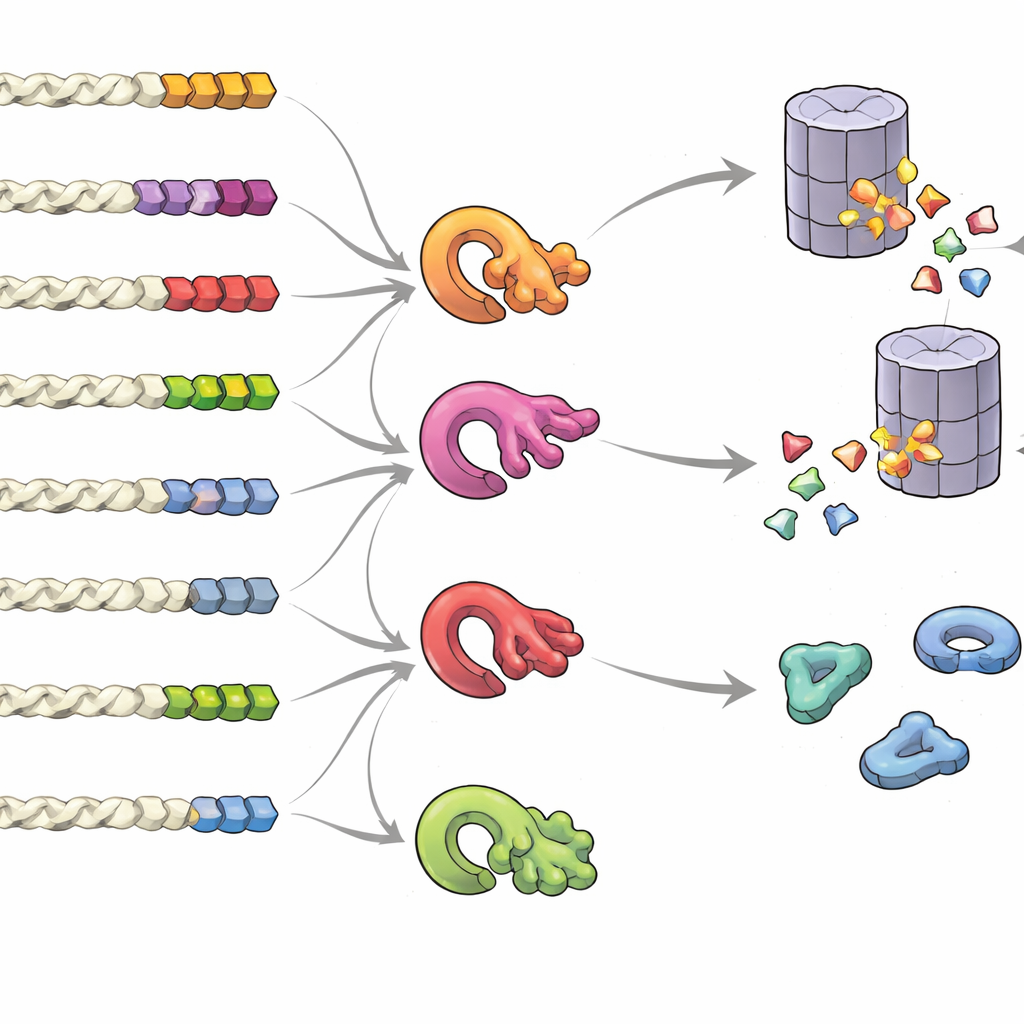
ما الذي يجعل الذيل علامة «احتفظ بي» أو «تخلص مني»
لفهم أي خصائص في الذيل تؤثر على مصير البروتين، أنشأت المجموعة مكتبات من الذيول العشوائية وقيست تأثيرها على نطاق واسع. وجدوا أنه ليس هناك «نمط» واحد ثابت فحسب، بل التركيب العام، الموضع، وتجميع بعض الوحدات هي المهمة. الذيول الغنية بمكونات صغيرة أو شحمية، أو بالحمض الأمينيين النادرين سيستئين وتريبتوفان، كانت تميل إلى دعوة التحلل، خاصة عندما تتجمع هذه البقايا. بالمقابل، الذيول الغنية بالمكونات الحمضية فضّلت الاستقرار. ومن خلال مقارنة العديد من الأنواع، أظهرت الذيول الطبيعية دلائل ضغط تطوري لتجنّب الأنماط الخطرة، بينما كانت الذيول الناتجة عن التجاوز أو تغير الإطار أكثر ميلاً إلى التركيبات المزعزعة للاستقرار. كما اكتشف الفريق أن عدة إنزيمات جودة—مختلفة لِجِازات يوبيكويتين—تتخصص في التعرف على أنماط ذيلية كارهة للماء، مكوِّنة شبكة معقدة تقرر أي البروتينات تُدمّر.
لماذا يهم هذا للطب والتكنولوجيا الحيوية
تعيد هذه الدراسة تصوّر الذيول البروتينية من نهايات سلبية إلى منظّمات نشطة لوفرة البروتينات. بالنسبة للقارئ العام، يعني هذا أن العديد من الأمراض قد تنشأ ليس فقط من بروتينات تالفة، بل أيضًا من تغييرات طفيفة في مدة بقاء البروتينات، ناجمة عن اختلافات صغيرة في نهاياتها. كما تحذر من أن العلاجات التي تشجّع عمداً تجاوز إشارات التوقف، المستخدمة لمعالجة بعض الاضطرابات الوراثية، قد تغيّر عن طريق الخطأ أعمار العديد من البروتينات الطبيعية. وفي الوقت نفسه، تشير النتائج إلى استراتيجيات جديدة قوية: من خلال هندسة تسلسلات الذيول أو تحفيز الخلايا لتفضيل أشكال مطوية أو أحداث تجاوز معينة، قد يتمكن العلماء في المستقبل من ضبط مستويات البروتين بدقة ملحوظة.
الاستشهاد: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
الكلمات المفتاحية: ثبات البروتين, ذيل C الطرفي, تحلل البروتين, طفرات جينية, اتزان البروتينات