Clear Sky Science · ar
الاستفادة من التآثر غير المتصل لإنزيم فوكوزيل ترانسفيراز 8 البشري بمثبط تساهمي لقمع الفوكوزيلة الأساسية
لماذا قد يهم منع سكر صغير في السرطان
تزيّن خلايانا البروتينات باستمرار بسلاسل سكرية صغيرة تعدّل بدقّة كيفية عمل تلك البروتينات. علامة سكرية واحدة على وجه الخصوص، تُسمى الفوكوزيلة الأساسية، تساعد الأورام على النمو والانتشار والتملص من الجهاز المناعي وحتى مقاومة علاجات السرطان الحديثة. تصف هذه الورقة كيف اكتشف العلماء نقطة تحكم خفيّة على الإنزيم البشري الذي يضيف هذا السكر، وصنعوا جزيئاً جديداً منخفض السُمّية يتشبّث بتلك النقطة لإيقاف نشاط الإنزيم. يفتح عملهم مساراً جديداً للأدوية التي تعيد برمجة سكريات سطح الخلايا بشكل دقيق بدلاً من استهداف الحمض النووي أو البروتينات مباشرة.
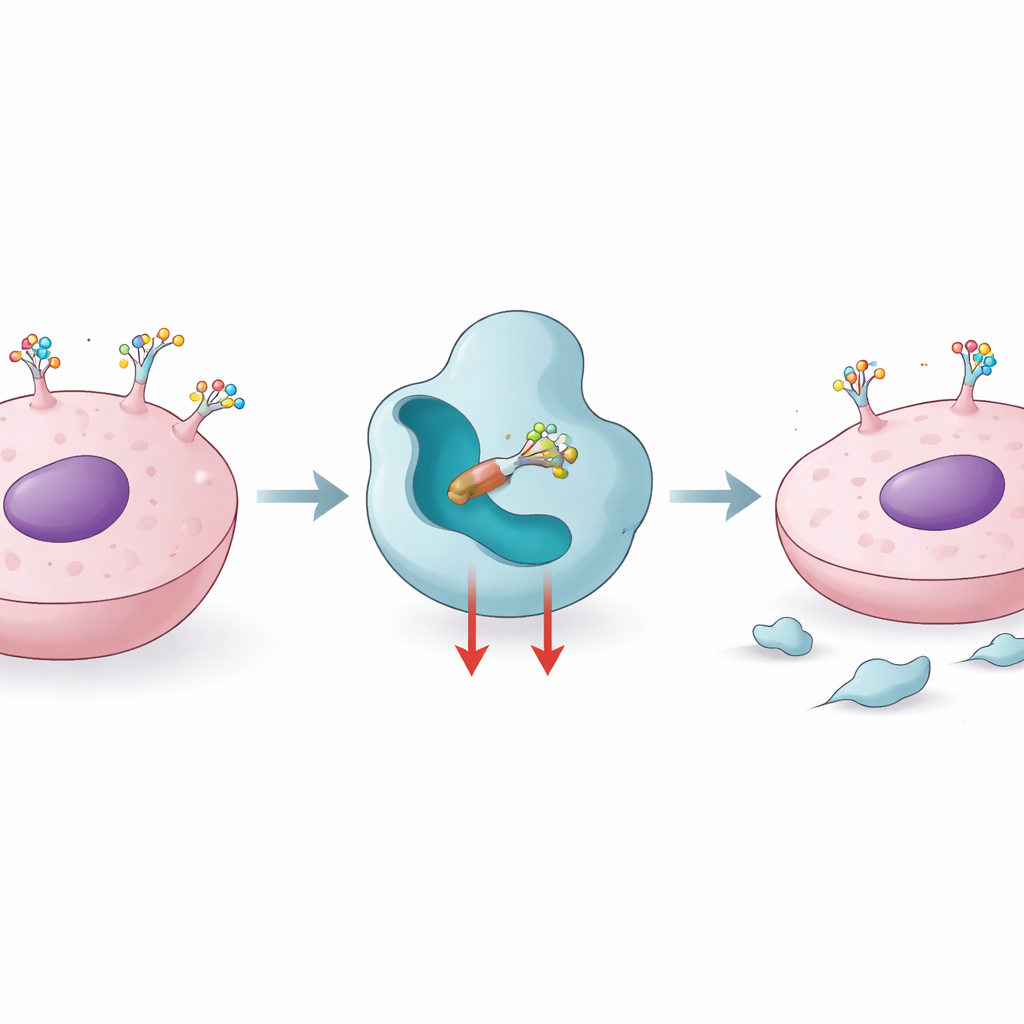
كيف تستخدم الخلايا العلامات السكرية لتشكيل المرض
تمر البروتينات الخارجة من «مصنع» الخلية الداخلي عبر "خط تشطيب" جزيئي حيث تُضاف السلاسل السكرية وتُحرر. الفوكوزيلة الأساسية خطوة تشطيب من هذا النوع، يقوم بها إنزيم يُدعى FUT8، الذي يضيف سكر فوكوز واحد إلى موضع رئيسي في العديد من الغليكانات المرتبطة بالبروتينات. عندما ترتفع مستويات FUT8، تصبح هذه العلامة السكرية أكثر شيوعاً على الجزيئات التي تتحكم في نمو الخلايا وحركتها والتعرّف المناعي. ربطت دراسات نشاط FUT8 العالي بسرطانات عدوانية مثل الورم الميلانيني، وسرطان الثدي ثلاثي السلبية، وسرطان الرئة، وبالمقاومة للأدوية المستهدفة وبعض علاجات الأجسام المضادة. إن حجب FUT8 يمكن أن يزيل بعض بروتينات الكبح المناعي، مثل PD‑1، من سطح الخلايا ويجعل الأورام أكثر وضوحاً للجهاز المناعي، مما يجعل FUT8 هدفاً جذاباً للعلاج المناعي للسرطان ولتحسين الأدوية الحيوية.
الحاجة إلى مانعات أذكى وأكثر انتقائية
كان تصميم أدوية ضد FUT8 صعباً لأن العديد من الإنزيمات المرتبطة تستخدم نفس «وقود» السكر الأساسي. غالباً ما قلدت المثبطات السابقة هذا الوقود، ما أدى إلى إيقاف واسع وغير انتقائي لعديد من مسارات الفوكوزيلة وآثار جانبية غير مرغوب فيها، بما في ذلك مشكلات تخثر أوقفت تجربة سريرية. استنتج المؤلفون أن استراتيجية أفضل ستكون تجنّب الموقع الفعّال المزدحم والبحث عوضاً عن ذلك عن موقع «بعيد» فريد على FUT8 يمكن أن يعمل كمفتاح تحكم. باستخدام فحص عالي الإنتاجية راقب نشاط الإنزيم، مرّوا بأكثر من ستة آلاف مركب وميّزوا بعض الجزيئات الشبيهة بالسلاسل التي أبطأت FUT8 بينما خفّضت أيضاً غزو الخلايا السرطانية في أطباق المختبر.
اكتشاف جيب تحكم مخفي
باستخدام حيود الأشعة السينية البلورية، حلّل الفريق البنى ثلاثية الأبعاد لـ FUT8 المرتبطة باثنين من هذه المثبطات. لدهشتهم، لم يجلس أي من المركبين في الموضع المعتاد الذي يرتبط به مانح السكر والمستقبل. بدل ذلك، استقرّا داخل جيب طويل يشبه القناة بين فصّين رئيسيين من الإنزيم، قريب لكن متميز عن المركز النشط. أدى الارتباط في هذا الموقع إلى دفع حلقات وأحماض أمينية مفتاحية عن مواضعها، خصوصاً عناصر تساعد عادةً في احتضان مانح السكر. أظهرت المحاكاة الحاسوبية أنه عندما يُملأ هذا الجيب، تتغير حركات FUT8 ومشهد الطاقة الخاص به، مفضلة أشكالاً ضعيفة في تحفيز التفاعل. بعبارة أخرى، عملت المثبطات بطريقة تآثرية: ضغطت زرّاً بعيداً تسبب في اختلال محاذاة أجزاء الإنزيم العاملة.
تحويل جزيء ضارب إلى أداة تساهمية دقيقة
مسلحين بهذا الخريطة البنيوية، بحث الباحثون عن جزيئات لا تشغل الجيب فحسب بل يمكنها أيضاً تكوين رابطة دائمة مع بقاعدة لايزين قريبة (K216) التي تنحرف طبيعياً نحو القناة. وجدوا أن عاملًا يُدعى SSO، يحمل إستر N‑هيدروكسيسكسنيميد التفاعلي، ارتبط في نفس الأخدود وشكل رابطاً تساهمياً مع K216، مؤمّناً الإنزيم في حالة غير نشطة. بالاستفادة من السمات المشتركة بين SSO وضربتهم الأولى NH125، دمجوا أجزاء من كل منهما لصنع جزيء جديد اسمه CAIF. أكدت البنى البلورية أن CAIF يمر على طول القناة، ويتناسب بإحكام بين بقايا محبة للماء والدهون، ويكوّن رابطة تساهمية مع K216. عزّز هذا التصميم تثبيط FUT8 بعدة أضعاف مقارنةً بالمركبات الأصلية مع الحفاظ على إنزيمات مرتبطة قريبة من التأثير، مما يبرز شكلية فريدة لجيب التآثر في FUT8.
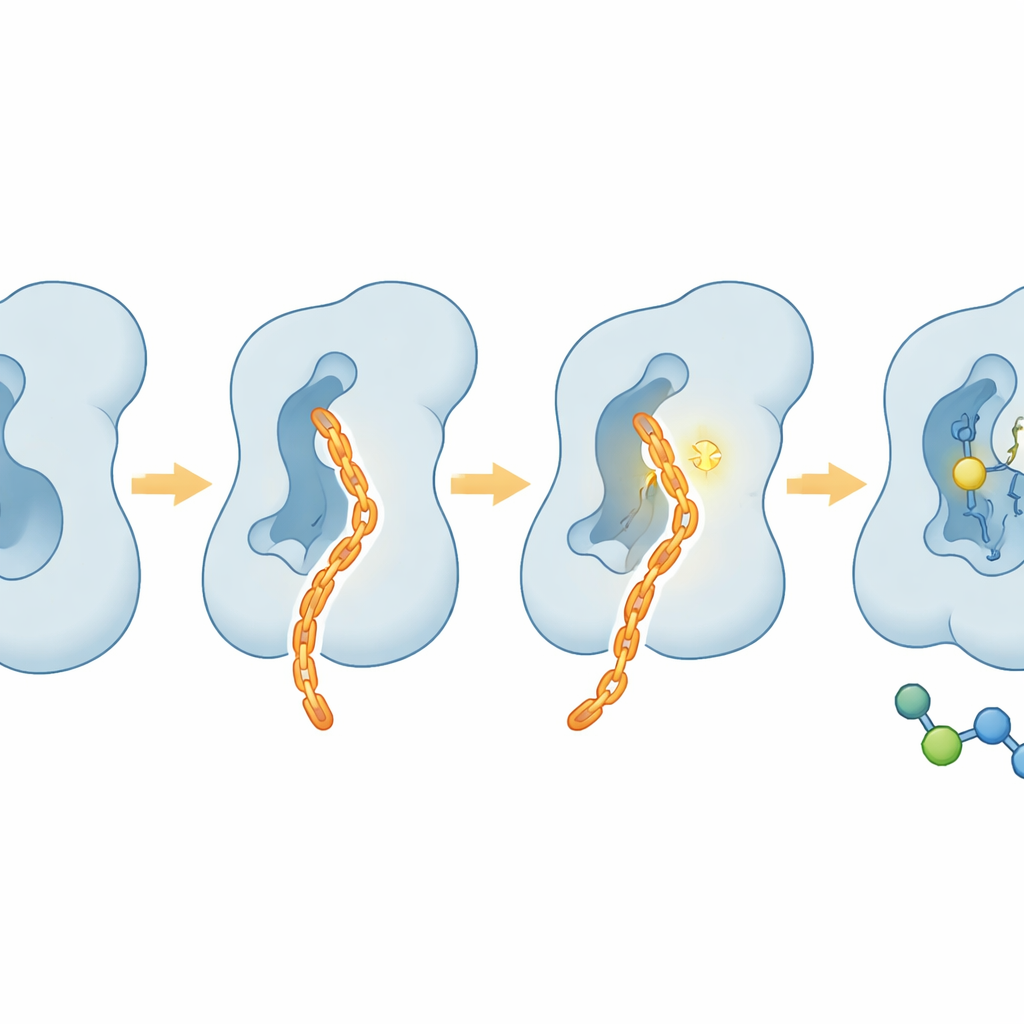
لطيف على الخلايا، صارم على سلوك الورم
خارج أنابيب الاختبار، فحص الفريق كيفية تصرّف CAIF في الخلايا الحية. عبر عدة خطوط خلوية بشرية، أظهر CAIF سمّية طفيفة حتى عند جرعات عالية، مشيراً إلى أنه لا يسمم آليات الخلية على نطاق واسع. ومع ذلك قلّل بشكل ملحوظ من الفوكوزيلة الأساسية على سطح الخلية، كما كشفته أصباغ رابطة للسكريات، وكان ذلك بانتقائية أفضل بكثير تجاه FUT8 مقارنةً بالمانعات الشاملة السابقة. في تجارب غزو الخلايا السرطانية، تفوق CAIF على مانع قائم على السكر مستخدم شائعاً في الحد من قدرة الخلايا الورمية على الهجرة عبر مصفوفة، وهو سمة مميزة للإمكانات النقيلية. تتوافق هذه التأثيرات مع الدور المعروف لـ FUT8 في تعزيز الغزو والتملص المناعي بدلاً من دفع انقسام الخلايا مباشرة.
ماذا يعني هذا لعلاجات السرطان المستقبلية
لا تدّعي هذه الدراسة أن CAIF جاهز بذاته ليكون دواءً. بل تُظهر أن FUT8 يحتوي على جيب تآثري قابل للعلاج لم يكن معروفاً سابقاً ويمكن استهدافه بجزيئات مشكّلة بعناية تُكوّن رابطة دائمة إلى لايزين واحد. عبر استغلال هذا الموقع، يمكن للباحثين خفض نشاط إنزيم معدّل للسكريات بشكل انتقائي يقع عند مفترق طرق تقدم السرطان والتملص المناعي ومقاومة الدواء، مع ترك الإنزيمات المرتبطة إلى حد كبير دون مساس. يقدم العمل مخططاً لتصميم مثبطات الجيل التالي التي تعيد تشكيل أنماط السكر ذات الصلة بالمرض على البروتينات وقد توسّع في نهاية المطاف مجموعة الأدوات للعلاج المناعي للسرطان وتحسين أدوية الأجسام المضادة.
الاستشهاد: Jiang, J., He, D., Ke, M. et al. Exploiting human fucosyltransferase 8 allostery with a covalent inhibitor for core fucosylation suppression. Nat Commun 17, 2607 (2026). https://doi.org/10.1038/s41467-026-68971-7
الكلمات المفتاحية: مثبطات FUT8, الفوكوزيلة الأساسية, مثبطات تآثرية تساهمية, تعديلات سكرية في السرطان, تصميم أدوية غليكوزيل ترانسفيراز