Clear Sky Science · ar
تقييد FANCD2 لتقدّم الشُعب ومنع الهشاشة عند البِدايات المبكرة أثناء إعادة النسخ
عندما تحيد نسخ الحمض النووي قليلاً عن المسار
في كل مرة تنقسم فيها الخلية عليها أن تنسخ مكتبة حمضها النووي بالكامل مرة واحدة بدقة. إذا نُسخت أجزاء من تلك المكتبة مرتين، أو نُفذت النسخة بسرعة وبعشوائية، فقد يؤدي ذلك إلى كروموسومات مكسورة وطفرات تغذي السرطان. تدرس هذه الدراسة ما يحدث عندما تبدأ آليات الخلية لمنع جولات النسخ الإضافية بالفشل، وتكشف كيف يتدخل بروتين إصلاح يُسمى FANCD2 لحفظ الخلايا التي تنحرف قليلاً عن المسار من الانزلاق إلى فوضى جينومية كاملة.
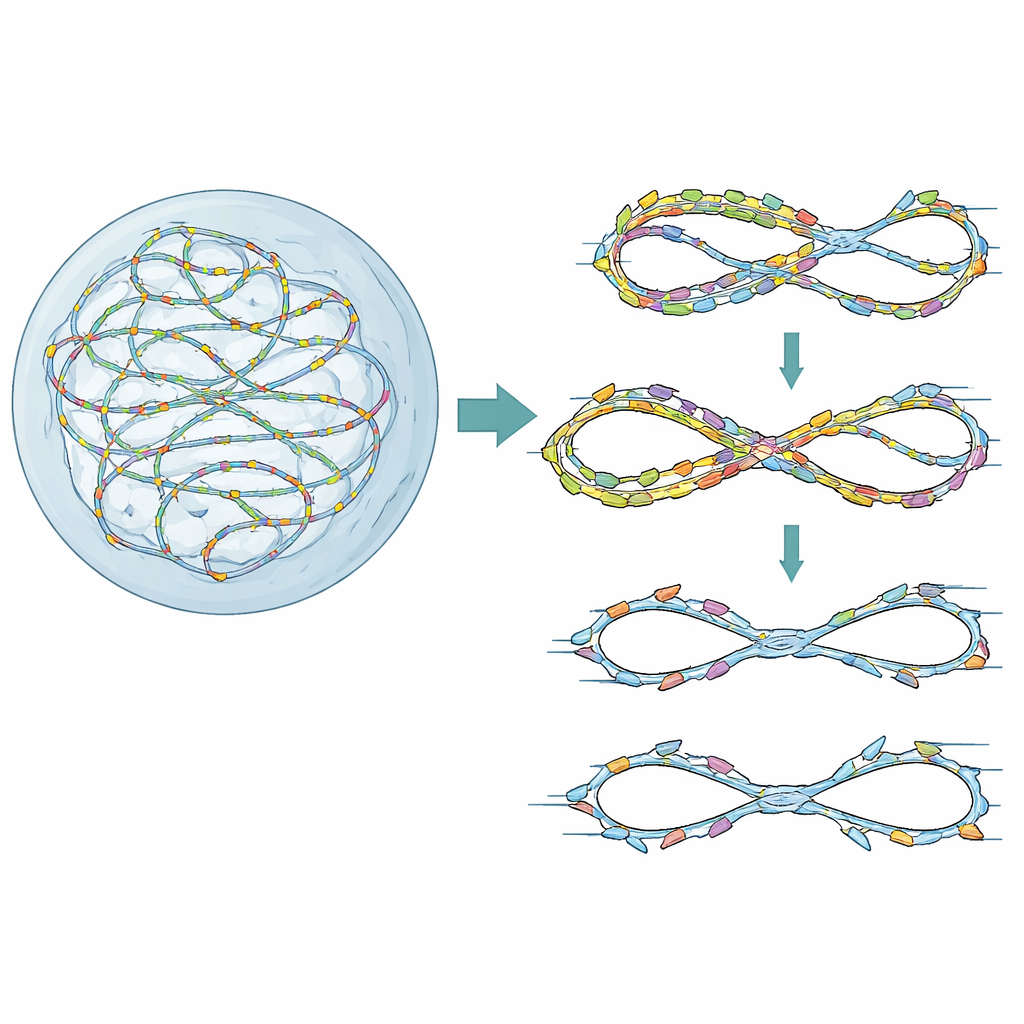
حواجز لضمان نسخة واحدة نظيفة
تتضاعف كروموسوماتنا من آلاف نقاط بدء، أو «بدايات»، التي تُرخص ثم تُفعّل في تسلسل مُوقّت بعناية. يساعد بروتين صغير يُدعى Geminin عادةً على ضمان أن كل بداية تُفعّل مرة واحدة فقط خلال دورة الخلية. عندما يُفقد Geminin أو يضعف، قد تُفعّل بعض البدايات مرة أخرى على حمض نووي سبق نسخه، وهي حالة تُعرف بإعادة النسخ. خلايا السرطان، التي غالباً ما تُنتج عوامل ترخيص بفرط، تكون عرضة لهذا المشكلة بشكل خاص. استخدم المؤلفون أولاً فحصًا جينيًا ذا محتوى عالٍ في خلايا بشرية مهيّأة لإعادة نسخ منخفضة المستوى عن طريق نزع Geminin. سألوا أي جينات إصلاح الحمض النووي ونقاط التفتيش تصبح حاسمة في هذه الحالة المتوترة ووجدوا أن FANCD2، المعروف أساسًا بإصلاح الوصلات العرضية في داء فانكوني، برز كحامي رئيسي لبقاء الخلايا وسلامة الجينوم.
المستجيب الأول عند آلات النسخ المُجهدة
تبع الفريق بعد ذلك مكان وزمان ظهور FANCD2 في الخلايا التي تمر بإعادة النسخ. بعد وقت قصير من إزالة Geminin يتجمع FANCD2 بسرعة على الكروماتين ويكوّن نقاطًا نووية ساطعة، قبل وقت طويل من إمكانية اكتشاف تكسر واسع للحمض النووي. باستخدام وسم الحمض النووي المصنع حديثًا معا مع اختبارات القرب، أظهروا أن FANCD2 يُستدعى مباشرة إلى آلات التضاعف النشطة، خاصة في الخلايا التي يُنسخ حمضها النووي للمرة الثانية بالفعل. في خلايا مزامنة أُطلق سراحها إلى دورة الانقسام التالية، ظهرت مجموعة مميزة تُظهر نمط حمض نووي مفرط النسخ منتشر. عرضت هذه الخلايا إشارات قوية لـ FANCD2 وRPA، مما يشير إلى استمرار إجهاد التضاعف، وتم إيقافها عند الحد الفاصل قبل الطور الانقسامي بواسطة نقطة تفتيش نشطة، ما يوحي بأن FANCD2 هو جزء من استجابة مبكرة تثبّت الشُعب المُجهدة بدلاً من مجرد التفاعل مع الحمض النووي المكسور.
كبح الشُعب الهاربة والفجوات المخفية
لاختبار كيف يشكل FANCD2 عملية النسخ، جمع الباحثون فقدان Geminin مع نزع FANCD2. ومن المدهش أن إزالة FANCD2 لم تزد في نسبة الخلايا ذات الجينومات المعاد نسخها بوضوح. بدلًا من ذلك كشفت اختبارات ألياف الحمض النووي أحادية الجزيء أن الشُعب التضاعفية قطعت مسافات أطول وأصبحت أكثر لامركزية، وهو علامة على تقدم غير متكافئ وغير مستقر. هذه الشُعب الأسرع تركت وراءها المزيد من الفجوات أحادية الشريطة في الحمض النووي المشكّل حديثًا، المرصودة كنقاط مكثفة لـ RPA وBrdU الطبيعي وتأكدت بحساسية الشرائط المعلّمة لإنزيم يقطع المناطق أحادية الشريطة. أظهرت الخلايا التي تفتقر إلى كل من Geminin وFANCD2 طفرة في تكسرات الكروموسوم وشرائحه والأجسام النووية والميكرونوكلات، كلها سمات لعدم استقرار جينومي شديد. محاصرة PARP، وهو عامل يساعد عادةً في إدارة مثل هذه الفجوات، قلدت وفاقمت هذه العيوب، مما يؤكد أن تكوّن الفجوات غير المنضبط محور الضرر.
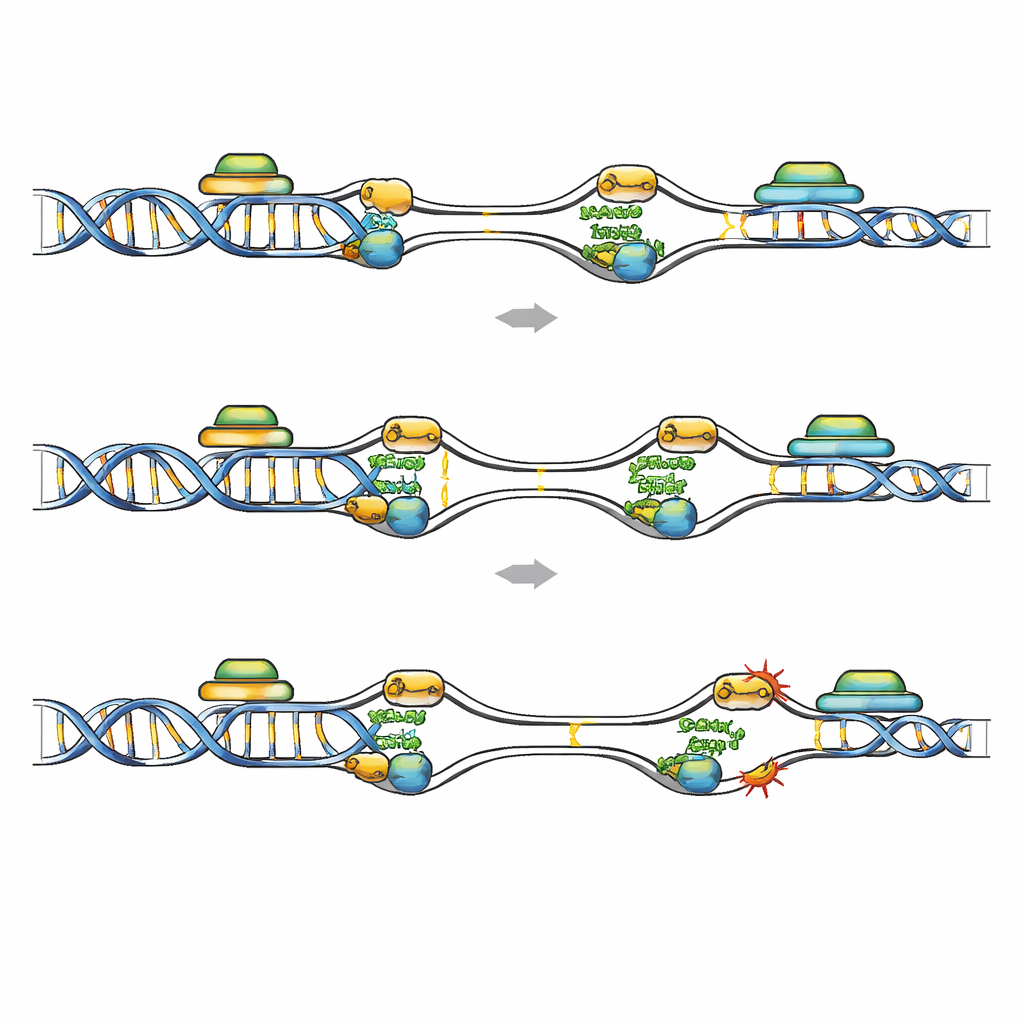
مواقع هشة حيث تتصادم النسخ والقراءة
قدّم رسم خرائط ارتباط FANCD2 على مستوى الجينوم رؤية للمناطق التي تكون فيها إعادة النسخ أكثر خطورة. في خلايا لمفاوية مصابة باللوكيميا مُنزوعَة Geminin، انتقل FANCD2 من مواقع الهشاشة الشائعة التقليدية إلى بدايات تضاعف تُفعّل مبكرًا وموجودة ضمن جينات قصيرة غنية بـ GC وعالية النسخ. تحمل هذه المناطق علامات النسخ النشط ومعرضة لتشكّل حلقات RNA–DNA (R-loops)، حيث يشكل الحمض الريبي الناشئ هجينًا مع قالب الدنا الخاص به، ما قد يعيق التضاعف. أظهرت مجموعات بيانات عامة مزيدًا من ضرر الدنا وإشارات مرتفعة للهجين RNA–DNA في الجينات الغنية بـ FANCD2 بعد فقدان Geminin، وتطابقت هذه المناطق مع ما يسمى مواقع الهشاشة المبكرة المتكررة. عندما انخفض النسخ عمومًا بدواء ما، أو عندما أزيلت حلقات R بشكل محدد عبر فرط التعبير عن RNase H1، انخفض عدد نقاط FANCD2 وRPA وأضرار الدنا في الخلايا الناقصة Geminin بشكل ملحوظ. وهذا يشير إلى أن التصادمات بين البدايات المعاد تفعيلها ووحدات النسخ النشطة، والمكثفة بواسطة حلقات R، تخلق نقاطًا هشة يجب على FANCD2 حمايتها.
ضبط الحماية عبر علامات كيميائية دقيقة
يُفعّل FANCD2 جزئيًا عن طريق ارتباط علامة صغيرة شبيهة باليوبيكويتين. عبر نزع FANCA، المكوّن الأساسي لآلة الوسم، وباستخدام خلايا تُعبّر عن طفرة في FANCD2 مقاومة لهذا التعديل، أظهر المؤلفون أن الوصم الأحادي يُحسّن بقاء الخلايا التي تُعيد النسخ لكنه ليس ضروريًا تمامًا. حتى FANCD2 غير الموسوم وفر حماية جزئية، متسقًا مع أدوار مميزة في كل من الاستشعار وتثبيت الشُعب المُجهدة. الصورة العامة هي أن FANCD2 يساعد على إبطاء وتنظيم التضاعف عند البدايات المبكرة الضعيفة ويحد من عدد وحجم الفجوات أحادية الشريطة.
لماذا يهم هذا لعلاج السرطان
لغير المتخصصين، الرسالة الأساسية أن ليس كل أخطاء النسخ كارثية من البداية. يمكن تحمل إعادة النسخ الخفيفة، كما يحدث في بعض الأورام، إذا حافظت أنظمة الحماية مثل FANCD2 على كبح النسخ الهائج ومنعت الفجوات الهشة من التحول إلى كروموسومات مكسورة. عندما تُزال هذه الحماية أو تُرغَم، تتصاعد نفس أخطاء الترخيص منخفضة المستوى بسرعة إلى تحطيم للجينوم. وبما أن فقدان Geminin وعيوب ترخيص التضاعف مُتكدّسة في خلايا السرطان، والعديد من الأورام تحمل بالفعل نقاط ضعف في شبكة فانكوني/BRCA، فإن نقاط الضعف المكتشفة هنا تقترح استراتيجيات علاجية: الجمع بين مثبطات تدفع الخلايا السرطانية نحو إعادة النسخ وأدوية تُفاقم تراكم الفجوات، مثل مثبطات PARP، قد يدفع الخلايا الخبيثة انتقائيًا إلى تجاوز حد تحملها بينما تُبقي الخلايا السليمة ذات الحماية السليمة بصحة أفضل.
الاستشهاد: Badra-Fajardo, N., Karydi, E., Bayona-Feliu, A. et al. FANCD2 restrains fork progression and prevents fragility at early origins upon re-replication. Nat Commun 17, 2478 (2026). https://doi.org/10.1038/s41467-026-68966-4
الكلمات المفتاحية: إجهاد تضاعف الحمض النووي, FANCD2, Geminin, إعادة النسخ, عدم استقرار الجينوم