Clear Sky Science · ar
عدوى فيروس السيتوميجالو البشري تعطل وظائف الحاجز وتُحفِّز التحول الظهاري-الحرشفي في نموذج عضو صفائحي القنوات الصفراوية
لماذا تهمنا قصة هذا الفيروس في الكبد
فيروس السيتوميجالو البشري شائع جدًا ويحمله معظمنا دون أن نعلم. ومع ذلك، لدى المواليد الجدد والأشخاص ذووا المناعة الهشة يمكن أن يرتبط بمشاكل خطيرة في الكبد والقنوات الصفراوية، بما في ذلك مرض نادر لكنه مدمر في الطفولة يُسمى ضمور القنوات الصفراوية. تستخدم هذه الدراسة قنوات صفراوية بشرية مصغرة مزروعة مخبريًا لتوضيح كيف يمكن للفيروس أن يضر مباشرة بهذه الأنابيب الرقيقة ويُحفِّز تغييرات تليفية قد تساعد في تفسير الروابط المطروحة منذ زمن طويل بين العدوى ومرض الكبد المزمن.
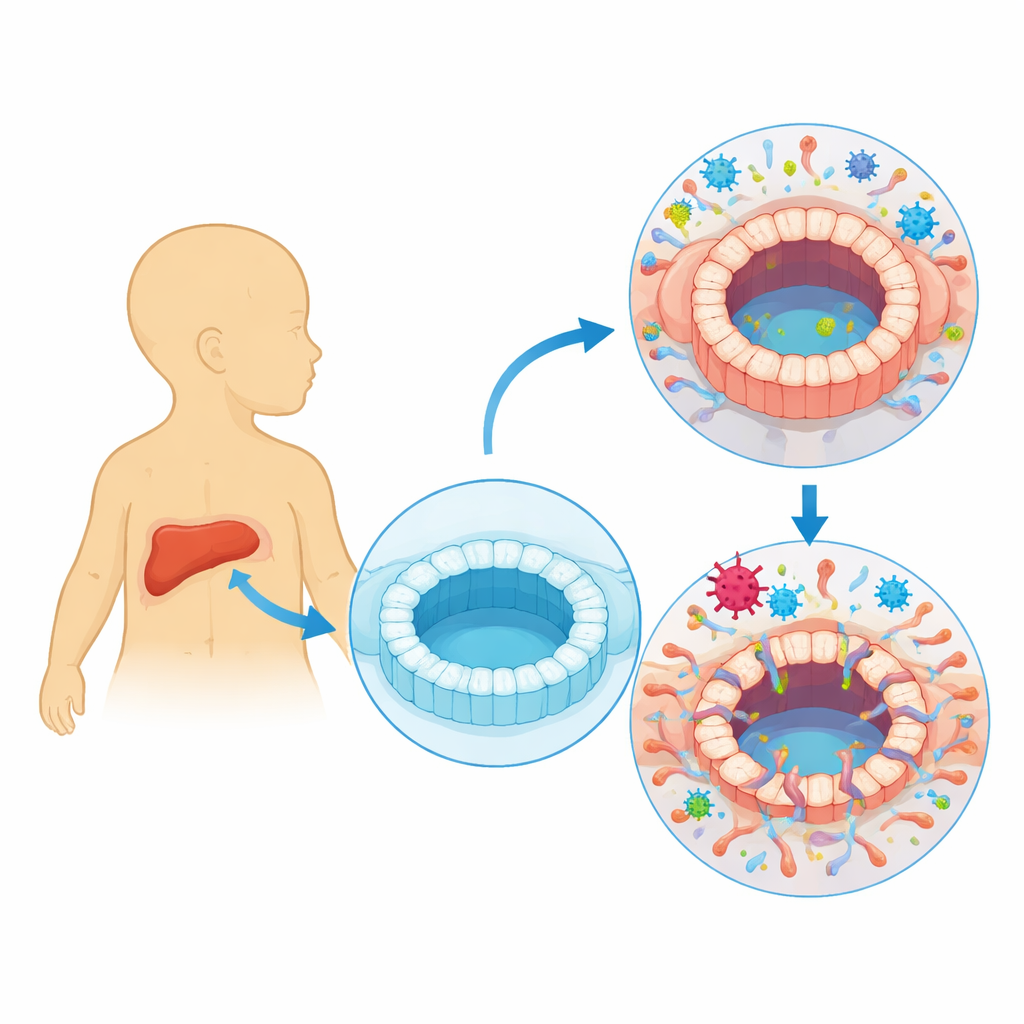
نظرة أقرب إلى فيروس شائع لكنه صامت
عادة يعيش فيروس السيتوميجالو البشري بهدوء داخل أجسامنا، متقلبًا بين طور نشط ينتج فيه جزيئات فيروسية جديدة وطور كسول يختبئ فيه داخل خلايا دموية معينة. لاحظ الأطباء منذ زمن أن الأشخاص الذين تظهر لديهم عدوى فعالة بفيروس السيتوميجالو قد يطوّرون إصابة في القنوات الصفراوية وركودًا صفراويًا حيث تعجز الصفراء عن التدفق بشكل صحيح. كما أن العديد من الرُضّع المصابين بضمور القنوات الصفراوية، وهي حالة تنسد فيها القنوات وتُصاب بالتليف بعد الولادة بفترة قصيرة، يظهرون أيضًا علامات عدوى حديثة بفيروس السيتوميجالو. ومع ذلك، ظل الأمر غير واضح عما إذا كان الفيروس يُصيب فعلاً الخلايا المبطنة للقنوات الصفراوية أم أنه مجرد مترافق خلال المرض.
بناء قنوات صفراوية مصغرة في طبق
للإجابة عن ذلك، أنشأ الباحثون «أعضاء صفائحية» ثلاثية الأبعاد تُحاكي القنوات الصفراوية البشرية. بدأوا بخلايا جذعية متعددة القدرات المستحثة، أعيد برمجتها من دم بشري، ووجهوها لتتكوّن إلى خلايا شبيهة بالخلايا الصفراوية (الخلايا المبطنة للقنوات الصفراوية). نظّمت هذه الخلايا نفسها إلى كريات مجوفة ذات تجويف مركزي وصلات خلوية متينة، شبيهة بقناة صفراوية مصغرة. ثم عرّض الفريق هذه الأعضاء لسلالة من فيروس السيتوميجالو الموسومة بعلامة فلورية تتوهج عندما يكون الفيروس في طور التكاثر النشط. سمح ذلك بتتبُّع الخلايا المصابة وقياس كيفية تغيّر الأعضاء مع مرور الوقت.
كيف تشوّه البنية وتضعف الحاجز
بمجرد الإصابة، توقّفت الأعضاء عن النمو بصورة طبيعية وأصبحت مشوهة، بجدران سميكة وغير منتظمة. أضاءت بعض الخلايا بشكل قوي، ما دلّ على نشاط فيروسي كامل وإنتاج جزيئات فيروسية جديدة؛ بينما حملت خلايا أخرى المادة الوراثية الفيروسية بمستويات أضعف، ما يوحي بحالة أكثر سكوتًا شبيهة بالكمون. كشفت اختبارات وظيفية أن الأعضاء المصابة فقدت قدرات مهمة للقناة الصفراوية. لم تعد تنتفخ بشكل مناسب استجابة لمثير يعتمد على قنوات نقل الأيونات، وتسربت بسهولة أكبر في اختبار المقاومة الكهربائية الذي يقيس إحكام الحاجز. تراجعت البروتينات التي تغلق الفجوات بين الخلايا، مثل مكونات الوصلات الضيقة، وأصبح نقل صبغة اختبار إلى التجويف الداخلي وخارجه غير طبيعي. مجتمعة، تظهر هذه التغييرات أن فيروس السيتوميجالو يمكنه أن يقوّض مباشرة جدار القناة الصفراوية، مما يجعله مسربًا ومعطلاً لوظائفه.
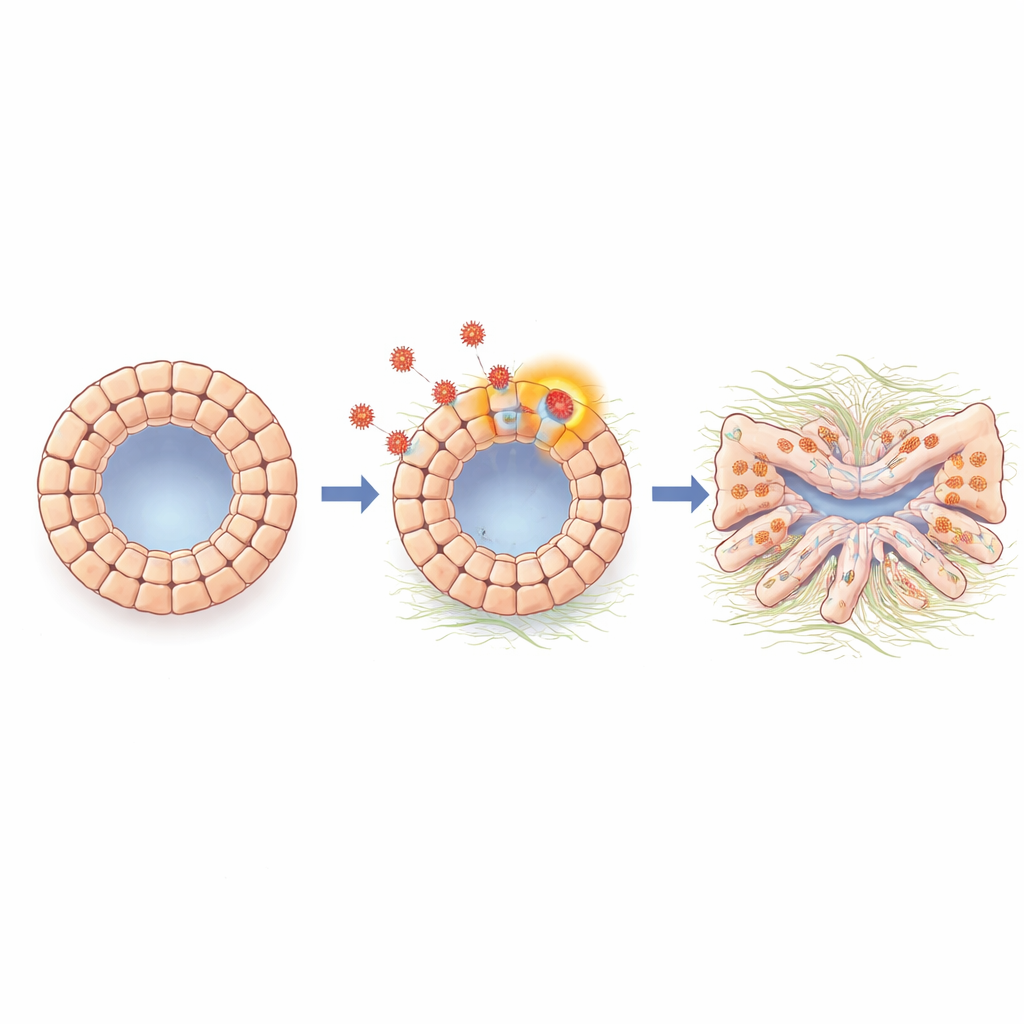
تحول هوية الخلايا نحو حالة تليفية
بالغ الباحثون في التحليل، فدرسوا نشاط الجينات على مستوى الأعضاء ككل وعلى مستوى الخلية الواحدة. وجدوا تنشيطًا قويًا لبرنامج شبيه بالتحول الظهاري-الحرشفي، وهي عملية تفقد فيها الخلايا السطحية المترابطة صلابة تواصلها، وتكتسب طابعًا أكثر حركةً وليفيًا، وتبدأ بإنتاج جزيئات مرتبطة بتكوّن النسيج الندبي. أظهرت الأعضاء المصابة مستويات مرتفعة من N-كادهرين وعلامات أخرى مرتبطة بهذا التحول، بالإضافة إلى جينات مشاركة في التليف وإنتاج المادة بين الخلوية. ارتفعت مستويات عامل إشاري اسمه TGF-بيتا، المعروف بتحفيز التليف في العديد من الأعضاء، أثناء العدوى. عندما قام الفريق بحجب إشارة TGF-بيتا بمثبط جزيئي صغير أو بواسطة جسم مضاد، استعادت الأعضاء شكلًا أكثر طبيعية، وانخفضت العديد من الجينات المرتبطة بالتليف والتحول عائدةً نحو الوضع الطبيعي، ما يشير إلى أن TGF-بيتا هو وسيط رئيسي يربط وجود الفيروس بالتغيرات الخلوية الضارة.
من الأنابيب المزروعة مخبريًا إلى الأطفال المرضى
للاطلاع ما إذا كانت هذه الملاحظات المختبرية لها صلة بالمرض الحقيقي، فحص الباحثون أنسجة كبدية من أطفال مصابين بضمور القنوات الصفراوية ومن حالات كبدية أطفالية أخرى. باستخدام مجسات حساسة، اكتشفوا DNA لفيروس السيتوميجالو في الخلايا الصفراوية — خلايا بطانة القنوات — في نحو ثلثي عينات ضمور القنوات الصفراوية، لكن بدرجة أقل بكثير في أكباد حالات غير ضمور القنوات. في نفس المناطق التي تم فيها العثور على DNA الفيروسي، أظهرت خلايا القناة مستويات أعلى من TGF-بيتا وN-كادهرين، متوافقة مع نمط التحول والتليف الذي لوحظ في الأعضاء المصغرة. يشير هذا إلى أنه في مجموعة فرعية من الأطفال، يُصيب فيروس السيتوميجالو خلايا القنوات الصفراوية مباشرة ويدفعها نحو حالة ليفية عن طريق تنشيط مسارات مدفوعة بـTGF-بيتا.
ما الذي يعنيه ذلك لفهم وعلاج أمراض القنوات الصفراوية
بعبارة بسيطة، تُظهر هذه الدراسة أن فيروسًا شائعًا يمكن أن يغزو الخلايا المبطنة للقنوات الصفراوية، يرخّي وصلاتها الضيقة، ويدفعها نحو هوية ليفية وأقل تخصصًا عبر إشارة قائمة على TGF-بيتا. تضعف هذه التغييرات وظائف الحاجز والنقل في القنوات وقد تسهم في انسداد القنوات الصفراوية واعتلالها الليفي كما يُرى في أمراض مثل ضمور القنوات الصفراوية. ورغم أن ليس كل حالة من أمراض القنوات الصفراوية سيسببها فيروس السيتوميجالو، فإن الدراسة تعزز الفرضية القائلة إنه في الرضع المعرضين للخطر قد تكون العدوى الفيروسية قطعة مهمة من أحجية المرض — وأن استهداف المسارات المرتبطة بـTGF-بيتا قد يساعد يومًا ما في حماية أو استعادة القنوات الصفراوية الهشة.
الاستشهاد: Ye, Z., Hu, X., Rahaman, S.M. et al. HCMV infection disrupts barrier functions and promotes epithelial–mesenchymal transition in a cholangiocyte organoid model. Nat Commun 17, 2273 (2026). https://doi.org/10.1038/s41467-026-68962-8
الكلمات المفتاحية: فيروس السيتوميجالو, ضمور القنوات الصفراوية, أعضاء قنوات صفراوية مصغرة, التحول الظهاري-الحرشفي, إشارة TGF-بيتا